Mysodelle - vaginaalravivahend (200mcg) - Ravimi omaduste kokkuvõte
Artikli sisukord
RAVIMI OMADUSTE KOKKUVÕTE
1. RAVIMPREPARAADI NIMETUS
Mysodelle 200 mikrogrammi vaginaalravivahend
2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Mysodelle sisaldab 200 mikrogrammi misoprostooli.
Misoprostooli keskmine vabanemiskiirus in vivo on ligikaudu 7 mikrogrammi/tunnis 24 tunni jooksul. Toimeaine vabaneb Mysodelle tupes olemise ajal.
INN. Misoprostolum.
Teadaolevat toimet omav abiaine: 0,13 mg butüülhüdroksüanisooli annuse kohta (vt lõik 4.4).
Abiainete täielik loetelu vt lõik 6.1.
3. RAVIMVORM
Vaginaalravivahend.
Ravivahend, mis koosneb nööriga polüestertaskust, milles asetseb polümeerkapsel. Polümeerkapsel on ristkülikukujuline, ümardatud nurkadega, värvuselt tuhmkollane, poolläbipaistev, bioloogiliselt lagunematu. Mõõdud: pikkus ligikaudu 30 mm, laius 10 mm ja paksus 0.8 mm.
Mysodelle paisub niiskuse toimel.
4. KLIINILISED ANDMED
4.1 Näidustused
Sünnituse esilekutsumiseks ebaküpse emakakaelaga naistel alates 36. rasedusnädalast, kellel on kliiniliselt näidustatud sünnituse esilekutsumine.
4.2 Annustamine ja manustamisviis
Annustamine
Mysodelle 200 mikrogrammi on toimeainet kontrollitult vabastav süsteem, mis vabastab misoprostooli kiirusega ligikaudu 7 mikrogrammi/tunnis 24 tunni jooksul.
Maksimaalne soovitatav annus on üks Mysodelle vaginaalravivahend (200 mikrogrammi).
Mysodelle tuleb eemaldada:
- sünnitustegevuse alguses (emakakael peaks olema avanenud vähemalt 4 cm olenemata kontraktsioonide sagedusest või regulaarsete, tugevate emaka kokkutõmmete korral, st 3 või enam
kontraktsiooni 10 minuti jooksul kestusega vähemalt 45 sekundit, mille tulemusena emakakael lüheneb ja avaneb);
-juhul kui emaka kokkutõmbed kestavad liiga pikka aega või on liiga sagedased;
-juhul kui esineb oht lootele või
-kui paigaldamisest on möödunud 24 tundi.
Kui Mysodelle kukub välja, ei tohi seda asendada.
Kui järgnevalt manustatakse oksütotsiini, on soovitatav pärast vaginaalravivahendi eemaldamist oodata vähemalt 30 minutit (vt lõik 4.5).
Lapsed
Mysodelle ohutus ja efektiivsus rasedatel naistel vanuses alla 18 aastat ei ole tõestatud. Andmed puuduvad.
Manustamisviis
Mysodelle’t võib manustada ainult haigla sünnitusabi spetsialist, kui on olemas loote ja emaka jälgimiseks vajalikud vahendid. Enne Mysodelle kasutamist tuleb emakakaela seisundit hoolikalt hinnata. Pärast paigaldamist jälgida hoolikalt emaka aktiivsust ja loote seisundit.
Mysodelle on pakendatud alumiiniumfooliumist kotikestesse, mida tuleb hoida sügavkülmas. Ei vaja sulatamist enne kasutamist.
Fooliumkotikese ühel poolel on „rebimise märk“. Avage pakend rebimise märgi kohast kotikese ülaosas. Ärge kasutage kääre või muid teravaid esemeid, mis võivad ravivahendit vigastada.
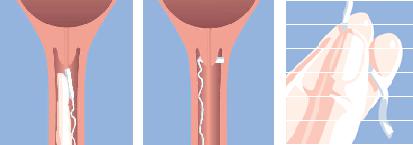
Paigaldage Mysodelle sügavale tupevõlvi tagumisse ossa (joonis a). Sügavale tagumisse tupevõlvi lükkamise järgselt tuleb seda pöörata 90°, et see paikneks risti tagumise tupevõlviga (joonis b). Paigaldamise abistamiseks võib vajadusel kasutada vees lahustuvaid libesteid.
Joonis a. |
Joonis b. |
Joonis c. |
Peale vaginaalravivahendi paigaldamist võib kääridega lõigata nööri lühemaks, kuid tuleb olla kindel, et tupest jääb välja piisavalt nööri, et ravivahendi saab hiljem eemaldada.
Patsient peab jääma peale vaginaalravivahendi paigaldamist 30 minutiks voodisse ja pärast seda võib ta jätta ambulatoorsele jälgimisele. Jälgida, et Mysodelle ei tule kogemata välja tualetis käimisel ega vaginaalsel läbivaatusel.
Eemaldamine
Mysodelle eemaldamiseks tõmmake ettevaatlikult ravivahendit nöörist (joonis c).
Toimeainet sisaldav osa EI TOHIKS KUNAGI eemalduda ilma ravivahendita.
Mysodelle ravimvormi puhul vabaneb toimeaine eelnevalt kindlaksmääratud moel, ta paisub niiskes keskkonnas, mille tulemusena ravim vabaneb. Sisestamise järgselt Mysodelle paisub 2...3 korda võrreldes originaalsuurusega ja muutub painduvaks. Peale eemaldamist kontrollige kas kogu vahend (kapsel ja nööriga tasku) on tupest eemaldatud.
4.3 Vastunäidustused
Mysodelle on vastunäidustatud:
•kui esineb ülitundlikkus toimeaine või lõigus 6.1 loetletud ravimi mis tahes abiaine suhtes
•kui sünnitegevus on alanud
•kui on kahtlus, et loode on ohus enne sünnituse induktsiooni (nt ebaõnnestunud
•kui patsiendile antakse oksütotsiini sisaldavaid ravimeid ja/või teisi sünnitegevust indutseerivaid ravimeid (vt lõik 4.4)
•kui on tõendeid emakaarmile, mis on tingitud varasemast emaka või emakakaela operatsioonist, nt keiserlõikest
•kui esineb emaka anomaaliaid (nt kahesarveline emakas)
•kui esineb placenta praevia või on esinenud selle raseduse jooksul pärast 24. rasedusnädalat emaka seletamatu verejooks
•vale looteasendi (malpresentatsioon) korral
•kui esinevad koorionamnioniidi sümptomid ning vajalikku ravi ei ole eelnevalt määratud
•enne 36. rasedusnädalat.
4.4 Erihoiatused ja ettevaatusabinõud kasutamisel
Mysodelle võib põhjustada tugevat emaka stimulatsiooni, kui seda ei eemaldata sünnitegevuse alguses (vt lõik 4.9).
Kui emaka kontraktsioonid on pikaajalised või ülemäärased või sünnituse käigus tekib oht emale või lapsele, eemaldage vaginaalravivahend. Juhul kui ülemäärased kontraktsioonid jätkuvad pärast ravimi eemaldamist, peaks kaaluma tokolüütilise ravi kasutamist.
Preeklampsiaga rasedatel tuleb välistada oht lootele (vt lõik 4.3). III faasi uuringusse
Mysodelle’t ei ole uuritud naistel, kelle lootekott on rebenenud rohkem kui 48 tundi tagasi enne Mysodelle paigaldamist.
Rasedatel, kellel on
Mysodelle tuleb eemaldada enne oksütotsiini manustamist. Oodake vähemalt 30 minutit pärast Mysodelle eemaldamist enne oksütotsiini manustamist (vt lõigud 4.2, 4.3 ja 4.5).
Mysodelle’t on uuritud ainult üksikraseduste korral, kus loode on pea eesseisus. Mitmikraseduste korral ei ole uuringuid läbi viidud. Mysodelle’t ei ole uuringutes kasutatud naistel, kellel on olnud 3 eelnevat vaginaalset sünnitust raseduse kestusega üle 24 rasedusnädala.
Mysodelle’t tohib kasutada ainult kliiniliselt näidustatud sünnituse esilekutsumiseks.
Mysodelle’t tuleb kasutada ettevaatusega patsientidel, kellel on emakkaela küpsus modifitseeritud Bishopi skaala järgi > 4.
Mysodelle teine annus ei ole soovitatav, sest teise annuse toimet ei ole uuritud.
Füsioloogilise või farmakoloogilise meetodi abil esile kutsutud sünnitustel on patsientidel kirjeldatud sünnitusjärgse intravaskulaarse koagulatsiooni suurenenud riski.
Butüülhüdroksüanisooli kasutatakse võrkstruktuuriga hüdrogeelpolümeeris antioksüdandina. Seda võib preparaadis esineda jälgedena. Butüülhüdroksüanisool võib põhjustada nahareaktsioone (nt kontaktdermatiiti) või silmade ja limaskestade ärritust.
4.5 Koostoimed teiste ravimitega ja muud koostoimed
Koostoimeid Mysodelle’ga ei ole uuritud.
Oksütotsiini ja teiste sünnitegevust indutseerivate ravimite samaaegne kasutamine on vastunäidustatud võimaliku suurenenud uterotoonilise toime tõttu (vt lõigud 4.2, 4.3 ja 4.4).
Kui Mysodelle ei avaldanud nähtavat ebasoodsat mõju, siis manustati rasedatele kliinilistes uuringutes vajadusel peale Mysodelle eemaldamist teisi prostaglandiine sisaldavaid preparaate. Nende preparaatide manustamise ja Mysodelle eemaldamise vahele pidi jääma üks tund.
4.6 Fertiilsus, rasedus ja imetamine
Fertiilsus
Rottidega tehtud fertiilsuse ja varase embrüonaalse arengu uuringutes on tõendeid misoprostooli võimalikust kahjulikust toimest implantatsioonile, vaatamata sellele ei ole see oluline Mysodelle näidustusejärgsel kasutamisel (vt lõik 5.3).
Rasedus
Mysodelle’t uuriti rasedatel ≥ 36. rasedusnädalast.
Mysodelle’t ei tohi kasutada enne 36. rasedusnädalat (vt lõik 4.3).
Imetamine
Misoprostoolhappe koguseid, mis erituvad ternespiima või rinnapiima pärast Mysodelle kasutamist, ei ole uuritud.
Misoprostoolhapet on leitud rinnapiimas pärast misoprostooli tablettide suukaudset manustamist.
Pärast Mysodelle eemaldamist on misoprostoolhappe keskmine poolväärtusaeg plasmas ligikaudu 40 minutit. Pärast viiekordset poolväärtusaega, st ligikaudu 3 tunni pärast, on misoprostoolhappe tase ema vereplasmas ebaoluline. Misoprostoolhape võib erituda ternespiima ja rinnapiima, kuid kogused
on väga väikesed ja püsimise periood väga lühike, mistõttu ei ole takistatud rinnaga toitmine. Kliiniliste uuringute ajal ei täheldatud Mysodelle’l mingit mõju rinnapiima saavatele vastsündinutele.
4.7 Toime reaktsioonikiirusele
Ei ole asjakohane.
4.8 Kõrvaltoimed
Kliiniliste uuringute kogemused
Ohutusprofiili kokkuvõte
Kõrvaltoimete profiil tabelis 1 põhineb viiel läbi viidud kliinilisel uuringul Mysodelle’ga, kus osales 874 rasedat ajalise rasedusega. Kõige sagedasemad kõrvaltoimed on ebanormaalsed emaka kontraktsioonid, loote südame löögisageduse häire ja ebanormaalne sünnitus, mis mõjub lootele.
Tabel 1 Kliinilistes uuringutes täheldatud kõrvaltoimed
Organsüsteemi |
Väga |
Sage |
|
klass |
sage |
(≥1/100 kuni <1/10) |
(≥1/1000 kuni <1/100) |
|
(≥1/10) |
||
|
|
|
|
Närvisüsteemi |
|
|
|
häired |
|
|
entsefalopaatia * |
|
|
|
|
Südame häired |
|
Loote südame löögisageduse |
|
|
|
häire† |
|
|
|
|
|
Respiratoorsed, |
|
|
Vastsündinu respiratoorne |
rindkere ja |
|
|
depressioon |
mediastiinumi |
|
|
|
häired |
|
|
|
|
|
|
Vastsündinu respiratoorse distressi |
|
|
|
sündroom* |
|
|
|
Vastsündinu mööduv tahhüpnoe* |
|
|
|
|
Seedetrakti häired |
|
|
Iiveldus |
|
|
|
Oksendamine |
|
|
|
|
Naha ja |
|
|
Lööve |
nahaaluskoe |
|
|
|
kahjustused |
|
|
|
|
|
|
|
Rasedus, |
|
Ebanormaalne sünnitus, mis |
Sünnituseelne verejooks |
sünnitusjärgsed ja |
|
|
|
Organsüsteemi |
Väga |
Sage |
|
klass |
sage |
(≥1/100 kuni <1/10) |
(≥1/1000 kuni <1/100) |
|
(≥1/10) |
||
|
|
|
|
perinataalsed |
|
mõjub lootele†† |
Loote atsidoos* |
seisundid |
|
Mekoonium lootevedelikus |
Sünnitusjärgne verejooks |
|
|
||
|
|
Ebanormaalsed emaka |
Enneaegne platsenta irdumine |
|
|
kontraktsioonid††† |
Emaka hüpertoonus |
|
|
|
|
|
|
|
|
Reproduktiivse |
|
|
Genitaalide sügelus |
süsteemi ja |
|
|
|
rinnanäärme häired |
|
|
|
|
|
|
|
Uuringud |
|
|
Madal Apgari hinne* |
|
|
|
Vererõhu tõus |
|
|
|
|
Vigastus, mürgistus |
|
|
Emaka rebend |
ja protseduuri |
|
|
|
tüsistused |
|
|
|
|
|
|
|
Tabel hõlmab kõrvaltoimeid uuringutest
* Vastsündinute kõrvaltoimed.
† Loote südame löögisageduse häire hõlmas järgmisi seisundeid: loote südametoonide kõrvalekalded, loote bradükardia, loote tahhükardia, seletamatu normaalse variaabluse puudumine, loote südame löögisageduse aeglustumine, loote südame löögisageduse detseleratsioon, liiga varane või hiline detseleratsioon, variaabel detseleratsioonid, prolongeeritud detseleratsioonid.
†† Ebanormaalne sünnitus, mis mõjutab loodet, hõlmas järgmisi seisundeid: emaka tahhüsüstoolsus või emaka hüpertoonus, millega kaasnes loote südame löögisageduse häire.
††† Ebanormaalsed emaka kontraktsioonid hõlmasid ka emaka tahhüsüstoolsust.
Keskses Mysodelle uuringus
Võimalikest kõrvaltoimetest teavitamine
Ravimi võimalikest kõrvaltoimetest on oluline teavitada ka pärast ravimi müügiloa väljastamist. See võimaldab jätkuvalt hinnata ravimi kasu/riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest www.ravimiamet.ee kaudu.
4.9 Üleannustamine
Puuduvad kogemused rohkem kui ühe annuse Mysodelle kasutamise kohta. Üleannustamise oht on väike, sest Mysodelle on toimeainet kontrollitult vabastav süsteem, mida saab vajadusel eemaldada. Kui Mysodelle unustatakse eemaldada sünnitegevuse alguses, võivad tekkida prostaglandiinide üleannustamise sümptomid (liiga tugev emaka stimulatsioon). Kui see juhtub, siis tuleb Mysodelle eemaldada ja toimida vastavalt kohalikele juhistele.
5. FARMAKOLOOGILISED OMADUSED
5.1 Farmakodünaamilised omadused
Farmakoterapeutiline rühm: teised günekoloogias kasutatavad ained, emakasse toimivad ained, prostaglandiinid,
Toimemehhanism
Misoprostool on sünteetiline prostaglandiin E1 (PGE) analoog, loomulikult esinev emakasse toimiv ühend. Prostaglandiinide E ja F mõjul tõuseb in vitro küülikutega tehtud katsetes emakakaela fibroblastides kollagenaasi aktiivsus, samuti emakakael küpseb ja suurenevad emaka kontraktsioonid in vivo. Nimetatud farmakodünaamilised toimed on olulised Mysodelle kliinilise toime saavutamiseks.
PGE analoogidel on veel mitmeid toimeid, nt bronhide ja trahhealihaste lõdvestamine, limaerituse suurendamine, maohappe ja pepsiini sekretsiooni vähendamine, neerude verevarustuse suurendamine ning tsirkuleeriva adenokortikotroopse hormooni ja prolaktiini kontsentratsioonide suurendamine. Nimetatud farmakodünaamilised toimed ei oma olulist kliinilist tähtsust lühiajalise ravi korral.
Kliiniline efektiivsus ja ohutus
III faasi uuring
Tabelis 2 on toodud peamised esmased ja teisesed nimetatud uuringu tulemusnäitajad.
Tabel 2
|
Mysodelle |
PROPESS® |
|
|
200 mikrogrammi |
10mg |
|
|
(N=678) |
(N=680) |
|
Vaginaalse sünnituse mediaanne aeg, mis |
|
|
|
lõppes lapse sünniga |
21,5h** |
32,8h** |
p < 0,001 |
Sünnitamata naised |
29,2 h (n=441) |
43,1 h (n=451) |
p < 0,001 |
|
|||
Sünnitanud naised |
13,4 h (n=237) |
20,1 h (n=229) |
p < 0,001 |
|
|||
|
|
|
|
Keiserlõikega lõppenud sünnitused (n %) |
176 (26,0%) |
184 (27,1%) |
p = 0,646 |
Sünnitamata naised |
|
|
|
|
152 (34,5%) |
168 (37,3%) |
p = 0,386 |
Sünnitanud naised |
|
|
|
|
|
|
|
|
24 (10,1%) |
16 (7,0%) |
p = 0,226 |
|
|
|
|
|
|
sünnituse mediaanne aeg* (vaginaalne ja |
† |
† |
|
|
keiserlõige kokku) |
18,3h |
27,3h |
p < 0,001 |
|
|
|
|||
|
|
|
|
|
Mediaanne aeg sünnitegevuse alguseni |
†† |
†† |
|
|
12,1h |
18,6h |
p < 0,001 |
||
Uuritavate koguarv, kellele manustati |
324 (48,1%) |
497 (74,1%) |
p < 0,001 |
|
sünnituseelselt oksütotsiini [n (%)] |
(N=674) |
(N=671) |
||
|
||||
|
|
|
|
* Uuritavaid, kellele tehti keiserlõige, kes lülitati uuringust välja enne sünnitust või kes ise keeldusid uuringus osalemast, jälgiti milline oli pikim aeg ravimi manustamisest keiserlõikeni või sünnituseni ja sünnitusjärgse perioodi lõpuni (Kaplan Meieri järgi).
** Mediaanne aeg vaginaalse sünnituseni (ainult vaginaalselt sünnitanud isikutel): Mysodelle, 200 mikrogrammi: 16,6 tundi; PROPESS® 10 mg: 25,1 tundi
† Igasuguse sünnituse mediaanne aeg: Mysodelle, 200 mikrogrammi: 18,2 tundi; PROPESS® 10 mg: 27,2 tundi †† Mediaanne aeg sünnitegevuse alguseni: Mysodelle, 200 mikrogrammi: 12,0 tundi; PROPESS® 10 mg: 18,0 tundi
Lapsed
Euroopa Ravimiamet ei kohusta esitama Mysodelle’ga läbi viidud uuringute tulemusi sünnituse esilekutsumise suhtes laste kõikide alarühmade kohta kinnitatud näidustuse korral (teave lastel kasutamise kohta: vt lõik 4.2).
5.2 Farmakokineetilised omadused
Misoprostool, mis on ester, metaboliseerub kiiresti aktiivseks metaboliidiks misoprostoolhappeks. Plasmast on tuvastatav ainult misoprostoolhape. Hape metaboliseerub enne uriiniga eritumist inaktiivseteks metaboliitideks dinoor- ja tetranoorhappeks.
Mitterasedatel naistel Mysodelle manustamisel on toimeaine keskmiseks kontrollitud vabanemiskiiruseks in vivo ligikaudu 7 mikrogrammi tunnis 24 tunni jooksul. Uuringus, kus osales 24 ajalise sünnitusega lõppenud rasedusega naist, oli osalejatel CMAX mediaan 45,8 pg/ml ja TMAX mediaan 4 tundi.
Poolväärtusaeg mediaan (pärast eemaldamist) oli ligikaudu 40 minutit.
Misoprostoolhape seondub plasmavalkudega vähem kui 90% ulatuses ja terapeutiliste annuste manustamisel ei sõltu see ravimi plasmakontsentratsioonist.
5.3 Prekliinilised ohutusandmed
Mysodelle toimeaine, misoprostooli, farmakoloogilise ohutuse, korduvtoksilisuse, genotoksilisuse ja kartsinogeensuse mittekliinilised uuringud ei ole näidanud kahjulikku toimet inimesele.
Misoprostoolil ei täheldatud teratogeenset toimet rottidele annustes kuni 10 mg/kg/päevas. Küülikutel täheldati loodete ribide arvu suurenemist annuses 1 mg/kg/päevas, mis on tõenäoliselt seotud selle annuse toksilisusega emasloomal. Peaaegu letaalse annuse manustamisel hiirtele täheldati erinevaid loote defekte. Rottidega tehtud fertiilsuse ja varase embrüonaalse arengu uuringutes on tõendeid misoprostooli võimalikust kahjulikust mõjust implantatsioonile. Annus, millest allapoole kõrvaltoimeid ei täheldatud, oli 0,4 mg/kg päevas. Eespool mainitud hiirtel ja rottidel tehtud järeldused ei ole Mysodelle kasutamisel probleemiks, kuna preparaati ei tohi kasutada enne 36. rasedusnädalat.
Rottidega läbi viidud perinataalsetes / postnataalsetes toksilisuse uuringutes suukaudse misoprostooliga 1,0 mg/kg päevas ei tuvastatud toimet reproduktiivsele süsteemile. Võrreldes rottide ja inimeste kineetilistes uuringutes saadud ekspositsiooni väärtusi, tehti Mysodelle puhul (mida
manustati annuses 200 mikrogrammi misoprostooli vaginaalravivahendi miniatuurse vormina) kindlaks ohutusfaktor 20.
Tiinetel rottidel ei tuvastatud Mysodelle kasutamisel lokaalseid ärritusnähtusid tupes või emakakaelal.
Kasutades standardseid in vitro ja in vivo teste ja tuginedes avaldatud toksilisuse andmetele, ei ole inimestele
6. FARMATSEUTILISED ANDMED
6.1. Abiainete loetelu
Võrkstruktuuriga hüdrogeelpolümeer (koosneb makrogoolist, 1,2,6 - heksanetrioolist ja
Butüülhüdroksüanisool Polüesterravivahend (kootud polüesternöör)
6.2 Sobimatus
Ei kohaldata.
6.3 Kõlblikkusaeg
3 aastat.
6.4 Säilitamise eritingimused
Hoida sügavkülmas
6.5 Pakendi iseloomustus ja sisu
1 x 200 mikrogrammi vaginaalravivahend
5 x 200 mikrogrammi vaginaalravivahend
5 x 200 mikrogrammi vaginaalravivahend (multipakend).
Iga vaginaalravivahend on pakendatud kuivatusainet sisaldavasse lamineeritud alumiiniumfooliumist kotikesse, mis on pakendatud pappkarpi.
Kõik pakendi suurused ei pruugi olla müügil.
6.6 Erihoiatused ravimpreparaadi hävitamiseks ja käsitlemiseks
Mysodelle tuleb võtta sügavkülmast ja eemaldada lamineeritud alumiiniumfooliumist kotikesest vahetult enne paigaldamist.
Kasutamata ravimpreparaat või jäätmematerjal tuleb hävitada vastavalt kohalikele nõuetele. Ravimpreparaat tuleb pärast tupest eemaldamist ära visata.
7. MÜÜGILOA HOIDJA
Ferring GmbH
Wittland 11
Saksamaa
8. MÜÜGILOA NUMBER
9. ESMASE MÜÜGILOA VÄLJASTAMISE/MÜÜGILOA UUENDAMISE KUUPÄEV
25.11.2013
10. TEKSTI LÄBIVAATAMISE KUUPÄEV
november 2015
