Fluarix - süstesuspensioon (1annust 0.5ml) - Ravimi omaduste kokkuvõte
Artikli sisukord
RAVIMI OMADUSTE KOKKUVÕTE
1.RAVIMPREPARAADI NIMETUS
Fluarix, süstesuspensioon süstlis.
Gripivaktsiin (inaktiveeritud purustatud viirus)
2.KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Gripiviiruse (inaktiveeritud, purustatud) järgmised tüved*:
A/California/7/2009 (H1N1)pdm09 - sarnane tüvi (A/Christchurch/16/2010,
15 mikrogrammi HA**
A/Hong Kong/4801/2014 (H3N2) - sarnane tüvi (A/Hong Kong/4801/2014, NYMC
15 mikrogrammi HA**
B/Brisbane/60/2008 – sarnane tüvi (B/Brisbane/60/2008, metsikut tüüpi)
15 mikrogrammi HA**
0,5 ml annuse kohta
* kasvatatud hea tervisega kanakarjast saadud viljastatud kanaembrüotel. ** hemaglutiniin.
Vaktsiin vastab Maailma Terviseorganisatsiooni (WHO) soovitustele (põhja poolkeral) ja Euroopa Liidu soovitusele hooajaks 2016/2017.
Teadaoleva toimega abiained
See ravim sisaldab ligikaudu 3,75 mg naatriumkloriidi ja ligikaudu 1,3 mg dinaatriumfosfaatdodekahüdraati annuse kohta (vt lõik 4.4).
See ravim sisaldab ligikaudu 0,2 mg kaaliumdivesinikfosfaati ja ligikaudu 0,1 mg kaaliumkloriidi annuse kohta (vt lõik 4.4).
Fluarix võib sisaldada jälgedena munavalke (näiteks ovalbumiin, kanavalgud), formaldehüüdi, gentamütsiinsulfaati või naatriumdeoksükolaati, mida kasutatakse tootmisprotsessis (vt lõik 4.3).
Abiainete täielik loetelu vt lõik 6.1.
3.RAVIMVORM
Süstesuspensioon süstlis.
Suspensioon on värvitu või kergelt opalestseeruv.
4.KLIINILISED ANDMED
4.1Näidustused
Gripiprofülaktika, iseäranis nendel, kellel esineb suurem risk kaasuvate tüsistuste tekkeks.
Fluarix on näidustatud täiskasvanutele ja lastele vanuses alates 6 kuud.
Fluarix´i kasutamisel tuleb lähtuda kohalikest kehtivatest immuniseerimisjuhistest.
4.2Annustamine ja manustamisviis
Annustamine
Täiskasvanud: 0,5 ml
Lapsed
Lapsed alates
Lapsed 6
Lastele vanuses < 9 aastat, keda ei ole varem gripi vastu vaktsineeritud, peab teise annuse manustama vähemalt
Alla 6 kuu vanused lapsed: Fluarix’i ohutus ja efektiivsus alla 6 kuu vanustel lastel ei ole tõestatud. Andmed puuduvad.
Manustamisviis
Vaktsiini manustatakse lihasesse või sügavale naha alla.
Enne ravimi käsitlemist või manustamist tuleb järgida ettevaatusabinõusid.
Ravimpreparaadi manustamiskõlblikuks muutmise juhised vt lõik 6.6.
4.3Vastunäidustused
Ülitundlikkus toimeainete või lõigus 6.1 loetletud mis tahes abiainete või jääkide suhtes, näiteks nagu munajäägid (ovalbumiin, kanavalgud), formaldehüüd, gentamütsiinsulfaat või naatriumdeoksükolaat.
Kõrge palavikuga kulgevate haiguste või ägedate infektsioonide korral tuleb vaktsineerimine edasi lükata.
4.4Erihoiatused ja ettevaatusabinõud kasutamisel
Nagu kõikide süstitavate vaktsiinide puhul, peab kättesaadav olema adekvaatne meditsiiniline abi ning järelevalve, kui vaktsineerimisega seoses peaks tekkima harvaesinev anafülaktiline reaktsioon.
Vaktsiini ei tohi mitte mingil tingimusel manustada veeni.
Vaktsiini manustamine immuunsupressiivravi saavatele või immuunpuudulikkusega patsientidele võib jääda toimeta.
Pärast, või isegi enne, ükskõik missugust vaktsineerimist võib tekkida psühhogeense reaktsioonina nõelatorkele sünkoop (minestamine), eriti noorukitel. Sellega võivad kaasneda mitmed neuroloogilised nähud, näiteks mööduvad nägemishäired, paresteesia ja
Mõju seroloogilistele uuringutele
Vt lõik 4.5.
See ravim sisaldab vähem kui 1 mmol naatriumi (23 mg) annuse kohta, st on sisuliselt naatriumivaba.
See ravim sisaldab vähem kui 1 mmol kaaliumi (39 mg) annuse kohta, st on sisuliselt kaaliumivaba.
4.5Koostoimed teiste ravimitega ja muud koostoimed
Fluarix’i võib manustada samaegselt teiste vaktsiinidega, kasutades erinevaid süstekohti erinevatel jäsemetel. Võib suureneda kõrvaltoimete esinemissagedus.
Immuunvastus võib olla puudulik kui patsient saab samaegselt immunosupressiivset ravi.
Pärast gripivastast vaktsineerimist võivad seroloogilised uuringud
4.6Fertiilsus, rasedus ja imetamine
Rasedus
Inaktiveeritud gripivaktsiini võib kasutada raseduse igas staadiumis. Rohkem andmeid ohutuse kohta on olemas teise ja kolmanda trimestri kohta, võrreldes esimese trimestriga. Siiski, andmed gripivaktsiinide kasutamise kohta mujal maailmas ei näita mingit ebasoodsat mõju lootele ja emale, mida võiks seostada vaktsiiniga.
Imetamine
Fluarix’i võib kasutada imetamise ajal.
Fertiilsus
Fertiilsuse kohta andmed puuduvad.
4.7Toime reaktsioonikiirusele
Fluarix ei mõjuta või mõjutab ebaoluliselt autojuhtimise ja masinate käsitsemise võimet.
4.8 Kõrvaltoimed
Ohutusprofiili kokkuvõte
Kliiniliste uuringute jooksul on täheldatud järgmiseid kõrvaltoimed vastavalt järgmistele esinemissagedustele:
Väga sage (≥1/10)
Sage (≥1/100 kuni <1/10)
Kõrvaltoimete loetelu
Organsüsteemi klass |
Väga sage |
Sage |
|
|
≥1/10 |
≥1/100 kuni <1/10 |
≥1/1000 kuni <1/100 |
Närvisüsteemi häired |
|
Peavalu* |
|
Naha ja nahaaluskoe |
|
Higistamine* |
|
kahjustused |
|
|
|
|
Lihas- ja liigesvalu* |
|
|
kahjustused |
|
|
|
Üldised häired ja |
|
Palavik, üldine halb |
|
manustamiskoha |
|
enesetunne, |
|
reaktsioonid |
|
külmavärinad, väsimus. |
|
|
|
Lokaalsed reaktsioonid: |
|
|
|
punetus, turse, valu, |
|
|
|
verevalum, induratsioon* |
|
* Need kõrvaltoimed mööduvad tavaliselt 1…2 päeva jooksul ilma ravita. Lapsed
Fluarix’i manustati tervete
Kõikides vanuserühmades oli kõige sagedamini teatatud lokaalne kõrvaltoime pärast vaktsineerimist valu, mille esinemissagedus oli 31,9% kuni 52.7% juhtudest.
Lastel vanuses kuni 6 aastat oli kõige tavalisem teatatud üldine kõrvaltoime ärrituvus, mis esines 8,1% kuni 23,2% juhtudest.
Vanuserühmas 6 aastased ja vanemad oli kõige sagedasem üldine kõrvaltoime lihasvalu, mis esines 10,7% kuni 24,6% juhtudest.
Selles vanusegrupis täheldati järgmisi kõrvaltoimeid.
Organsüsteemi klass |
Väga sage |
Sage |
|
|
≥1/10 |
≥1/100 kuni <1/10 |
≥1/1000 kuni <1/100 |
Ainevahetus ja |
Söögiisu kaotus |
|
|
toitumishäired |
|
|
|
Psühhiaatrilised häired |
Ärrituvus |
|
|
Närvisüsteemi häired |
Uimasus, peavalu |
|
|
Seedetrakti häired |
|
Seedetrakti nähud |
|
Liiigesvalu, lihasvalu |
|
|
|
kahjustused |
|
|
|
Üldised häired ja |
Palavik, väsimus. |
Palavik, |
|
manustamiskoha |
Paiksed reaktsioonid: |
külmavärinad |
|
reaktsioonid |
punetus, turse, valu. |
|
|
teatati lastel vanuses 6 kuud kuni 17 aastat
teatati lastel vanuses 6 kuud kuni <6 aastat
teatati lastel vanuses 6...17 aastat
Turuletulekujärgsed andmed
Turuletulekujärgselt on lisaks kliiniliste uuringute käigus täheldatud kõrvaltoimetele esinenud järgmisi:
Vere ja lümfisüsteemi häired:
Mööduv trombotsütopeenia, mööduv lümfadenopaatia.
Immuunsüsteemi häired:
Allergilised reaktsioonid (sh sümptomid nagu konjunktiviit), harva šokk, angioödeem.
Närvisüsteemi häired:
Neuralgia, paresteesia, febriilsed krambid, neuroloogilised häired nagu entsefalomüeliit, neuriit ja Guillain Barré sündroom.
Vaskulaarsed häired:
Vaskuliit, väga harva koos mööduva neerufunktsiooni häirega.
Naha ja nahaaluskoe kahjustused:
Üldised nahareaktsioonid sh pruritus, urtikaaria või mittespetsiifiline lööve.
Võimalikest kõrvaltoimetest teavitamine
Ravimi võimalikest kõrvaltoimetest on oluline teavitada ka pärast ravimi müügiloa väljastamist. See võimaldab jätkuvalt hinnata ravimi kasu/riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest www.ravimiamet.ee kaudu.
4.9Üleannustamine
Üleannustamisel ei ole tõenäoliselt ebasoodsat toimet.
5.FARMAKOLOOGILISED OMADUSED
5.1Farmakodünaamilised omadused
Farmakoterapeutiline rühm: gripivaktsiin,
Kaitseefekt saabub tavaliselt 2…3 nädalat pärast vaktsineerimist. Vaktsinatsioonijärgne immuunsus homoloogiliste tüvede või vaktsiinitüvedega väga sarnaste tüvede suhtes varieerub, kuid püsib tavaliselt 6…12 kuud.
5.2Farmakokineetilised omadused
Ei ole asjakohane.
5.3Prekliinilised ohutusandmed
Farmakoloogilise ohutuse, ägeda toksilisuse, lokaalse taluvuse, korduvtoksilisuse, reproduktsiooni- ja arengutoksilisuse mittekliinilised uuringud ei ole näidanud kahjulikku toimet inimesele.
6.FARMATSEUTILISED ANDMED
6.1Abiainete loetelu
Naatriumkloriid, dinaatriumfosfaatdodekahüdraat, kaaliumdivesinikfosfaat, kaaliumkloriid, magneesiumkloriidheksahüdraat,
6.2Sobimatus
Sobivusuuringute puudumise tõttu ei tohi seda ravimpreparaati teiste ravimitega segada.
6.3Kõlblikkusaeg
1 aasta.
6.4Säilitamise eritingimused
Hoida külmkapis (2ºC...8°C).
Mitte lasta külmuda.
Hoida originaalpakendis, valguse eest kaitstult.
6.5Pakendi iseloomustus ja sisu
Süstesuspensioon 0,5 ml
-kinnitatud nõelaga: 1, 10 või 20 tk pakendis
-ühe eraldi nõelaga: 1, 10 või 20 tk pakendis
-kahe eraldi nõelaga: 1 tk pakendis
-nõelata: 1, 10 või 20 tk pakendis
Kõik pakendi suurused ei pruugi olla müügil.
6.6Erihoiatused ravimpreparaadi hävitamiseks ja käsitlemiseks
Enne manustamist peab vaktsiin soojenema toatemperatuurini.
Enne kasutamist loksutada. Enne manustamist kontrollida visuaalselt.
Kui on näidustatud 0,5 ml annuse manustamine, tuleb süstida kogu süstli sisu.
Vaktsiini 0,25 ml annuse manustamise juhised lastele 6 elukuust kuni 35 elukuuni.
Kui on näidustatud 0,25 ml annuse manustamine, tuleb hoida süstel püstises asendis ja väljutada pool selle sisust, kuni kolb jõuab märgistusjooneni süstlil. Süstlisse allesjäänud 0,25 ml kogus tuleb süstida.
Vaktsiini manustamise juhised ilma fikseeritud nõelata süstlis.
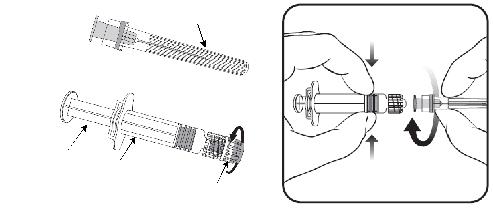
Selleks, et kinnitada nõel süstlale, vaadake allpool olevat pilti 1.
Pilt 1
Nõel
Nõelakaitse
Süstel
Süstli kolb |
Süstli silinder |
|
|
Süstli kate
1.Hoides süstli silindrit ühes käes (vältige süstla kolvist kinni hoidmist), keerake maha süstli kate, keerates seda vastupäeva.
2.Nõela kinnitamiseks süstli külge, keerake nõela päripäeva, kuni tunnete, et see on kinnitunud (vt pilt 1).
3.Eemaldage nõelakaitse, mis võib mõnikord olla tugevalt kinni.
4.Manustage vaktsiin.
Kasutamata ravimpreparaat või jäätmematerjal tuleb hävitada vastavalt kohalikele nõuetele.
7.MÜÜGILOA HOIDJA
GlaxoSmithKline Biologicals s.a. 89, rue de l´Institut
1330 Rixensart Belgia
8.MÜÜGILOA NUMBER
9.ESMASE MÜÜGILOA VÄLJASTAMISE/MÜÜGILOA UUENDAMISE KUUPÄEV
Müügiloa esmase väljastamise kuupäev: 28.02.1997
Müügiloa viimase uuendamise kuupäev: 14.12.2007
10.TEKSTI LÄBIVAATAMISE KUUPÄEV
juuni 2018
