Ezetrol - tablett (10mg) - Ravimi omaduste kokkuvõte
Artikli sisukord
RAVIMI OMADUSTE KOKKUVÕTE
1.RAVIMPREPARAADI NIMETUS
Ezetrol, 10 mg tabletid
2.KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Iga tablett sisaldab 10 mg esetimiibi.
INN. Ezetimibum
Teadaolevat toimet omav abiaine
Iga tablett sisaldab 55 mg laktoosmonohüdraati.
Abiainete täielik loetelu vt lõik 6.1.
3.RAVIMVORM
Tablett.
Valge või määrdunudvalge kapslikujuline ligikaudu 2,60 mm paksune tablett, mille ühel küljel on pimetrükk „414”.
4.KLIINILISED ANDMED
4.1Näidustused
Primaarne hüperkolesteroleemia
Ezetroli koosmanustamine
Ezetroli monoteraapia on näidustatud lisaks dieedile nendele primaarse (perekondliku ja mitteperekondliku heterosügootse) hüperkolesteroleemiaga patsientidele, kellele ei sobi või kes ei talu statiini.
Kardiovaskulaarsete sündmuste ennetamine
Ezetrol on näidustatud kardiovaskulaarsete sündmuste riski vähendamiseks (vt lõik 5.1) südame isheemiatõvega ja anamneesis ägeda koronaarsündroomiga patsientidel, lisatuna käimasolevale statiinravile või alustatuna samaaegselt statiini manustamisega.
Homosügootne perekondlik hüperkolesteroleemia (HoPH)
Ezetrol manustatuna koos statiiniga on näidustatud lisaks dieedile HoPHga patsientide raviks. Patsiendid võivad saada ka muud täiendavat ravi (nt LDL afereesi).
Homosügootne sitosteroleemia (fütosteroleemia)
Ezetrol on näidustatud lisaks dieedile homosügootse perekondliku sitosteroleemiaga patsientide raviks.
4.2Annustamine ja manustamisviis
Annustamine
Patsient peab olema sobival lipiide langetaval dieedil ning jätkama seda kogu Ezetroli ravi ajal.
1/19
Ravimit manustatakse suu kaudu. Soovitatav annus on üks Ezetroli 10 mg tablett ööpäevas. Ezetroli võib manustada ükskõik millisel kellaajal koos toiduga või ilma.
Ezetroli lisamisel statiinile tuleb jätkata eelnevalt määratud ravi vastava statiini algannusega või juba kindlaks määratud tõstetud annusega. Statiini annus tuleb sellise kombinatsiooni korral üle vaadata.
Kasutamine südame isheemiatõvega ja anamneesis ägeda koronaarsündroomi (ÄKS) sündmusega patsientidel
Kardiovaskulaarsete nähtude
Manustamine koos sapphapete sekvestrantidega
Ezetroli peab manustama kas ≥ 2 tundi enne või ≥ 4 tundi pärast sapphapete sekvestrandi võtmist.
Eakad
Eakatel patsientidel ei ole vaja annuseid kohandada (vt lõik 5.2).
Lapsed
Ravi peab alustama spetsialisti järelevalve all.
Kui Ezetroli manustatakse koos statiiniga, tuleb tutvuda statiini annustamisjuhistega lastele.
Alla
Maksakahjustusega patsiendid
Kerge maksakahjustuse korral
Neerukahjustusega patsiendid
Neerukahjustusega patsientidel ei ole vaja annust kohandada (vt lõik 5.2).
4.3Vastunäidustused
Ülitundlikkus toimeaine või lõigus 6.1 loetletud mis tahes abiainete suhtes.
Ezetroli manustamisel koos statiiniga lugeda vastavat ravimi omaduste kokkuvõtet.
Ezetroli kasutamine koos statiiniga on vastunäidustatud raseduse ja rinnaga toitmise ajal.
Ezetroli kasutamine koos statiiniga on vastunäidustatud ägeda maksahaigusega ja ebaselgel põhjusel püsivalt kõrgete seerumi transaminaaside väärtustega patsientidel.
4.4Erihoiatused ja ettevaatusabinõud kasutamisel
Ezetroli manustamisel koos statiiniga lugeda vastavat ravimi omaduste kokkuvõtet.
Maksaensüümid
Kliinilistes uuringutes on Ezetroli ja statiini samaaegselt saanud patsientidel kirjeldatud transaminaaside tõusu (≥ 3 korral üle normväärtuse ülemise piiri). Ezetroli manustamisel koos
2/19
statiiniga tuleb määrata maksafunktsiooni näitajad ravi alustamisel ning ravi ajal vastavalt statiinravi puhul ettenähtule (vt lõik 4.8).
Uuringus
Ühes kontrollitud kliinilises uuringus, milles randomiseeriti üle 9000 kroonilise neeruhaigusega patsiendi, kes said ööpäevas 10 mg Ezetroli kombinatsioonis 20 mg simvastatiiniga (n = 4650) või platseebot (n = 4620) (jälgimisperioodi mediaan 4,9 aastat), oli transaminaaside järjestikuste tõusude (> 3 korral üle normväärtuse ülemise piiri) esinemissagedus Ezetroli ja simvastatiini kombinatsiooni puhul 0,7% ja platseebo puhul 0,6% (vt lõik 4.8).
Skeletilihased
Ezetroli turuletulekujärgselt on teatatud mõnedest müopaatia ja rabdomüolüüsi juhtudest. Enamik patsiente, kellel tekkis rabdomüolüüs, võtsid samaaegselt Ezetroliga statiini. Kuid rabdomüolüüsi on väga harva teatatud Ezetroli monoteraapiaga ning väga harva, kui Ezetroli on lisatud ravile toimeainetega, milliseid seostatakse suurenenud ohuga rabdomüolüüsi tekkeks. Kui kahtlustatakse müopaatiat põhinedes lihaste haigustunnustele või seda kinnitab kreatiniini fosfokinaasi (CPK) tase, mis on > 10 korda üle normväärtuse ülemise piiri, siis tuleb otsekohe lõpetada Ezetroli, iga statiini ja iga teise sellise toimeaine, mida samaaegselt võetakse, manustamine. Kõiki patsiente, kes alustavad ravi Ezetroliga tuleb teavitada müopaatia tekke ohust ning käskida neil otsekohe teatada igast seletamatust lihasvalust,
Ühes kontrollitud kliinilises uuringus, milles randomiseeriti üle 9000 kroonilise neeruhaigusega patsiendi, kes said ööpäevas 10 mg Ezetroli kombinatsioonis 20 mg simvastatiiniga (n = 4650) või platseebot (n = 4620) (jälgimisperioodi mediaan 4,9 aastat), oli müopaatia/rabdomüolüüsi esinemissagedus Ezetroli ja simvastatiini kombinatsiooni puhul 0,2% ja platseebo puhul 0,1% (vt lõik 4.8).
Maksakahjustusega patsiendid
Kuna mõõduka või raske maksakahjustuse korral ei ole esetimiibi suurenenud mõju toimed teada, siis Ezetroli nendele patsientidele ei soovitata (vt lõik 5.2).
Lapsed
Ezetroli efektiivsust ja ohutust heterosügootse perekondliku või mitteperekondliku hüperkolesteroleemiaga 6 kuni
Ezetroli kasutamist ei ole uuritud alla 6 aasta vanustel patsientidel (vt lõigud 4.2 ja 4.8).
3/19
Koos simvastatiiniga manustatud Ezetroli efektiivsust ja ohutust heterosügootse perekondliku hüperkolesteroleemiaga 10 kuni
Selles piiratud kontrollitud uuringus ei täheldatud üldjuhul mõju kasvule või sugulisele küpsemisele teismelistel poistel või tüdrukutel ega menstruaaltsükli pikkusele tüdrukutel. Samas ei ole uuritud üle 33 nädala kestnud esetimiibravi toimet kasvule ja sugulisele küpsemisele (vt lõigud 4.2 ja 4.8).
Koos simvastatiini 40 mg ületavate ööpäevaste annustega manustatud Ezetroli ohutust ja efektiivsust ei ole uuritud lastel vanuses 10 kuni 17 aastat.
Koos simvastatiiniga manustatud Ezetroli ohutust ja efektiivsust ei ole uuritud alla
Ei ole uuritud
Fibraadid
Ezetroli ohutus ja efektiivsus manustamisel koos fibraatidega ei ole tõestatud.
Kui Ezetroli ja fenofibraati saaval patsiendil kahtlustatakse sapikivitõbe, on näidustatud sapipõie uuringud ja antud ravi tuleb katkestada (vt lõigud 4.5 ja 4.8).
Tsüklosporiin
Ezetroli lisamisel tsüklosporiinile tuleb olla ettevaatlik. Ezetroli ja tsüklosporiini samaaegselt saavatel patsientidel tuleb jälgida tsüklosporiini kontsentratsioone (vt lõik 4.5).
Antikoagulandid
Kui varfariini, mõne teise kumariini rühma antikoagulandi või fluindiooni ravile lisatakse Ezetrol, siis tuleb vastavalt jälgida
Abiaine
Seda ravimit ei tohi kasutada patsiendid, kellel on harva esinev pärilik galaktoosi talumatus, laktaasi vaegus või
4.5Koostoimed teiste ravimitega ja muud koostoimed
Prekliinilistes uuringutes on näidatud, et esetimiib ei indutseeri tsütokroom P450 ravimit metaboliseerivaid ensüüme. Kliiniliselt olulisi farmakokineetilisi koostoimeid ei ole täheldatud esetimiibi ja ravimite vahel, mida teadaolevalt metaboliseerivad järgmised tsütokroomid P450 1A2, 2D6, 2C8, 2C9 ja 3A4 või
Koostoimete kliinilistes uuringutes ei avaldanud esetimiib koosmanustamisel toimet dapsooni, dekstrometorfaani, digoksiini, suukaudsete kontratseptiivide (etünüülöstradiooli ja levonorgestreeli), glipisiidi, tolbutamiidi või midasolaami farmakokineetikale. Koos esetimiibiga manustatud tsimetidiin ei mõjutanud esetimiibi biosaadavust.
Antatsiidid
Samaaegne antatsiidi manustamine vähendas esetimiibi imendumist, kuid ei mõjutanud esetimiibi biosaadavust. Esetimiibi vähenenud imendumist ei peeta kliiniliselt oluliseks.
Kolestüramiin
Samaaegne kolestüramiini manustamine vähendas kogu esetimiibi (esetimiib + esetimiibglükuroniid) keskmist kontsentratsioonikõvera alust pindala (AUC) ligikaudu 55%. Ezetroli lisamisel kolestüramiinile võib selle koostoime tõttu väikese tihedusega lipoproteiin kolesterooli
4/19
langus olla oodatust väiksem (vt lõik 4.2).
Fibraadid
Fenofibraati ja Ezetroli kasutavate patsientide puhul peavad arstid olema teadlikud sapikivitõve ja sapipõie haiguse võimalikust tekkeriskist (vt lõigud 4.4 ja 4.8).
Kui Ezetroli ja fenofibraati saaval patsiendil kahtlustatakse sapikivitõbe, on näidustatud sapipõie uuringud ja antud ravi tuleb katkestada (vt lõik 4.8).
Fenofibraadi või gemfibrosiili samaaegne manustamine suurendas vähesel määral esetimiibi üldkontsentratsiooni (vastavalt ligikaudu 1,5 ja 1,7 korda).
Ezetroli ja teiste fibraatide koosmanustamist ei ole uuritud.
Fibraadid võivad suurendada kolesterooli eritumist sappi, mis võib põhjustada sapikivitõbe. Loomkatsetes suurendas esetimiib mõnikord kolesterooli sisaldust sapis, aga mitte kõikide liikide puhul (vt lõik 5.3). Ezetroli terapeutilise kasutamise korral ei saa välistada sapikivide tekke võimalust.
Statiinid
Kliiniliselt olulisi farmakokineetilisi koostoimeid ei täheldatud esetimiibi koosmanustamisel atorvastatiiniga, simvastatiiniga, pravastatiiniga, lovastatiiniga, fluvastatiiniga või rosuvastatiiniga.
Tsüklosporiin
Uuringus, milles osales 8 neerusiirdamise läbiteinud patsienti, kes said stabiilset tsüklosporiini annust ja kelle kreatiniini kliirens oli > 50 ml/min, suurendas Ezetroli 10 mg üksikannus kogu esetimiibi keskmist AUC 3,4 korda (2,3…7,9 korda), võrreldes terve kontrollgrupiga teisest uuringust (n = 17), kus saadi ainult esetimiibi. Teises uuringus osalenud siirdatud neeruga patsiendil, kellel oli raske neerukahjustus ning kes sai tsüklosporiini ja mitmeid teisi ravimeid, tõusis esetimiibi üldkontsentratsioon võrreldes kontrollgrupiga, kus saadi ainult esetimiibi, 12 korda. Kaheperioodilises ristkatses 12 tervel inimesel, kes manustasid iga päev 20 mg esetimiibi 8 päeva jooksul koos 100 mg tsüklosporiini ühekordse annusega suurenes 7. päeval keskmine tsüklosporiini AUC 15% (vahemik: vähenemine 10%...suurenemine 51%) võrreldes ainult 100 mg tsüklosporiini üksikannusega. Siirdatud neeruga patsientidel ei ole tehtud kontrollitud kliinilisi uuringuid esetimiibi mõju kohta tsüklosporiini kontsentratsioonile nende koosmanustamisel. Ezetroli lisamisel tsüklosporiinile tuleb olla ettevaatlik. Ezetroli ja tsüklosporiini samaaegselt saavatel patsientidel tuleb jälgida tsüklosporiini kontsentratsioone (vt lõik 4.4).
Antikoagulandid
Uuringus 12 tervel täiskasvanud mehel ei olnud esetimiibi (10 mg üks kord ööpäevas) samaaegsel manustamisel olulist mõju varfariini biosaadavusele ja protrombiini ajale. Kuid turule toomise järgselt on teatatud suurenenud
Lapsed
Koostoimete uuringud on läbi viidud ainult täiskasvanutel.
4.6Fertiilsus, rasedus ja imetamine
Raseduse ja imetamise ajal on Ezetroli kasutamine koos statiiniga vastunäidustatud (vt lõik 4.3), palun lugeda vastava statiini ravimi omaduste kokkuvõtet.
Rasedus
Ezetroli võib kasutada raseduse ajal ainult selge vajaduse korral. Ezetroli kasutamise kohta raseduse ajal kliinilised andmed puuduvad. Esetimiibi kasutamisel monoteraapiana loomkatsetes ei ole ilmnenud otsest või kaudset kahjulikku toimet rasedusele, embrüo/loote arengule, sünnitusele või postnataalsele arengule (vt lõik 5.3).
5/19
Imetamine
Ezetroli ei tohi imetamise ajal kasutada. Uuringud rottidel on näidanud, et esetimiib eritub emapiima. Ei ole teada, kas esetimiib eritub inimestel rinnapiima.
Fertiilsus
Puuduvad kliinilised andmed esetimiibi toime kohta inimese fertiilsusele. Esetimiibil puudus toime isaste või emaste rottide fertiilsusele (vt lõik 5.3).
4.7Toime reaktsioonikiirusele
Ravimi toime kohta autojuhtimisele ja masinate käsitsemise võimele ei ole uuringuid läbi viidud. Vaatamata sellele tuleb autot juhtides või masinatega töötades arvestada, et teatatud on pearingluse esinemisest.
4.8Kõrvaltoimed
Kõrvaltoimete loetelu tabelis (kliinilised uuringud ja turuletulekujärgne kogemus) Kliinilised uuringud kestusega kuni 112 nädalat, kus Ezetroli 10 mg ööpäevas manustati monoteraapiana 2396 patsiendile, koos statiiniga 11 308 patsiendile või koos fenofibraadiga
185 patsiendile, näitasid, et kõrvaltoimed olid tavaliselt kerged ning mööduvad. Üldine kõrvaltoimete esinemissagedus oli Ezetroli ja platseebo kasutamisel sarnane. Samuti oli Ezetroli ja platseebo korral võrreldav kõrvaltoimete tõttu ravimi kasutamise katkestamise määr.
Ezetrol monoteraapiana või koosmanustamisel statiiniga:
Järgmisi kõrvaltoimeid täheldati Ezetroliga ravitud patsientidel (N = 2396) suurema esinemissagedusega kui platseebo puhul (N = 1159) või Ezetroli ja statiini koosmanustamisel (N = 11 308) suurema esinemissagedusega kui ainult statiini kasutamisel (N = 9361). Andmed turuletulekujärgsete kõrvaltoimete kohta saadi teadetest, kus Ezetroli manustati üksi või koos statiiniga.
Esinemissagedused on määratletud kui: väga sage (≥ 1/10), sage (≥ 1/100 kuni < 1/10),
(≥ 1/1000 kuni < 1/100), harv (≥ 1/10 000 kuni < 1/1000), väga harv (< 1/10 000) ja teadmata (ei saa hinnata olemasolevate andmete alusel).
6/19

Ezetroli monoteraapia
Organsüsteemi klass |
Kõrvaltoimed |
Esinemissagedus |
Uuringud |
ALAT ja/või ASAT aktiivsuse suurenemine, |
|
|
kreatiinfosfokinaasi (KFK) aktiivsuse |
|
|
suurenemine veres, gammaglutamüültransferaasi |
|
|
aktiivsuse suurenemine, kõrvalekalded |
|
|
maksafunktsiooni näitajates |
|
Respiratoorsed, rindkere ja |
köha |
|
mediastiinumi häired |
|
|
Seedetrakti häired |
kõhuvalu, kõhulahtisus, kõhupuhitus |
sage |
|
düspepsia, gastroösofageaalne reflukshaigus, |
|
|
iiveldus |
|
liigesvalu, lihasspasmid, kaelavalu |
||
kahjustused |
|
|
Ainevahetus- ja toitumishäired |
söögiisu vähenemine |
|
Vaskulaarsed häired |
kuumahood, hüpertensioon |
|
Üldised häired ja |
väsimus |
sage |
manustamiskoha reaktsioonid |
rindkerevalu, valu |
|
Täiendavad kõrvaltoimed Ezetroli koosmanustamisel statiiniga |
|
|
Organsüsteemi klass |
Kõrvaltoimed |
Esinemissagedus |
Uuringud |
ALAT ja/või ASAT aktiivsuse suurenemine |
sage |
Närvisüsteemi häired |
peavalu |
sage |
|
paresteesia |
|
Seedetrakti häired |
suukuivus, gastriit |
|
Naha ja nahaaluskoe |
sügelus, lööve, urtikaaria |
|
kahjustused |
|
|
lihasvalu |
sage |
|
kahjustused |
seljavalu, lihasnõrkus, jäsemevalu |
|
Üldised häired ja |
asteenia, perifeersed tursed |
|
manustamiskoha reaktsioonid |
|
|
Turuletulekujärgne kogemus (manustamisel koos statiiniga või ilma) |
|
|
Organsüsteemi klass |
Kõrvaltoimed |
Esinemissagedus |
Vere ja lümfisüsteemi häired |
trombotsütopeenia |
teadmata |
Närvisüsteemi häired |
pearinglus, paresteesia |
teadmata |
Respiratoorsed, rindkere ja |
düspnoe |
teadmata |
mediastiinumi häired |
|
|
Seedetrakti häired |
pankreatiit, kõhukinnisus |
teadmata |
Naha ja nahaaluskoe |
multiformne erüteem |
teadmata |
kahjustused |
|
|
müalgia, müopaatia/rabdomüolüüs (vt lõik 4.4) |
teadmata |
|
kahjustused |
|
|
Üldised häired ja |
asteenia |
teadmata |
manustamiskoha reaktsioonid |
|
|
Immuunsüsteemi häired |
ülitundlikkus, sh lööve, urtikaaria, anafülaksia ja |
teadmata |
|
angioödeem |
|
Maksa ja sapiteede häired |
hepatiit, kolelitiaas, koletsüstiit |
teadmata |
Psühhiaatrilised häired |
depressioon |
teadmata |
Ezetrol koosmanustamisel fenofibraadiga
Seedetrakti häired: kõhuvalu (sage).
Mitmekeskuselises topeltpimedas platseebokontrolliga kliinilises uuringus segatüüpi hüperlipideemiaga patsientidel said 625 patsienti ravi kuni 12 nädala ja 576 patsienti kuni 1 aasta jooksul. Selles uuringus raviti Ezetroli ja fenofibraadiga 172 patsienti 12 nädala jooksul ja
230 patsienti (sealhulgas 109 patsienti, kes said esimese 12 nädala jooksul ainult Ezetroli) 1 aasta
7/19
jooksul. Selle uuringu eesmärk ei olnud võrrelda harvade kõrvaltoimete esinemist ravigruppides. Maksaensüümide aktiivsuse kliiniliselt olulise suurenemise (> 3 x kõrgem normivahemiku ülempiirist, järjestikused mõõtmised) esinemissagedus (95% CI) oli 4,5% (1,9; 8,8) ja 2,7% (1,2; 5,4) vastavalt fenofibraadi monoteraapia ning Ezetroli ja fenofibraadi koosmanustamise puhul (kohandatud ravi kestuse järgi). Vastavad esinemissagedused koletsüstektoomia järgselt olid 0,6% (0,0; 3,1) ja 1,7% (0,6; 4,0) vastavalt fenofibraadi monoteraapia ning Ezetroli ja fenofibraadi koosmanustamise puhul (vt lõigud 4.4 ja 4.5).
Lapsed (vanuses 6 kuni 17 aastat)
Uuringus, kus osalesid heterosügootse perekondliku või mitteperekondliku hüperkolesteroleemiaga lapsed (vanuses 6 kuni 10 aastat) (n = 138), täheldati ALATi ja/või ASATi aktiivsuse suurenemist (≥3 x üle normivahemiku ülempiiri järjestikuste mõõtmiste puhul)
Eraldi uuringus, kus osalesid heterosügootse perekondliku hüperkolesteroleemiaga teismelised patsiendid (vanuses 10 kuni 17 aastat) (n = 248), täheldati ALAT ja/või ASAT aktiivsuse suurenemist (≥3 x üle normivahemiku ülempiiri järjestikuste mõõtmiste puhul) 3% (4 patsiendil) esetimiibi/simvastatiini saanud patsientidest ja 2% (2 patsiendil) simvastatiini monoteraapia grupis; vastavad väärtused kreatiinfosfokinaasi (KFK) aktiivsuse suurenemise kohta olid 2% (2 patsiendil) ja 0%. Müopaatia juhtusid ei kirjeldatud.
Need uuringud ei sobinud harvaesinevate kõrvaltoimete võrdlemiseks.
Südame isheemiatõvega ja anamneesis ÄKS sündmusega patsiendid
esinemissagedus oli 0,2% esetimiibi/simvastatiini ja 0,1% simvastatiini saanute hulgas. Müopaatia oli defineeritud kui seletamatu lihasnõrkus või
Kroonilise neeruhaigusega patsiendid
Uuringus The Study of Heart and Renal Protection (SHARP) (vt lõik 5.1), milles osales üle 9000 patsiendi, kes said ööpäevas 10 mg Ezetroli ja 20 mg simvastatiini fikseeritud annusega
kombinatsiooni (n = 4650) või platseebot (n = 4620), olid ohutusandmed
8/19
Selles uuringus ei täheldatud statistiliselt olulist esinemissageduse suurenemist eelnevalt määratletud kõrvaltoimete osas, sealhulgas vähi (9,4% Ezetroli ja simvastatiini kombinatsiooni puhul ja 9,5% platseebo puhul), hepatiidi, koletsüstektoomia ega sapikivide või pankreatiidi tüsistuste osas.
Laboratoorsete analüüside väärtused
Monoteraapia kliinilistes uuringutes oli seerumi transaminaaside (järjestikused ALAT ja/või ASAT väärtused ≥ 3 korral üle normväärtuse ülemise piiri) kliiniliselt olulise tõusu esinemine Ezetroli (0,5%) ja platseebo (0,3%) korral sarnane. Ravimite koosmanustamise uuringutes oli esinemissagedus Ezetroli ja statiini koos kasutavatel patsientidel 1,3% ning ainult statiiniga ravitud patsientidel 0,4%. Need tõusud olid üldiselt asümptomaatilised, ei olnud seotud sapipaisuga ning pärast ravi katkestamist või ravi jätkamist normväärtus taastus (vt lõik 4.4).
Kliinilistes uuringutes teatati CPKst, mis oli > 10 korda üle normväärtuse ülemise piiri, neljal patsiendil 1674st (0,2%), kes said ainult Ezetroli vs. ühe patsiendiga 786st (0,1%), kes said platseebot ja ühe patsiendiga 917st (0,1%), kes said Ezetroli koos statiiniga vs. nelja patsiendiga 929st (0,4%), kes said ainult statiini. Ezetroliga ei seostatud liigset müopaatia või rabdomüolüüsi esinemist võrreldes vastavate kontrollrühmadega (platseeboga või ainult statiiniga) (vt lõik 4.4).
Võimalikest kõrvaltoimetest teavitamine
Ravimi võimalikest kõrvaltoimetest on oluline teavitada ka pärast ravimi müügiloa väljastamist. See võimaldab jätkuvalt hinnata ravimi kasu/riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest www.ravimiamet.ee kaudu.
4.9Üleannustamine
Kliinilistes uuringutes, kus manustati esetimiibi 50 mg ööpäevas 15 tervele isikule kuni 14 päeva või 40 mg ööpäevas
On teatatud vähestest Ezetroli üleannustamise juhtudest; enamust neist ei ole seostatud kõrvaltoimetega. Teatatud kõrvaltoimed ei ole olnud tõsised. Üleannustamise korral tuleb rakendada sümptomaatilise ja toetava ravi võtteid.
5.FARMAKOLOOGILISED OMADUSED
5.1Farmakodünaamilised omadused
Farmakoterapeutiline rühm: teised lipiidisisaldust muutvad ained,
Toimemehhanism
Ezetrol on uude klassi kuuluv lipiidide sisaldust langetav ravim, mis selektiivselt pärsib kolesterooli ja sarnaste taimsete steroolide imendumist soolest. Ezetrol on suukaudsel manustamisel aktiivne ning sellel on teistest kolesterooli sisaldust vähendavatest ravimitest (nt statiinid, sapphapete sekvestrandid (resiinid), fibraadid ja taimsed stanoolid) erinev toimemehhanism. Esetimiibi sihtmärk molekuli tasandil on sterooli transporter
Esetimiib lokaliseerub peensoole hattudele ja pärsib kolesterooli imendumist, mille tulemusena väheneb soole kolesterooli transport maksa. Statiinid vähendavad kolesterooli sünteesi maksas ja nende kahe erineva mehhanismi tulemusena saavutatakse täiendav kolesteroolitaseme langus. Kahenädalases kliinilises uuringus 18 hüperkolesteroleemiaga patsiendil pärssis Ezetrol soole kolesterooli imendumist võrreldes platseeboga 54%.
Farmakodünaamilised toimed
Esetimiibi selektiivsuse määramiseks kolesterooli imendumise vähendamisel on teostatud mitmeid
9/19
prekliinilisi uuringuid. Esetimiib pärssis
Epidemioloogilised uuringud on tõestanud, et kardiovaskulaarsüsteemi haigustesse haigestumus ja suremus sõltuvad otseselt üldkolesterooli ja
Ezetroli manustamine koos statiiniga on efektiivne kardiovaskulaarsete sündmuste riski vähendamisel südame isheemiatõvega ja anamneesis ÄKS sündmusega patsientidel.
Kliiniline efektiivsus ja ohutus
Kontrollitud kliinilistes uuringutes langetas Ezetrol manustatuna kas monoteraapiana või koos statiiniga hüperkolesteroleemiaga patsientidel tunduvalt üldkolesterooli (ÜK), väikese tihedusega lipoproteiiniga kolestrooli
Primaarne hüperkolesteroleemia
Topeltpimedas platseebokontrolliga
Statiinravi saanud patsientide hulgast, kes algselt ei olnud saavutanud
Kahes topeltpimedas randomiseeritud platseebokontrolliga
Mitmekeskuselises topeltpimedas kontrollitud kliinilises uuringus (ENHANCE) randomiseeriti 720 heterosügootse perekondliku hüperkolesteroleemiaga patsienti saama 2 aasta jooksul esetimiibi annuses 10 mg kombinatsioonis 80 mg simvastatiiniga (n = 357) või 80 mg simvastatiini (n = 363). Uuringu esmane eesmärk oli hinnata esetimiibi/simvastatiini kombinatsioonravi toimet unearterite
Esmane tulemusnäitaja, kahemõõtmelise ultraheli abil mõõdetud kõigi kuue unearteri segmendi keskmise IMT muutus, ei erinenud oluliselt (p = 0,29) kahe ravigrupi vahel. 10 mg esetimiibi ja 80 mg simvastatiini kombinatsiooni või ainult 80 mg simvastatiini kasutamisel suurenes
Esetimiib 10 mg kombinatsioonis 80 mg simvastatiiniga langetas
10/19
Lapsed
Mitmekeskuselises topeltpimedas kontrollitud uuringus randomiseeriti 138 heterosügootse perekondliku või mitteperekondliku hüperkolesteroleemiaga patsienti (59 poissi ja 79 tüdrukut) vanuses 6 kuni 10 aastat (keskmine vanus 8,3 aastat), kellel oli
12. nädalal olid Ezetroli toimel oluliselt vähenenud üldkolesterooli (‒21% vs. 0%),
Mitmekeskuselises, topeltpimedas, kontrollitud uuringus randomiseeriti 142 heterosügootse perekondliku hüperkolesteroleemiaga (HePH) poissi (puberteedi aste Tanneri skaalal II või enam) ja 106 tüdrukut (kellel olid menstruatsioonid alanud) vanuses 10 kuni 17 aastat (keskmine vanus
14,2 aastat), kellel oli
6. nädalal olid koosmanustatud Ezetroli ja simvastatiini (kõik annused) toimel oluliselt vähenenud üldkolesterooli (38% vs. 26%),
Koos simvastatiini 40 mg ületavate ööpäevaste annustega manustatud Ezetroli ohutust ja efektiivsust ei ole uuritud lastel vanuses 10 kuni 17 aastat. Koos simvastatiiniga manustatud Ezetroli ohutust ja efektiivsust ei ole uuritud alla
Kardiovaskulaarsete sündmuste ennetamine
Uuring
Patsientide vanuse mediaan oli 63,6 aastat; 76% olid meessoost, 84% europiidid ja 27% diabeetikud. Uuringusse kvalifitseeruva seisundi ajal oli
11/19
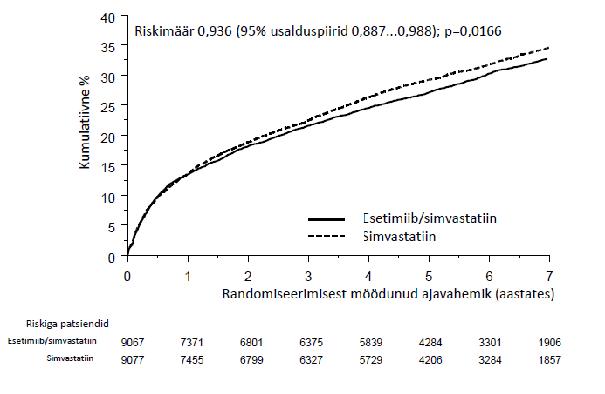
Esmane tulemusnäitaja oli
Esines üldine kasu kõigi insultide puhul; samas esines ka väike mitteoluline suurenemine hemorraagiliste insultide esinemissageduses esetimiibi+simvastatiini rühmas võrreldes ainult simvastatiiniga (vt Tabel 1). Hemorraagilise insuldi riski esetimiibi manustamisel koos tugevamatoimeliste statiinidega ei ole uuritud pikaajaliste tulemuste suhtes.
Esetimiibi/simvastatiini raviefekt oli üldiselt samasugune paljudes, sealhulgas soo, vanuse, rassi, diabeedi anamneesi, ravieelse lipiidisisalduse, varasema statiinravi, varasema insuldi ja hüpertensiooni alarühmades.
Joonis 1: Esetimiibi/simvastatiini toime esmasele
12/19

Tabel 1
Tulemusnäitaja |
Esetimiib/simvastatiin |
Simvastatiin |
Riskimäär |
p- |
|
10/40 mgA |
40 mgB |
(95% CI) |
väärtus |
|
(N=9067) |
(N=9077) |
|
|
n
Primaarne efektiivsuse
(kardiovaskulaarne surm, rasked |
|
|
|
|
|
|
isheemilised seisundid ja mitteletaalne |
32,72% |
34,67% |
0,936 (0,887; 0,988) |
0,016 |
||
insult) |
|
|
|
|
|
|
|
|
|
|
|
|
|
Efektiivsuse sekundaarsed |
|
|
|
|
|
|
|
|
|
|
|
|
|
Isheemiatõvega seotud surmajuhud, |
|
|
|
|
|
|
mitteletaalne müokardi infarkt, |
|
|
|
|
|
|
erakorraline koronaaride |
17,52% |
18,88% |
0,912 (0,847; 0,983) |
0,016 |
||
revaskulariseerimine 30 päeva |
|
|
|
|
|
|
möödudes |
|
|
|
|
|
|
|
|
|
|
|
|
|
Raske isheemiline seisund, |
|
|
|
|
|
|
mitteletaalne insult, surm (kõik |
38,65% |
40,25% |
0,948 (0,903; 0,996) |
0,035 |
||
põhjused) |
|
|
|
|
|
|
|
|
|
|
|
|
|
Kardiovaskulaarne surm, mitteletaalne |
|
|
|
|
|
|
müokardi infarkt, ebastabiilne |
|
|
|
|
|
|
stenokardia, mis vajab |
34,49% |
36,20% |
0,945 (0,897; 0,996) |
0,035 |
||
|
||||||
hospitaliseerimist, mis tahes revaskulariseerimine, mitteletaalne insult
Esmase
Kardiovaskulaarne surm |
6,89% |
6,84% |
1,000 (0,887; 1,127) |
0,997 |
||||
|
|
|
|
|
|
|
||
Rasked isheemilised seisundid: |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Mitteletaalne müokardi infarkt |
12,77% |
14,41% |
0,871 (0,798; 0,950) |
0,002 |
|||
|
|
|
|
|
|
|
|
|
|
Ebastabiilne stenokardia, mis vajab |
2,06% |
1,92% |
1,059 (0,846; 1,326) |
0,618 |
|||
|
hospitaliseerimist |
|||||||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Koronaaride revaskulariseerimine |
21,84% |
23,36% |
0,947 (0,886; 1,012) |
0,107 |
|||
|
30 päeva möödudes |
|||||||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
||
Mitteletaalne insult |
3,49% |
4,24% |
0,802 (0,678; 0,949) |
0,010 |
||||
|
|
|
|
|
|
|
||
Kõik müokardi infarkti juhud |
13,13% |
14,82% |
0,872 (0,800; 0,950) |
0,002 |
||||
(letaalsed ja mitteletaalsed)) |
||||||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
Kõik insuldi juhud (letaalsed ja |
4,16% |
4,77% |
0,857 (0,734; 1,001) |
0,052 |
||||
mitteletaalsed)) |
||||||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Mittehemorraagiline insult D |
3,48% |
4,23% |
0,793 (0,670; 0,939) |
0,007 |
|||
|
|
|
|
|
|
|
|
|
|
Hemorraagiline insult |
0,77% |
0,59% |
1,377 (0,930; 2,040) |
0,110 |
|||
|
|
|
|
|
|
|
||
Mis tahes põhjusega surmajuhud |
15,36% |
15,28% |
0,989 (0,914; 1,070) |
0,782 |
||||
|
|
|
|
|||||
A |
|
|
||||||
B |
|
|
|
|||||
C |
Hinnanguline väärtus |
|
|
|
|
|||
D |
Kaasa arvatud isheemiline insult ja täpsustamata insult. |
|
|
|
|
|
||
Raskete vaskulaarsete sündmuste ennetamine kroonilise neeruhaigusega patsientidel
SHARP (The Study of Heart and Renal Protection) uuring oli rahvusvaheline randomiseeritud platseeboga kontrollitud topeltpimendatud uuring, mis viidi läbi 9438 kroonilise neeruhaigusega patsiendiga, kellest kolmandik oli ravieelselt dialüüsravil. Kokku 4650 patsiendile määrati 10 mg Ezetroli ja 20 mg simvastatiini fikseeritud annustega kombinatsioonravi ja 4620 patsiendile platseebot ning neid jälgiti
13/19
uuringusse kaasamise tingimusi ei olnud. Ravieelne keskmine
SHARP uuringuplaanis määratletud esmaseks võrdluseks oli ravikavatsuslik
Esmase tulemusnäitaja analüüsis ilmnes, et Ezetrol kombinatsioonis simvastatiiniga vähendas oluliselt raskete vaskulaarsete seisundite tekke riski (need seisundid tekkisid 749 patsiendil platseeborühmas vs. 639 patsiendil Ezetroli ja simvastatiini kombineeritud ravi rühmas) suhtelise riski vähenemisega 16% (p=0,001).
Sellele vaatamata ei võimaldanud antud uuringu ülesehitus eraldi hinnata esetimiibi kui üksiku komponendi efektiivsust raskete vaskulaarsete sündmuste tekke olulisel riski vähendamisel kroonilise neeruhaigusega patsientidel.
Raskete vaskulaarsete seisundite individuaalsed komponendid on esitatud Tabelis 2. Ezetrol kombineerituna simvastatiiniga vähendas oluliselt insuldi ja mis tahes revaskulariseerimiste riski ilma märkimisväärsete arvuliste erinevusteta Ezetroli ja simvastatiini kombinatsioonravi kasuks mitteletaalse müokardi infarkti ja kardiaalse surma vähendamisel.
14/19
Tabel 2
SHARP uuringus osalenud patsientidel ilmnenud rasked vaskulaarsed seisundid ravirühmade kaupa
|
Ezetrol 10 mg |
Platseebo |
Riskimäär |
|
Tulemusnäitaja |
kombineeritud |
(N=4620) |
(95% CI) |
|
|
ravi 20 mg |
|
|
|
|
simvastatiiniga |
|
|
|
|
(N=4650) |
|
|
|
Rasked vaskulaarsed seisundid |
701 (15,1%) |
814 (17,6%) |
0,85 |
0,001 |
|
|
|
(0,77...0,94) |
|
|
|
|
|
|
Mitteletaalne müokardi infarkt |
134 (2,9%) |
159 (3,4%) |
0,84 |
0,12 |
|
|
|
(0,66...1,05) |
|
|
|
|
|
|
Kardiaalsed surmad |
253 (5,4%) |
272 (5,9%) |
0,93 |
0,38 |
|
|
|
(0,78...1,10) |
|
|
|
|
|
|
Mis tahes insult |
171 (3,7%) |
210 (4,5%) |
0,81 |
0,038 |
|
|
|
(0,66...0,99) |
|
|
|
|
|
|
Mittehemorraagiline insult |
131 (2,8%) |
174 (3,8%) |
0,75 |
0,011 |
|
|
|
(0,60...0,94) |
|
|
|
|
|
|
Hemorraagiline insult |
45 (1,0%) |
37 (0,8%) |
1,21 |
0,40 |
|
|
|
(0,78...1,86) |
|
|
|
|
|
|
Mis tahes revaskularisatsioon |
284 (6,1%) |
352 (7,6%) |
0,79 |
0,004 |
|
|
|
(0,68...0,93) |
|
|
|
|
|
|
Rasked aterosklerootilised |
526 (11,3%) |
619 (13,4%) |
0,83 |
0,002 |
seisundidB |
|
|
(0,74...0,94) |
|
|
|
|
|
|
ASHARP uuringus osalenud kõigi Ezetroli ja simvastatiini kombineeritud ravi või platseebo ravirühmadesse randomiseeritud patsientidega tehtud ravikavatsuslik
BRaske vaskulaarne seisund – määratletud kui kombineeritud tulemusnäitaja, mille hulka kuuluvad mitteletaalne müokardi infarkt, isheemiline surm, mittehemorraagiline insult või mis tahes revaskularisatsioon
Ezetroli ja simvastatiini kombineeritud ravi abil saavutatud
Homosügootne perekondlik hüperkolesteroleemia (HoPH)
Topeltpimedasse, randomiseeritud 12 nädalat kestnud uuringusse kaasati 50 kliinilise ja/või geneetilise HoPH diagnoosiga patsienti, kes said eelnevalt atorvastatiini või simvastatiini (40 mg) koos samaaegse LDL afereesiga või ilma. Ezetrol manustatuna koos atorvastatiiniga (40 või 80 mg) või simvastatiiniga (40 mg või 80 mg), vähendas oluliselt
Homosügootne sitosteroleemia (fütosteroleemia)
Topeltpimedas platseebokontrolliga
Aordistenoos
Uuring SEAS (The Simvastatin and Ezetimibe for the Treatment of Aortic Stenosis) oli mitmekeskuseline, topeltpime, platseebokontrollitud uuring, mis kestis keskmiselt 4,4 aastat ja kus osales 1873 patsienti asümptomaatilise aordistenoosiga (AS), mida dokumenteeriti kui Doppleriga
15/19
mõõdetud maksimaalset verevoolu kiirust aordis vahemikus 2,5...4,0 m/s. Uuringusse kaasati ainult patsiendid, kes ei vajanud aterosklerootilise kardiovaskulaarse haiguse riski vähendamise eesmärgil statiinravi. Patsiendid randomiseeriti 1 : 1 saama platseebot või samaaegselt manustatud 10 mg esetimiibi ja 40 mg simvastatiini ööpäevas.
Esmane kombineeritud tulemusnäitaja hõlmas olulisi kardiovaskulaarseid tüsistusi, milleks olid kardiovaskulaarne surm, aordiklapi asendamise operatsioon, kongestiivne südamepuudulikkus aordistenoosi süvenemise tulemusena, mittefataalne müokardiinfarkt, koronaararteri šunteerimine, perkutaanne koronaarangioplastika, hospitaliseerimine ebastabiilse stenokardia tõttu ja mittehemorraagiline insult. Põhilised teisesed tulemusnäitajad olid esmase tulemusnäitaja kategooriate alamgruppide kombineeritud näitajad.
Platseeboga võrreldes esetimiib/simvastatiin 10/40 mg ei vähendanud märkimisväärselt oluliste kardiovaskulaarsete tüsistuste riski. Esmane tulemusnäitaja ilmnes 333 patsiendil (35,3%) esetimiibi/simvastatiini grupis ja 355 patsiendil (38,2%) platseebogrupis (riskisuhe esetimiibi/simvastatiini grupis 0,96; 95% usaldusvahemik 0,83...1,12; p = 0,59). Aordiklapi asendamine tehti 267 patsiendile (28,3%) esetimiibi/simvastatiini grupis ja 278 patsiendile (29,9%) platseebogrupis (riskisuhe 1,00; 95% CI 0,84...1,18; p = 0,97). Esetimiibi/simvastatiini grupis
(n = 148) esinesid isheemilised kardiovaskulaarsed tüsistused väiksemal arvul patsientidest kui platseebogrupis (n = 187) (riskisuhe 0,78; 95% CI 0,63...0,97; p = 0,02), põhiliselt väiksema arvu patsientide tõttu, kellele tehti koronaararteri šunteerimine.
Vähk tekkis sagedamini esetimiibi/simvastatiini grupis (105 vs. 70, p = 0,01). Selle leiu kliiniline tähtsus ei ole kindel, kuna suuremas SHARP uuringus mis tahes vähijuhtumiga patsientide koguarv ei erinenud (438 esetimiibi/simvastatiini grupis vs. 439 platseebogrupis). Lisaks sellele ei olnud
5.2Farmakokineetilised omadused
Imendumine
Suukaudsel manustamisel imendub esetimiib kiiresti ja konjugeeritakse farmakoloogiliselt aktiivseks fenoolglükuroniidiks (esetimiibglükuroniid). Keskmine maksimaalne plasmakontsentratsioon (CMAX) saabub esetimiibglükuroniidil keskmiselt 1...2 tunni jooksul ja esetimiibil 4...12 tunni jooksul.
Esetimiibi absoluutset biosaadavust ei saa määrata, kuna aine ei ole lahustatav süstelahustele sobivas vesikeskkonnas.
Ravimi suukaudne manustamine samaaegselt toiduga (rasvane või rasvavaene toit) ei mõjuta esetimiibi biosaadavust manustatuna Ezetrol 10 mg tablettidena. Ezetroli võib manustada nii toiduga kui ilma.
Jaotumine
Esetimiib ja esetimiibglükuroniid seotakse inimese plasmavalkudega vastavalt 99,7% ja 88...92%.
Biotransformatsioon
Esetimiib metaboliseeritakse primaarselt peensooles ja maksas glükuroniidi konjugatsiooni teel
(II faasi reaktsioon) ning järgnevalt eritub ta sapiga. Minimaalset oksüdatiivset metabolismi (I faasi reaktsioon) on täheldatud kõigil uuritud liikidel. Esetimiib ja esetimiibglükuroniid on peamised plasmast leitavad ravimist pärinevad ühendid, moodustades vastavalt 10...20% ja 80...90% kogu ravimist plasmas. Mõlemad, nii esetimiib kui ka esetimiibglükuroniid, erituvad plasmast aeglaselt tõendatult olulise enterohepaatilise retsirkulatsiooni teel. Esetimiibi ja esetimiibglükuroniidi poolväärtusaeg on ligikaudu 22 tundi.
Eritumine
Pärast
16/19
radioaktiivsusest leiti üle 10 päeva kestnud kogumisperioodil vastavalt väljaheidetes ja uriinis. 48 tunni möödudes ei olnud vereplasmas võimalik radioaktiivsust määrata.
Patsientide erirühmad
Lapsed
Esetimiibi farmakokineetika on lastel vanuses alates 6. eluaastast täiskasvanutega sarnane. Farmakokineetilisi andmeid alla
Eakad
Esetimiibi üldkontsentratsioon plasmas on vanematel
Maksakahjustus
Võrreldes tervete inimestega tõusis kerge maksakahjustusega
Neerukahjustus
Võrreldes tervetega (n = 9) suurenes raske neeruhaigusega patsientidel (n = 8; keskmine kreatiniini kliirens ≤ 30 ml/min/1,73 m) pärast esetimiibi 10 mg üksikannust kogu esetimiibi keskmine kontsentratsioonikõvera alune pindala ligikaudu 1,5 korda. Seda tulemust ei peeta kliiniliselt oluliseks. Neerukahjustusega patsiendid ravimiannuse kohandamist ei vaja.
Ühel selle uuringu patsiendil (neerusiirdamisejärgne, keda raviti paljude ravimitega, sealhulgas tsüklosporiiniga) oli ekspositsioon esetimiibile 12 korda suurem.
Sugu
Esetimiibi üldkontsentratsioon on naistel veidi kõrgem (ligikaudu 20%) kui meestel.
5.3Prekliinilised ohutusandmed
Esetimiibi korduvtoksilisuse loomkatsetes ei ole leitud sihtorganeid toksilistele toimetele. Koertel, keda raviti 4 nädala jooksul esetimiibiga (≥ 0,03 mg/kg/päevas) suurenes kolesterooli sisaldus sapis faktorilt 2,5
300 mg/kg päevas sagedasemat sapikivitõve või mõne teise maksa ja sapiteede häire esinemist. Nende andmete tähtsus inimesele ei ole teada. Ezetroli terapeutilise kasutamise korral ei saa välistada sapikivide tekke võimalust.
Statiinide ja esetimiibi koosmanustamise uuringutes täheldati peamiselt statiinidele omaseid toksilisi toimeid. Mõned toksilised toimed olid rohkem väljendunud kui ravi korral ainult statiinidega. Selle põhjuseks peetakse koosmanustamisel esinevaid farmakokineetilisi ja farmakodünaamilisi koostoimeid. Selliseid koostoimeid kliinilistes uuringutes ei täheldatud. Müopaatiad esinesid rottidel üksnes pärast ravi annustega, mis olid inimese terapeutilisest annusest mitmeid kordi suuremad (statiinide kontsentratsioonikõvera alune ala ligikaudu 20 korda suurem ja aktiivsete metaboliitide kontsentratsioonikõvera alune ala 500…2000 korda suurem).
Esetimiibi in vivo ja in vitro uuringutel monoteraapiana või koos statiinidega genotoksilist toimet ei
17/19
täheldatud. Esetimiibi kantserogeensuse pikaajalised uuringud olid negatiivsed.
Esetimiibil ei olnud toimet isaste ja emaste rottide viljakusele ega leitud ka teratogeenset toimet rottidele ja küülikutele, samuti ei esinenud mõju pre- ja postnataalsele arengule. Korduvas annuses 1000 mg/kg päevas läbis esetimiib tiinetel rottidel ja küülikutel platsentaarbarjääri. Esetimiibi ja statiinide koosmanustamine ei olnud rottidele teratogeenne. Tiinetel küülikutel esines mõnel juhul skeleti deformatsioone (torakaal- ja sabalülide kahjustus, sabalülide vähenenud arv). Esetimiibi ja lovastatiini koos manustamisel esines embrüo surma.
6.FARMATSEUTILISED ANDMED
6.1Abiainete loetelu
Naatriumkroskarmelloos
Laktoosmonohüdraat
Magneesiumstearaat
Mikrokristalliline tselluloos
Povidoon
Naatriumlaurüülsulfaat
6.2Sobimatus
Ei kohaldata.
6.3Kõlblikkusaeg
3 aastat.
6.4Säilitamise eritingimused
Hoida temperatuuril kuni 30 ºC.
Blistrid: hoida originaalpakendis, niiskuse eest kaitstult.
Pudelid: hoida pudel tihedalt suletuna, niiskuse eest kaitstult.
6.5Pakendi iseloomustus ja sisu
Läbipaistvast
Vinüülkattega alumiiniumile liimitud läbipaistvast
Läbipaistva
Polüpropüleenist korgiga HDPE pudelid, mis sisaldavad 100 tabletti.
Kõik pakendi suurused ei pruugi olla müügil.
6.6Erihoiatused ravimpreparaadi hävitamiseks
Erinõuded puuduvad.
18/19
7.MÜÜGILOA HOIDJA
Merck Sharp & Dohme OÜ
A. H. Tammsaare tee 47, 11316 Tallinn
Eesti
8.MÜÜGILOA NUMBER
9.ESMASE MÜÜGILOA VÄLJASTAMISE/MÜÜGILOA UUENDAMISE KUUPÄEV
Müügiloa esmase väljastamise kuupäev: 06.06.2003
Müügiloa viimase uuendamise kuupäev: 07.06.2013
10.TEKSTI LÄBIVAATAMISE KUUPÄEV
aprill 2016
19/19
