Cleodette - õhukese polümeerikattega tablett (3mg +0,02mg)
Artikli sisukord
õhukese polümeerikattega tablett (3mg +0,02mg)

Pakendi infoleht: teave kasutajale
Cleodette, 0,02 mg/3 mg õhukese polümeerikattega tabletid
Etünüülöstradiool/drospirenoon
Oluline teave kombineeritud hormonaalsete rasestumisvastaste vahendite kohta:
−Õigesti kasutatuna on need ühed kõige usaldusväärsemad, pöörduva toimega rasestumisvastased vahendid.
−Kombineeritud hormonaalsed rasestumisvastased vahendid suurendavad vähesel määral verehüübe tekkeriski veenides ja arterites, eriti esimesel kasutusaastal või hakates uuesti kasutama pärast
−Pöörake sellele tähelepanu ja konsulteerige oma arstiga, kui arvate, et teil võivad olla verehüübe sümptomid (vt lõik 2 „Verehüübed“).
Enne ravimi kasutamist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet.
-Hoidke infoleht alles, et seda vajadusel uuesti lugeda.
-Kui teil on lisaküsimusi, pidage nõu oma arsti või apteekriga.
-Ravim on välja kirjutatud üksnes teile. Ärge andke seda kellelegi teisele. Ravim võib olla neile kahjulik.
-Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga. Kõrvaltoime võib olla ka selline, mida selles infolehes ei ole nimetatud. Vt lõik 4.
Infolehe sisukord
1.Mis ravim on Cleodette ja milleks seda kasutatakse
2.Mida on vaja teada enne Cleodette võtmist
3.Kuidas Cleodette’t võtta
4.Võimalikud kõrvaltoimed
5.Kuidas Cleodette’t säilitada
6.Pakendi sisu ja muu teave
1.Mis ravim on Cleodette ja milleks seda kasutatakse
Cleodette on rasestumisvastane ravim, mida kasutatakse raseduse vältimiseks.
Iga tablett sisaldab väikeses koguses kahte erinevat naissuguhormooni, nimelt drospirenooni ja etünüülöstradiooli.
Kahte hormooni sisaldavaid rasestumisvastaseid tablette nimetatakse kombineeritud pillideks.
2.Mida on vaja teada enne Cleodette võtmist
Üldised märkused
Enne Cleodette kasutama hakkamist lugege lõigust 2 teavet verehüüvete kohta. Eriti oluline on lugeda verehüüvete sümptomite kohta, vt lõik 2 “Verehüübed”. Arst esitab teile mõningad küsimused teie ja teie lähisugulaste tervise kohta. Arst mõõdab ka teie vererõhku ja võib teie tervislikust seisundist sõltuvalt teostada ka mõningaid muid analüüse.
Selles infolehes kirjeldatakse mitmeid olukordi, mille korral tuleks lõpetada Cleodette kasutamine või mille puhul võib Cleodette usaldusväärsus langeda. Niisugustes olukordades tuleb loobuda seksuaalvahekorrast või kasutada täiendavaid mittehormonaalseid rasestumisvastaseid vahendeid, nt kasutada kondoomi või muud barjäärimeetodit. Ärge kasutage rütmi- või temperatuurimeetodeid. Need ei pruugi olla usaldusväärsed, sest Cleodette muudab menstruaaltsükliga kaasnevaid kehatemperatuuri ja emakakaela lima muutusi.

Sarnaselt teistele hormonaalsetele rasestumisvastastele vahenditele ei kaitse Cleodette HIV- nakkuse (AIDS) ega muude sugulisel teel levivate haiguste eest.
Ärge võtke Cleodette’t:
Te ei tohi Cleodette’t kasutada, kui teil esineb mis tahes allpool nimetatud seisund. Kui teil on mõni neist seisunditest, peate sellest rääkima oma arstile. Teie arst arutab koos teiega, milline teine rasestumisvastane meetod sobiks teile paremini.
−kui teil esineb (või on kunagi esinenud) verehüübeid jalgade veresoontes (süvaveeni tromboos, SVT), kopsus (pulmonaalne emboolia, PE) või muudes organites.
−kui te teate, et teil on vere hüübimist mõjutav häire, nt
−kui teile plaanitakse teha operatsioon või kui te ei saa pikemat aega liikuda (vt lõik „Verehüübed").
−kui teil on kunagi olnud südamelihaseinfarkt või insult.
−kui teil on (või on kunagi olnud) stenokardia (seisund, mis põhjustab tugevat valu rindkeres ja võib olla südameinfarkti esimene tunnus) või mööduv isheemiline atakk (mööduvad insuldi sümptomid).
−kui teil on mõni järgmistest haigustest, mis võib suurendada verehüübe tekkeriski arterites:
–raske suhkurtõbi koos veresoonte kahjustusega
-väga kõrge vererõhk
−väga kõrge rasvade (kolesterool või triglütseriidid) sisaldus veres
−seisund, mida nimetatakse hüperhomotsüsteineemiaks.
−kui teil on (või on kunagi olnud) teatud tüüpi migreen, mida nimetatakse „auraga migreeniks“.
−kui teil on (või on kunagi olnud) maksahaigus ja maksafunktsioon ei ole veel normaliseerunud.
−kui teie neerud ei tööta korralikult (neerupuudulikkus).
−kui teil on (või on kunagi olnud) maksakasvaja.
−kui teil on (või on kunagi olnud) või kui teil kahtlustatakse rinnanäärme vähki või suguelundite vähki.
−kui teil esineb ebaselge põhjusega verejooks tupest.
−kui olete etünüülöstradiooli, drospirenooni või selle ravimi mis tahes koostisosade (loetletud lõigus 6) suhtes allergiline. Allergia võib põhjustada sügelust, nahalöövet või turset.
−kui teil on
Hoiatused ja ettevaatusabinõud
Millal peate pöörduma oma arsti poole?
Pöörduge viivitamatult arsti poole
kui te märkate võimalikke verehüübe sümptomeid, mis võib tähendada, et teil on verehüüve jalas (st süvaveenitromboos), verehüüve kopsus (st kopsuemboolia), südameinfarkt või insult (vt allolevat lõiku „Verehüübed“).
Nende tõsiste kõrvaltoimete sümptomite kirjelduse leiate lõigust „Kuidas tunda ära verehüübe tunnuseid“.
Teatage oma arstile, kui teil esineb ükskõik milline järgmistest seisunditest
Mõningatel juhtudel tuleb Cleodette või mis tahes muu kombineeritud rasestumisvastase ravimi kasutamisel olla eriti tähelepanelik ja teie arst võib pidada vajalikuks teid regulaarselt kontrollida. Kui mõni järgnevatest seisunditest kehtib teie kohta, rääkige sellest oma arstile enne kui alustate Cleodette kasutamist. Samuti teavitage oma arsti, kui mõni neist seisunditest tekib või muutub ägedamaks Cleodette kasutamise ajal:.
−kui teie lähisugulasel on või on kunagi olnud rinnanäärmevähk.

−kui te põete mõnd maksa- või sapipõiehaigust.
−kui te põete suhkurtõbe.
−kui teil on depressioon.
−kui teil on Crohni tõbi või haavandiline koliit (krooniline põletikuline soolehaigus).
−kui teil on
−kui teil on sirprakuline aneemia (pärilik vere punaliblede haigus).
−kui teil on epilepsia (vt „Muud ravimid ja Cleodette“).
−kui teil on süsteemne erütematoosluupus (haigus, mis kahjustab teie organismi loomulikku kaitsevõimet).
−kui teie vere rasvasisaldus on suurenenud (hüpertriglütserideemia) või kui seda on esinenud teie perekonnas. Hüpertriglütserideemiat seostatakse pankreatiidi (kõhunäärme põletik) suurema tekkeriskiga.
−kui teile plaanitakse teha operatsioon või kui te ei saa pikemat aega liikuda (vt lõik 2 „Verehüübed").
−kui te olete äsja sünnitanud, on teil suurem oht verehüüvete tekkimiseks. Te peate küsima oma arstilt, kui ruttu pärast sünnitust saate hakata Cleodette’t võtma.
−kui teil on nahaaluste veenide põletik (pindmine tromboflebiit).
−kui teil on veenilaiendid.
−kui te põete haigust, mis avaldus esmakordselt raseduse ajal või suguhormoonide varasema kasutamisega seoses (nt kuulmiskadu, verehaigus nimega porfüüria, villiline nahalööve raseduse ajal (rasedusherpes), närvihaigus, millega kaasnevad äkilised keha liigutused (Sydenhami korea ehk tantstõbi).
−kui teil on või on kunagi olnud kloasmid (nahavärvi kadumine eelkõige näo- või kaelapiirkonnas, mida teatakse ka kui „raseduslaigud“). Niisugusel juhul vältige otsest päikesevalgust või
−kui teil esineb pärilik angioödeem, võivad östrogeene sisaldavad ravimid selle sümptomeid esile kutsuda või raskendada. Angioödeemi sümptomite, nagu
VEREHÜÜBED
Kombineeritud hormonaalsete rasestumisvastaste vahendite, nagu Cleodette, kasutamine suurendab verehüüvete tekkimise riski, võrreldes nendega, kes neid ei kasuta. Harvadel juhtudel võib verehüüve veresooned ummistada ja põhjustada tõsiseid probleeme.
Verehüübed võivad tekkida:
-veenides (nimetatakse venoosseks tromboosiks, venoosseks trombembooliaks või
−arterites (nimetatakse arteriaalseks tromboosiks, arteriaalseks trombembooliaks või
Verehüüvetest paranemine ei ole alati täielik. Harvadel juhtudel võivad verehüübed tekitada tõsiseid pikaajalisi tüsistusi, väga harva võivad need lõppeda surmaga.
Oluline on meeles pidada, et üldiselt on risk kahjuliku verehüübe tekkimiseks Cleodette kasutamisel väike.
KUIDAS TUNDA ÄRA VEREHÜÜBE TUNNUSEID
Pöörduge viivitamatult arsti poole, kui te märkate mis tahes järgmist nähtu või sümptomit.
Kas teil esineb neid nähte? |
Millisele haigusele see |
|
viitab? |
Ühe jala turse või paistetus piki jala või jalalaba veeni, eriti juhul, kui |
Süvaveenitromboos |
sellega kaasneb: |
|
•valu või hellus jalas, mida võib olla tunda ainult seistes või kõndides;
•haige jala kõrgem temperatuur;
•jalanaha värvimuutus, nt kahvatus, punetus või sinakaks värvumine.
Kas teil esineb neid nähte? |
Millisele haigusele see |
|
|
|
viitab? |
• |
Teadmata põhjusega, äkki tekkinud õhupuudus või kiire hingamine. |
Kopsuemboolia |
• |
Teadmata põhjusega, äkki tekkinud köha (võib kaasneda veriköha). |
|
• |
Terav valu rindkeres, mis võib tugevneda sügaval hingamisel. |
|
• |
Tugev peapööritus või pearinglus. |
|
• |
Kiire või ebakorrapärane südamerütm. |
|
• |
Tugev kõhuvalu. |
|
Kui te ei ole kindel, pöörduge oma arsti poole, sest osa sümptomeid (nt |
|
|
köha või õhupuudus) võivad ekslikult viidata ka vähemtõsistele haigustele |
|
|
nagu nt hingamisteede nakkus (nt külmetushaigus). |
|
|
Enamasti ühes silmas tekkivad sümptomid: |
Tromboos silma |
|
• |
kohene nägemiskaotus või |
võrkkesta veenis |
• |
valutu nägemise ähmastumine, mis võib viia nägemiskaotuseni. |
(verehüüve silmas) |
• |
Valu, |
Südameinfarkt |
• |
Pigistus- või täistunne rindkeres, käsivarres või rinnaku all. |
|
• |
Täistunne, seedehäired või lämbumistunne. |
|
• |
Ebamugavustunne ülakehas, mis kiirgub selga, lõuga, kõripiirkonda, |
|
|
käsivarde ja kõhtu. |
|
• |
Higistamine, iiveldus, oksendamine või pearinglus. |
|
• |
Äärmine nõrkus, ärevus või õhupuudus. |
|
• |
Kiire või ebakorrapärane südamerütm. |
|
• |
Äkki tekkinud tuimus või nõrkus näos, käes või jalas, eriti ühel |
Insult |
|
kehapoolel. |
|
• |
Äkki tekkinud segasusseisund, rääkimis- või mõistmisraskus. |
|
• |
Äkki tekkinud ühe või mõlema silma nägemishäired. |
|
• |
Äkki tekkinud kõndimisraskus, pearinglus, tasakaalu- või |
|
|
koordinatsioonikaotus. |
|
• |
Äkki tekkinud tugev või pikaajaline teadmata põhjusega peavalu. |
|
• |
Teadvusekaotus või minestamine krampidega või ilma. |
|
Mõnikord võivad insuldi sümptomid olla lühiajalised ning taanduvad |
|
|
peaaegu kohe ja täielikult. Te peate siiski pöörduma viivitamatult arsti |
|
|
poole, sest teil võib olla oht teise insuldi tekkeks. |
|
|
• |
Jäsemete turse ja kergelt sinakas värvus. |
Teisi veresooni |
• |
Tugev kõhuvalu (äge kõht). |
ummistavad verehüübed |
VEREHÜÜBED VEENIS
Mis võib juhtuda, kui veenis tekib verehüüve?
−Kombineeritud hormonaalsete rasestumisvastaste vahendite kasutamist on seostatud verehüüvete tekkeriski suurenemisega veenides (venoosne tromboos). Need kõrvaltoimed ilmnevad siiski harva. Kõige sagedamini esinevad need kombineeritud hormonaalsete rasestumisvastaste vahendite kasutamise esimesel aastal.
−Kui verehüüve tekib jala või jalalaba veenis, võib see põhjustada süvaveenitromboosi.
−Kui verehüüve liigub jalast kopsu, võib see põhjustada kopsuembooliat.
−Väga harva võib verehüüve tekkida teiste organite, nt silma veresoontes (tromboos silma võrkkesta veenis).
Millal on verehüübe tekkimise oht veenis kõige suurem?
Verehüübe tekkimise oht veenis on kõige suurem kombineeritud hormonaalse rasestumisvastase vahendi kasutamise esimesel aastal. Risk võib suureneda ka siis, kui hakkate kombineeritud hormonaalset rasestumisvastast vahendit (kas sama või mõnda muud ravimit) uuesti võtma pärast 4- nädalast või pikemat pausi.
Pärast esimest aastat jääb risk väiksemaks, kuid see on alati veidi suurem sellest, kui te ei kasutaks kombineeritud hormonaalset rasestumisvastast vahendit.
Kui te lõpetate Cleodette võtmise, langeb verehüübe tekkerisk tavalisele tasemele mõne nädala jooksul.
Kui suur on verehüübe tekkerisk?
Risk sõltub teie individuaalsest riskist VTE tekkeks ja sellest, millist kombineeritud hormonaalset rasestumisvastast vahendit te kasutate.
Verehüübe tekkimise üldine risk jalas (süvaveenitromboos) või kopsus (kopsuemboolia) Cleodette võtmise ajal on väike.
−Naistel, kes ei kasuta kombineeritud hormonaalseid rasestumisvastaseid vahendeid ja ei ole rasedad, tekib verehüüve ühe aasta jooksul ligikaudu kahel naisel 10
−Ühe aasta jooksul tekib verehüüve ligikaudu 5…7 naisel 10
−Ühe aasta jooksul tekib verehüüve ligikaudu 9…12 naisel 10
−Verehüübe tekkerisk on erinev, see sõltub teie tervislikust seisundist (vt allolevat lõiku „Faktorid, mis suurendavad verehüübe tekkimise riski“).
|
Verehüübe tekkerisk ühe |
|
aasta jooksul |
Naised, kes ei kasuta kombineeritud hormonaalset |
Ligikaudu kahel naisel 10 |
pilli/plaastrit/rõngast ja kes ei ole rasedad |
|
Naised, kes kasutavad levonorgestreeli, noretisterooni või |
Ligikaudu 5…7 naisel 10 |
norgestimaati sisaldavaid kombineeritud hormonaalseid tablette |
|
Naised, kes kasutavad Cleodette't |
Ligikaudu 9...12 naisel 10 |
Faktorid, mis suurendavad veenis verehüübe tekkeriski
Verehüübe tekkerisk Cleodette kasutamisel on väike, kuid mõned seisundid suurendavad seda riski. Teil on suurem risk:
−kui te olete väga ülekaaluline (kehamassiindeks üle 30 kg/m);
−kui kellelgi teie lähisugulastest on noores eas (nt enne 50. eluaastat) olnud verehüüve jalas, kopsus või mõnes muus elundis. Sel juhul võib teil esineda pärilikku vere hüübimishäiret;
−kui teile plaanitakse teha operatsioon või kui te ei saa kehavigastuse või haiguse tõttu pikka aega liikuda või kui teil on jalg lahases. Vajalikuks võib osutuda Cleodette kasutamise peatamine mitu nädalat enne operatsiooni või ajaks kui te olete vähem liikuvam. Kui te peate lõpetama Cleodette kasutamise, küsige oma arstilt, millal võite jälle ravimit võtma hakata;
−vanemaks saades (eriti üle 35. eluaasta);
−kui te sünnitasite vähem kui mõni nädal tagasi.
Mida rohkem on teil neid eespool loetletud seisundeid , seda suurem on teie verehüübe tekkerisk.
Lennureisid (> 4 tundi) võivad ajutiselt suurendada verehüübe tekkeriski, eriti kui teil esineb ka teisi eelpool loetletud riskifaktoreid.
Oluline on oma arsti teavitada, kui teil esineb mõni nimetatud seisunditest, isegi juhul, kui te ei ole selles päris kindel. Teie arst võib otsustada, et Cleodette kasutamine tuleb lõpetada.
Kui mõni nimetatud seisunditest muutub Cleodette kasutamise ajal, nt kui lähiperekonna liikmel tekib teadmata põhjusel tromboos või kui teie kehakaal oluliselt suureneb, rääkige oma arstiga.
VEREHÜÜBED ARTERIS
Mis võib juhtuda, kui arteris tekib verehüüve?
Nagu verehüüve veenis, võib ka verehüüve arteris põhjustada tõsiseid probleeme. Nt võib see põhjustada südameatakki või insulti.
Faktorid mis suurendavad arteris verehüübe tekkeriski
On oluline märkida, et südameataki või insuldi oht Cleodette kasutamisel on väga väike, kuid see võib suureneda:
−vanuse suurenedes (üle 35. eluaasta);
−kui te suitsetate. Kombineeritud hormonaalse rasestumisvastase vahendi nagu Cleodette kasutamise ajal on soovitatav suitsetamine lõpetada. Kui te ei suuda suitsetamist lõpetada ja olete üle
−kui te olete ülekaaluline;
−kui teil on kõrge vererõhk;
−kui kellelgi teie lähisugulastest on olnud noores eas (enne 50. eluaastat) südameatakki või insulti. Sellisel juhul võib teil olla suurem risk südameataki või insuldi tekkeks;
−kui teil või kellelgi teie lähisugulastest on kõrge rasvade (kolesterool või triglütseriidid) sisaldus veres;
−kui teil esinevad migreenihood, eriti auraga migreen;
−kui teil on probleeme südamega (klapirike, südamerütmihäire, mida nimetatakse kodade virvenduseks);
−kui teil on suhkurtõbi.
Kui teil on rohkem kui üks nendest seisunditest või kui mõni neist on eriti tõsine, võib verehüübe tekkimise oht veelgi suureneda.
Kui mõni nimetatud seisunditest muutub Cleodette kasutamise ajal, nt kui te hakkate suitsetama, kui lähiperekonna liikmel tekib teadmata põhjusel tromboos või kui teie kehakaal oluliselt suureneb, rääkige oma arstiga.
Cleodette ja vähk
Kombineeritud tablette kasutavate naiste seas esineb rinnavähki veidi sagedamini, kuid pole teada, kas see on põhjustatud tablettide kasutamisest. Näiteks võib olla, et kombineeritud tablette kasutavatel naistel avastatakse kasvajaid sagedamini, sest nad käivad sagedamini arstlikul läbivaatusel. Rasestumisvastaste hormonaalsete kombineeritud ravimite kasutamise lõpetamise järel väheneb rinnavähi esinemissagedus
Harvadel juhtudel on tablettide kasutajatel esinenud healoomulisi maksakasvajaid, veelgi harvem pahaloomulisi maksakasvajaid. Kui teil esineb ebatavaliselt tugev kõhuvalu, võtke ühendust oma arstiga.
Veritsus menstruatsioonidevahelisel ajal
Cleodette esimestel kasutuskuudel võivad tekkida ootamatu veritsus (veritsus väljaspool
Mida teha, kui tabletivabal nädalal ei alga vereeritus
Kui olete võtnud kõik tabletid õigesti, pole kannatanud oksendamise või ägeda kõhulahtisuse all ega ole kasutanud muid ravimeid, on rasedus äärmiselt ebatõenäoline.
Kui oodatud vereeritus jääb ära kaks korda järjest, on võimalik, et olete rase. Võtke viivitamatult ühendust arstiga. Ärge alustage järgmise ribapakendiga enne, kui olete kindel, et te pole rase.
Muud ravimid ja Cleodette

Teavitage oma arsti alati kõigist ravimitest või taimsetest preparaatidest, mida te juba kasutate. Samuti teavitage kõiki teisi arste või hambaarsti (või apteekrit), kes teile teisi ravimeid määravad, et te kasutate Cleodette’t. Niisugusel juhul oskavad nad teile öelda kas ja kui kaua te peate lisaks kasutama mõnda muud rasestumisvastast meetodit (näiteks kondoom).
Mõningad ravimid võivad mõjutada Cleodette sisaldust veres ning vähendada selle efektiivsust raseduse ärahoidmisel või põhjustada ootamatuid verejookse. Need hõlmavad:
-ravimeid, mida kasutatakse järgnevate seisundite raviks
-epilepsia (nt primidoon, fenütoiin, barbituraadid, karbamasepiin, okskarbasepiin, felbamaat, topiramaat)
-tuberkuloos (nt rifampitsiin)
-HIV ja viirusliku
-kõrge vererõhk kopsuveresoontes (bosentaan)
-ravimtaim naistepuna.
Cleodette võib mõjutada teiste ravimite toimet, näiteks
-tsüklosporiini sisaldavad ravimid
-epilepsiaravim lamotrigiin (võib põhjustada krambihoogude sagenemist).
Ärge kasutage Cleodette`t, kui teil on
Teie arst määrab teile teist tüüpi rasestumisvastase vahendi, enne kui alustate ravi nende ravimitega. Cleodette kasutamist võib uuesti alustada ligikaudu 2 nädalat pärast selle ravi lõpetamist. Vt lõik „Ärge kasutage Cleodette`t“.
Enne mis tahes ravimi kasutamist küsige nõu oma arstilt või apteekrilt.
Cleodette koos toidu ja joogiga
Cleodette’t võib võtta koos toiduga või ilma, vajadusel vähese koguse veega.
Laboratoorsed analüüsid
Kui teile tuleb teha vereanalüüs, siis teavitage oma arsti või laboripersonali sellest, et te kasutate rasestumisvastaseid tablette, sest hormonaalsed rasestumisvastased tabletid võivad mõjutada mõningate analüüside tulemusi.
Rasedus ja imetamine
Rasedus
Ärge kasutage Cleodette’t, kui te olete rase. Kui te rasestute Cleodette kasutamise ajal, lõpetage kasutamine viivitamatult ja pöörduge oma arsti poole. Kui te soovite rasestuda, võite Cleodette võtmise igal ajal lõpetada (vt ka „Kui soovite Cleodette kasutamist lõpetada“).
Imetamine
Üldjuhul pole Cleodette kasutamine rinnaga toitmise ajal soovitatav. Kui soovite võtta rasestumisvastaseid tablette rinnaga toitmise ajal, pidage nõu oma arstiga.
Kui te olete rase, imetate või arvate end olevat rase või kavatsete rasestuda, pidage enne selle ravimi kasutamist nõu oma arsti või apteekriga.
Autojuhtimine ja masinatega töötamine
Puudub teave selle kohta, et Cleodette mõjutaks kuidagi autojuhtimist või masinate kasutamist.
Cleodette sisaldab laktoosi
Kui arst on teile öelnud, et te ei talu teatud suhkruid, peate te enne selle ravimi kasutamist konsulteerima oma arstiga.
3.Kuidas Cleodette’t võtta
Võtke seda ravimit alati täpselt nii, nagu arst on teile selgitanud. Kui te ei ole milleski kindel, pidage nõu oma arsti või apteekriga.
Võtke iga päev üks Cleodette tablett, vajadusel koos vähese koguse veega. Tablette võib manustada koos toiduga või ilma, kuid neid tuleb manustada iga päev
Ribapakend sisaldab 21 tabletti. Iga tableti kõrvale on trükitud nädalapäev, millal see tuleks võtta. Kui te nt alustate kolmapäevaga, võtke tablett, mille kõrval on kiri „K“. Järgige noole suunda ribapakendil, kuni kõik 21 tabletti on võetud.
Seejärel te 7 päeva tablette ei võta. Nende 7 tabletivaba päeva jooksul (nimetatakse ka pausi- või vahenädalaks) peaks algama veritsus. See nn „läbimurdeveritsus“ algab tavaliselt vahenädala 2. või 3. päeval.
8. päeval pärast viimase Cleodette tableti võtmist (s.o pärast
Kui kasutate Cleodette’t vastavalt nendele juhistele, olete rasestumise eest kaitstud ka nende 7 päeva jooksul, mil te ei võta tablette.
Millal te võite alustada esimese ribaga
Kui te pole eelmisel kuul kasutanud hormoone sisaldavaid rasestumisvastaseid vahendeid Alustage Cleodette kasutamist tsükli esimesel päeval (s.t menstruatsiooni esimesel päeval). Kui
alustate Cleodette kasutamist menstruatsiooni esimesel päeval, olete koheselt raseduse eest kaitstud. Võite alustada ka tsükli 2...5. päeval, kuid niisugusel juhul peate esimese 7 päeva jooksul kasutama täiendavaid kaitsevahendeid (nt kondoom).
Üleminek kombineeritud hormonaalselt rasestumisvastaselt ravimilt või kombineeritud rasestumisvastaselt tuperõngalt või plaastrilt
Cleodette kasutamist tuleb eelistatavalt alustada eelnevalt kasutatud toimeainet sisaldava viimase tableti (viimane toimeainet sisaldav tablett) manustamisele järgneval päeval, kuid hiljemalt eelnevalt kasutatud tablettide tabletivabale päevale (või eelnevalt kasutatud tablettide viimase platseebotableti manustamisele) järgneval päeval. Üleminekul kombineeritud rasestumisvastaselt tuperõngalt või plaastrilt, järgige oma arsti nõuandeid.
Üleminek ainult progestageeni sisaldavalt meetodilt (ainult progestageeni sisaldavad tabletid, süst, implantaat või progestageeni vabastav emakasisene süsteem)
Üleminek ainult progestageeni sisaldavatelt tablettidelt on lubatud igal ajal (implantaadilt või emakasiseselt süsteemilt selle eemaldamise päeval, süstitavalt preparaadilt järgmise süsti ettenähtud päeval), kuid kõigil nendel juhtudel peate kasutama täiendavaid rasestumisvastaseid kaitsevahendeid (näiteks kondoom) tablettide võtmise esimese 7 päeva jooksul.
Pärast aborti
Järgige oma arsti nõuandeid.
Pärast sünnitust
Cleodette kasutamist võib alustada 21...28 päeva pärast sünnitust. Kui alustate hiljem kui 28. päeval, peate kasutama nn barjäärimeetodit (näiteks kondoom) Cleodette kasutamise esimese 7 päeva jooksul. Kui olete pärast sünnitust olnud vahekorras enne Cleodette kasutamise (taas)alustamist, peate veenduma selles, et te pole rase või ootama ära järgmise menstruatsioonini.
Kui toidate last rinnaga ja soovite pärast sünnitust (taas)alustada Cleodette kasutamist
Loe lõiku „Imetamine“.
Küsige oma arstilt nõu, kui te ei ole kindel, millal alustada.
Kui te võtate Cleodette’t rohkem kui ette nähtud
Puuduvad teated Cleodette tablettide üleannustamisest põhjustatud tõsiste kahjustuste kohta.
Kui te võtate mitu tabletti korraga, võib see põhjustada iiveldust või oksendamist. Noortel neidudel võib esineda verejooks tupest.
Kui olete võtnud liiga palju Cleodette tablette või kui avastate, et neid on sisse võtnud laps, pöörduge nõu saamiseks arsti või apteekri poole.
Kui te unustate Cleodette’t võtta
−Kui olete tableti võtmisega hilinenud alla 12 tunni, ei vähene rasestumisvastane kaitse. Võtke tablett niipea, kui see teile meenub ning jätkake tablettide võtmist tavalistel aegadel.
−Kui olete tableti võtmisega hilinenud üle 12 tunni, võib rasestumisvastane kaitse olla vähenenud. Mida rohkem tablette olete unustanud, seda suurem on risk rasestuda.
Rasestumisvastase kaitse puudumise risk on suurim, kui unustate tableti võtmata pakendi alguses või lõpus. Seetõttu tuleb kinni pidada järgnevatest reeglitest (vt diagramm allpool):
Ununenud on enam kui üks tablett samast ribapakendist
Pöörduge arsti poole.
Ununenud on üks tablett 1. nädalal
Võtke ununenud tablett niipea, kui see teile meenub, isegi kui see tähendab kahe tableti korraga võtmist. Jätkake tablettide võtmist tavalisel ajal ning rakendage täiendavaid ettevaatusabinõusid (näiteks kondoom) järgneva 7 päeva jooksul. Kui olete olnud vahekorras tablettide võtmise unustamisele eelneval nädalal, peate arvestama võimalusega, et olete rase. Niisugusel juhul pöörduge oma arsti poole.
Ununenud on üks tablett 2. nädalal
Võtke ununenud tablett niipea, kui see teile meenub, isegi kui see tähendab kahe tableti korraga võtmist. Jätkake tablettide võtmist tavalisel ajal. Rasestumisvastane kaitse ei ole vähenenud ja täiendavate ettevaatusabinõude rakendamine pole vajalik.
Ununenud on üks tablett 3. nädalal
Valida saab kahe variandi vahel:
1.Võtke ununenud tablett niipea, kui see teile meenub, isegi kui see tähendab kahe tableti korraga manustamist. Jätkake tablettide võtmist tavalisel ajal. Tabletivaba perioodi tegemise asemel alustage uue ribapakendiga.
Kõige tõenäolisemalt on teil päevad teise ribapakendi lõpus, kuid teil võib esineda kerget või menstruatsioonilaadset veritsust teise ribapakendi võtmise ajal.
2.Te võite ka lõpetada olemasoleva ribapakendiga ja kohe üle minna
Kui järgite ühte neist kahest soovitusest, säilib rasestumisvastane kaitse.
Kui te olete unustanud võtta mõne tableti ribapakendis ja teil ei teki verejooksu
Unustatud rohkem, kui 1 |
|
Pöörduge arsti poole |
tablett blistrist võtta |
|
|
|
|
|
|
|
⇑ |
|
|
|
|
|
|
|
Jah |
|
|
|
|
|
|
|
⇑ |
|
|
|
|
|
|
|
|
|
|
|
1. nädal |
|
|
Te olite nädal enne tableti vahelejätmist |
|
|
|
|
|
|
|
vahekorras? |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⇓ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ei |
|
|
|
|
|
|
|
⇓ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- Võtke vahele jäänud tablett |
|
|
|
|
|
|
|
- Kasutage 7 päeva lisakaitsevahendit |
|
|
|
|
|
|
|
- Kasutage pakend lõpuni |
|
|
|
|
|
|
|
||
Ununes ainult 1 tablett |
|
|
2. nädal |
|
|
- Võtke vahele jäänud tablett |
|
(rohkem kui 12 tundi |
|
|
|
|
|
− Kasutage pakend lõpuni |
|
hiljem) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
− Võtke vahele jäänud tablett |
|
|
|
|
|
|
|
− Kasutage pakend lõpuni |
|
|
|
|
|
|
|
− Ärge jätke tabletivaba intervalli kahe |
|
|
|
|
|
|
|
|
pakendi vahele |
|
|
|
|
|
|
− Jätkake järgmise pakendiga |
|
|
|
|
|
|
|
|
|
|
|
|
3. nädal |
|
|
|
või |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
Lõpetage kohe tablettide võtmine |
|
|
|
|
|
|
- |
Tehke tabletivaba vahe (mitte rohkem |
|
|
|
|
|
|
|
kui 7 päeva k.a võtmata jäänud |
|
|
|
|
|
|
|
tablett) |
|
|
|
|
|
|
− Jätkake seejärel uue pakendiga |
|
|
|
|
|
|
|
|
|
Mida teha oksendamise või ägeda kõhulahtisuse korral
Kui te oksendate 3...4 tunni jooksul pärast tableti võtmist või kui teil on äge kõhulahtisus, võib olla oht, et toimeained ei imendu täielikult teie organismi. Sisuliselt sarnaneb see olukord tableti unustamisega. Oksendamise või kõhulahtisuse järgselt võtke uus tablett varupakendist niipea kui võimalik. Võimalusel võtke see 12 tunni jooksul pärast tavapärast tableti võtmise aega. Kui see pole võimalik või kui möödunud on üle 12 tunni, peate te järgima nõuandeid, mis on toodud lõigus „Kui te unustate Cleodette’t võtta“.
Menstruatsiooni edasilükkamine: mida peate teadma
Ehkki see pole soovitav, võite menstruatsiooni edasi lükata alustades kohe uue Cleodette ribapakendiga ja võtate selle lõpuni, jättes tabletivaba perioodi vahele. Selle teise ribapakendi kasutamise ajal võib tekkida määrimine või menstruatsioonilaadne veritsus. Pärast tavalist
Enne, kui te otsustate menstruatsiooni edasi lükata, peaksite küsima nõu oma arstilt.
Menstruatsiooni alguspäeva muutmine: mida peate teadma
Kui te võtate tablette vastavalt juhistele, siis algab teil menstruatsioon tabletivaba nädala jooksul. Kui te soovite seda päeva muuta, siis lühendage tabletivabade päevade arvu (kuid ärge seda kunagi pikendage – 7 on maksimum!). Näiteks, kui teil algas siiani tabletivaba periood reedel ja te tahate, et see edaspidi algaks teisipäeval (3 päeva varem), tuleb teil alustada järgmise ribapakendiga 3 päeva varem kui tavaliselt. Kui te teete tabletivaba perioodi liiga lühikeseks (nt 3 päeva või vähem), võib teil verejooksu mitte tekkida nende päevade jooksul. Teil võib aga esineda määrimist või menstruatsioonilaadne verejooks.
Kui te pole kindel, kuidas toimida, pidage nõu oma arstiga.
Kui te lõpetate Cleodette võtmise
Te võite lõpetada Cleodette kasutamise ükskõik millal te soovite. Kui te soovite rasedust vältida, küsige nõu arstilt muude usaldusväärsete rasestumisvastaste meetodite kohta. Kui te soovite rasestuda, siis lõpetage Cleodette võtmine ja oodake ära menstruatsioon, enne kui proovite rasestuda. Te saate palju kergemini välja arvutada sünnituskuupäeva.
Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti või apteekriga.
4.Võimalikud kõrvaltoimed
Nagu kõik ravimid, võib ka see ravim põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki. Kui teil tekib ükskõik milline kõrvaltoime, eriti kui see on raske ja püsiv; või kui teil tekib mõni tervisehäire, mis võib olla tingitud Cleodette kasutamisest, siis rääkige sellest palun oma arstile.
Kõikidel kombineeritud hormonaalseid rasestumisvastaseid vahendeid kasutavatel naistel suureneb verehüüvete tekkerisk veenides (venoosne trombemboolia, VTE) või arterites (arteriaalne trombemboolia, ATE). Täpsemat teavet kombineeritud hormonaalsete rasestumisvastaste vahendite kasutamisega seotud erinevate riskide kohta vt lõigust 2 „Mida on vaja teada enne Cleodette kasutamist“.
Järgnev loetelu kõrvaltoimetest on seotud Cleodette kasutamisega.
Sageli esinevad kõrvaltoimed (võivad ilmneda kuni 1 inimesel
−meeleolu kõikumised
−peavalu
−kõhuvalu (maovalu)
−akne
−rindade valulikkus, rindade suurenemine, rindade tundlikkus, valulikud või ebaregulaarsed menstruatsioonid
−kehakaalu suurenemine.
−kandidiaas (seennakkus)
−ohatis (herpes simplex)
−allergilised reaktsioonid
−söögiisu suurenemine
−depressioon, närvilisus, unehäired
−torkimisetunne, peapööritus (vertigo)
−nägemisprobleemid
−südame rütmihäired või ebatavaliselt kiire südame löögisagedus
−kõrge vererõhk, madal vererõhk, migreen, veenilaiendid
−kurguvalu
−iiveldus, oksendamine, mao- ja/või soolepõletik, kõhulahtisus, kõhukinnisus
−naha ja/või limaskestade (nt keel või kõri) äkiline paistetus ja/või neelamisraskus või lööve koos hingamisraskusega (angioödeem), juuste väljalangemine (alopeetsia), ekseem, sügelus, nahalööbed, kuiv nahk, rasune nahk (seborroiline dermatiit)
−kaelavalu, jäsemete valu, lihasekrambid
−põiepõletik
−tükk rinnas (hea- ja pahaloomuline), piimaeritus väljaspool rasedust (galaktorröa), munasarja tsüstid, kuumahood, menstruatsiooni puudumine, väga vererohke menstruatsioon, tupeeritis, tupekuivus, valud alakõhus, normist erinev emakakaela äigepreparaat
−vedelikupeetus, energiapuudus, ülemäärane janu, suurenenud higistamine
−kehakaalu kaotus.
Harva esinevad kõrvaltoimed (võivad ilmneda kuni 1 inimesel
−astma
−kuulmiskahjustus
−nodoosne erüteem (iseloomulikud valulikud punetavad sõlmed nahal)
−multiformne erüteem (lööve koos märklauakujulise punetuse või haavanditega)
−ohtlikud verehüübed veenis või arteris, nt:
-jalas või jalalabas (süvaveenitromboos)
-kopsus (kopsuemboolia)
-südameatakk
-insult
-miniinsult või ajutised insuldilaadsed sümptomid, mida nimetatakse mööduvaks isheemiliseks atakiks
-verehüübed maksas, maos/soolestikud, neerudes või silmas.
Verehüüvete tekkerisk võib tõusta, kui teil esineb ka teisi seda riski suurendavaid seisundeid (lisateavet verehüübe tekkeriski suurendavate seisundite ja verehüübe sümptomite kohta vt lõigust 2).
Kõrvaltoimetest teavitamine
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga. Kõrvaltoime võib olla ka selline, mida selles infolehes ei ole nimetatud. Kõrvaltoimetest võite ka ise teavitada www.ravimiamet.ee kaudu. Teavitades aitate saada rohkem infot ravimi ohutusest.
5.Kuidas Cleodette’t säilitada
Hoidke seda ravimit laste eest varjatud ja kättesaamatus kohas.
See ravimpreparaat ei vaja säilitamisel eritingimusi.
Ärge kasutage seda ravimit pärast kõlblikkusaega, mis on märgitud pakendil pärast „Kõlblik kuni“. Kõlblikkusaeg viitab selle kuu viimasele päevale.
Ärge visake ravimeid kanalisatsiooni ega olmejäätmete hulka. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. Need meetmed aitavad kaitsta keskkonda.
6. Pakendi sisu ja muu teave
Mida Cleodette sisaldab
-Toimeained on 0,02 mg etünüülöstradiooli ja 3 mg drospirenooni.
-Teised koostisosad on
-Tableti sisu: laktoosmonohüdraat, eelželatiniseeritud (maisi)tärklis, povidoon
-Tableti kate: osaliselt hüdrolüüsitud polüvinüülalkohol, titaandioksiid (E 171), makrogool 3350, talk (E 553b), kollane raudoksiid (E 172), punane raudoksiid (E 172), must raudoksiid (E 172).
Kuidas Cleodette välja näeb ja pakendi sisu
Roosad, ümmargused, õhukese polümeerikattega tabletid.
Cleodette on saadaval 1, 2, 3, 6 ja 13 blistriga karbis, igas blistris 21 tabletti.
Blistrid võivad olla ka blistrihoidjas.
Kõik pakendi suurused ei pruugi olla müügil.
Müügiloa hoidja ja tootja
Müügiloa hoidja
Actavis Group PTC ehf
Reykjavíkurvegi
Island
Tootja
Laboratorios León Farma, S.A. C/ La Vallina s/n
Pol. Ind. Navatejera 24008, Navatejera – León Hispaania
Lisaküsimuste tekkimisel selle ravimi kohta pöörduge palun müügiloa hoidja kohaliku esindaja poole: UAB Actavis Baltics Eesti Filiaal,
Tiigi 28/Kesk tee 23a, Jüri, Rae vald,
75301 Harjumaa Tel: (+372) 6100565
Infoleht on viimati uuendatud novembris 2017.
RAVIMI OMADUSTE KOKKUVÕTE
1.RAVIMPREPARAADI NIMETUS
Cleodette, 0,02 mg/3 mg õhukese polümeerikattega tabletid
2.KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Iga õhukese polümeerikattega tablett sisaldab 0,02 mg etünüülöstradiooli ja 3 mg drospirenooni. INN. Ethinylestradiolum, drospirenonum
Teadaolevat toimet omav abiaine:
Iga õhukese polümeerikattega tablett sisaldab 44 mg laktoosmonohüdraati.
Abiainete täielik loetelu vt lõik 6.1.
3.RAVIMVORM
Õhukese polümeerikattega tablett.
Roosad, ümmargused, siledad õhukese polümeerikattega tabletid, mõõtudega 5,7 x 3,5 mm.
4.KLIINILISED ANDMED
4.1Näidustused
Raseduse vältimine.
Cleodette väljakirjutamisel tuleb võtta arvesse konkreetsel naisel käesoleval hetkel esinevaid riskifaktoreid, eriti venoosse trombemboolia (VTE) riskifaktoreid, ja seda, milline on VTE risk koos Cleodette'ga võrreldes teiste kombineeritud hormonaalsete kontratseptiividega (vt lõigud 4.3 ja 4.4).
4.2Annustamine ja manustamisviis
Annustamine
Tablette tuleb võtta iga päev
Kuidas alustada Cleodette võtmist
•Hormonaalseid rasestumisvastaseid vahendeid pole eelnevalt (möödunud kuul) kasutatud Tablettide võtmist tuleb alustada naise normaalse menstruaaltsükli 1. päeval (st menstruaalverejooksu esimesel päeval).
•Üleminek kombineeritud hormonaalselt rasestumisvastaselt vahendilt (kombineeritud
suukaudne kontratseptiiv (KSK), tuperõngas või nahaplaaster)
Eelistatult peaks naine Cleodette’ga alustama varem kasutatud KSK viimase aktiivse tableti (viimase toimeainet sisaldava tableti) võtmisele järgneval päeval, kuid hiljemalt eelneva KSK tavapärasele tabletivabale perioodile või platseebotablettide perioodile järgneval päeval. Tuperõngalt või nahaplaastrilt üleminekul tuleb Cleodette kasutamist eelistatavalt alustada selle eemaldamise päeval, kuid hiljemalt vastava vahendi ettenähtud järgmise paigaldamise ajal.
-Üleminek ainult progestageeni sisaldavalt meetodilt (ainult progestageeni sisaldav tablett, süst,
Naine võib ainult progestageenselt tabletilt üle minna mis tahes päeval (implantaadi või emakasisese vahendi kasutamisel selle eemaldamise päeval; süstitava preparaadi kasutamisel päeval, mil peaks tehtama järgmine süst), kuid kõigil neil juhtudel on soovitatav kasutada esimesel
-Esimese trimestri abordi järgselt
Naine võib alustada kohe. Sellisel juhul ei ole täiendavate rasestumisvastaste meetmete rakendamine vajalik.
-Sünnituse või teise trimestri abordi järgselt
Soovitatav on alustada 21...28. päeval pärast sünnitust või teise trimestri aborti. Hilisema alguse korral tuleb naisele soovitada barjäärimeetodi täiendavat kasutamist esimese 7 päeva jooksul. Kui aga vahekord on juba aset leidnud, tuleb enne KSK kasutamist välistada rasedus või oodata ära esimene menstruatsioon.
Rinnaga toitvate naiste kohta vt lõik 4.6.
Mida teha kui tablett jäi võtmata
Kui kasutaja on tableti võtmisega hilinenud vähem kui 12 tundi, ei ole rasestumisvastane toime nõrgenenud. Naine peab võtmata jäänud tableti võtma niipea, kui see talle meenub. Edasi tuleb tablette võtta tavapärastel aegadel.
Kui kasutaja on tableti võtmisega hilinenud rohkem kui 12 tundi, võib rasestumisvastane toime olla nõrgenenud. Unustatud tablettide korral on vaja järgida kahte põhireeglit:
1.Tablettide manustamist ei tohi kunagi katkestada kauemaks kui 7 päevaks.
2.
Sellest lähtuvalt saab igapäevases praktikas anda järgnevat nõu:
-1. nädal
Kasutaja peab võtma viimase võtmata jäänud tableti niipea, kui see talle meenub, isegi kui see tähendab, et samal ajal tuleb võtta kaks tabletti. Seejärel tuleb tablettide võtmist jätkata tavapärasel ajal. Lisaks tuleb järgneva 7 päeva jooksul kasutada ka barjäärimeetodit, nt kondoomi. Kui kasutaja oli eelneva 7 päeva jooksul vahekorras, tuleb arvestada võimaliku rasedusega. Mida rohkem tablette on võtmata jäänud ning mida lähemale jääb see tabletivabale perioodile, seda suurem on rasestumise risk.
-2. nädal
Kasutaja peab võtma viimase võtmata jäänud tableti niipea, kui see talle meenub, isegi kui see tähendab, et samal ajal tuleb võtta kaks tabletti. Seejärel tuleb tablettide võtmist jätkata tavapärasel ajal. Eeldusel, et esimesele ununenud tabletile eelnenud 7 päeval on tablette manustatud õigesti, pole täiendavate rasestumisvastaste abinõude rakendamine vajalik. Kui aga võtmata on jäänud enam kui 1 tablett, tuleb järgneva 7 päeva jooksul rakendada täiendavaid abinõusid raseduse vältimiseks.
-3. nädal
Läheneva
1.Kasutaja peab võtma viimase võtmata jäänud tableti niipea, kui see talle meenub, isegi kui see tähendab, et samal ajal tuleb võtta kaks tabletti. Seejärel tuleb tablettide võtmist jätkata tavapärasel ajal. Järgmise blisterpakendiga tuleb alustada kohe pärast eelmise lõpetamist, st kahe pakendi vahele ei tohi jätta tabletivaba perioodi. Tõenäoliselt ei ilmne kasutajal menstruatsioonilaadset vereeritust enne, kui teine pakend on lõpuni kasutatud, kuid tablettide võtmise ajal võib tal esineda määrivat vereeritust.
2.Naisele võib ka soovitada lõpetada tablettide võtmine käigusolevast blisterpakendist. Seejärel tuleb pidada kuni
Kui naisel jäi tablett võtmata ja pärast seda ei esinenud esimesel tavapärasel tabletivabal perioodil menstruatsioonilaadset vereeritust, tuleb arvestada raseduse võimalusega.
Mida teha seedetrakti häirete korral
Raskete seedetrakti häirete (nt oksendamine või kõhulahtisus) korral ei pruugi imendumine olla täielik ja rakendada tuleb täiendavaid rasestumisvastaseid meetmeid. Kui oksendamine esineb 3...4 tunni jooksul pärast tableti manustamist, tuleb esimesel võimalusel võtta uus
Kuidas menstruatsioonilaadset vereeritust edasi lükata
Menstruatsiooni edasilükkamiseks peab kasutaja alustama uut Cleodette blisterpakendit ilma tabletivaba perioodita. Pikendamine on võimalik soovitud arvu päevade võrra kuni teise pakendi lõppemiseni. Pikendamise vältel on võimalik läbimurdeveritsus või määrimine. Regulaarset Cleodette võtmist jätkatakse pärast tavalist
Kui soovitakse menstruatsiooni algust nihutada mõnele teisele, senikasutatavast skeemist erinevale nädalapäevale, tuleb tabletivaba intervalli lühendada vastavalt nii mitu päeva kui soovitakse. Mida lühemaks jääb intervall, seda väiksem on menstruatsioonilaadse vereerituse esinemise võimalus ning seda suurem on läbimurdeveritsuse ja määriva vereerituse võimalus teise pakendi kasutamise ajal (sarnaselt tsükli pikendamisele).
Manustamisviis
Suukaudne.
4.3Vastunäidustused
Kombineeritud hormonaalseid kontratseptiive (KHK) ei tohi kasutada järgmiste seisundite esinemisel. Kui mõni neist seisunditest ilmneb esmakordselt KHK kasutamise ajal, tuleb preparaadi kasutamine viivitamatult lõpetada.
−Venoosne trombemboolia (VTE) või selle tekkerisk.
-Venoosne trombemboolia - käesolev
-Teadaolev pärilik või omandatud eelsoodumus venoosse trombemboolia tekkeks, nt aktiveeritud
-Suurem kirurgiline protseduur koos pikaajalise liikumatusega (vt lõik 4.4).
-Mitme riskifaktori esinemisest tingitud venoosse trombemboolia kõrge risk (vt lõik 4.4).
−Arteriaalne trombemboolia (ATE) või selle tekkerisk.
-Arteriaalne trombemboolia - käesolev või anamneesis (nt müokardiinfarkt) või selle eelne seisund (nt stenokardia).
-Tserebrovaskulaarne haigus – insult praegu või anamneesis või selle eelne seisund (nt mööduv isheemiline atakk).

-Teadaolev pärilik või omandatud eelsoodumus arteriaalse trombemboolia tekkeks, nt hüperhomotsüsteineemia ja fosfolipiidivastased antikehad (kardiolipiinivastased antikehad, luupusantikoagulant).
-Varem esinenud koldeliste neuroloogiliste sümptomitega migreen.
-Kõrge risk arteriaalse trombemboolia tekkeks mitme riskifaktori esinemise tõttu (vt lõik 4.4) või kui esineb üks tõsine riskifaktor näiteks:
-vaskulaarsete sümptomitega suhkurtõbi
-raske hüpertensioon
-raske düslipoproteineemia.
−Raske maksahaigus käesolevalt või anamneesis, kuni maksafunktsiooni näitajad pole normaliseerunud.
−Raske neerupuudulikkus või äge neerukahjustus.
−Maksakasvaja (hea- või pahaloomuline) käesolevalt või anamneesis.
−Teadaolev või kahtlustatav suguhormoonidest sõltuv (näiteks suguelundite või rinnanäärmete) pahaloomuline kasvaja.
−Ebaselge etioloogiaga vaginaalne verejooks.
−Ülitundlikkus toimeainete või lõigus 6.1 loetletud mis tahes abiainete suhtes.
−Cleodette samaaegne kasutamine ombitasviiri/ paritapreviiri/ ritonaviiri ja dasabuviiri sisaldavate ravimitega on vastunäidustatud (vt lõigud 4.4 ja 4.5).
4.4Erihoiatused ja ettevaatusabinõud kasutamisel
Hoiatused
Kui esineb ükskõik milline allpool nimetatud seisunditest või riskifaktoritest, tuleb Cleodette sobivust arutada koos naisega. Naisele tuleb öelda, et nimetatud seisundite või riskifaktorite ägenemisel või esmakordsel ilmnemisel tuleb pöörduda oma arsti poole, et teha kindlaks, kas Cleodette kasutamine tuleb katkestada.
Arvesse tuleb võtta ka antikoagulantravi võimalust. Antikogulantravi (kumariinid) teratogeensuse tõttu tuleb alustada alternatiivse kontratseptsiooniga.
Venoosse trombemboolia (VTE) risk
Mis tahes kombineeritud hormonaalse kontratseptiivi (KHK) kasutamine suurendab venoosse trombemboolia (VTE) tekkeriski võrreldes mittekasutamisega. Levonorgestreeli, norgestimaati või noretisterooni sisaldavad ravimid on madalaima VTE tekkeriskiga. Teistel ravimitel, nt Cleodette, võib VTE risk olla kuni kaks korda suurem. Otsus mis tahes ravimi kasutamise kohta, mis ei ole madalaima VTE tekkeriskiga, tuleb teha alles pärast naisega nõu pidamist, veendumaks, et ta mõistab Cleodette kasutamisega seotud VTE tekkeriski; seda, kuidas tema olemasolevad riskifaktorid seda riski mõjutavad ja et tema VTE tekkerisk on kõige kõrgem esimesel kasutamisaastal. On olemas ka mõned tõendid selle kohta, et VTE risk suureneb ka
Naistel, kes ei kasuta
Hinnanguliselt1 tekib VTE ühe aasta jooksul 9…12 naisel 10
VTE juhtude arv aastas on mõlemal juhul väiksem, kui VTE eeldatav esinemissagedus raseduse ajal või sünnitusjärgsel perioodil.
VTE võib 1…2% juhtudest lõppeda surmaga.
1 Need juhud määratleti epidemioloogilise uuringu kõikide andmete alusel, kasutades erinevate ravimite suhtelisi riske
võrrelduna levonorgestreeli sisaldavate
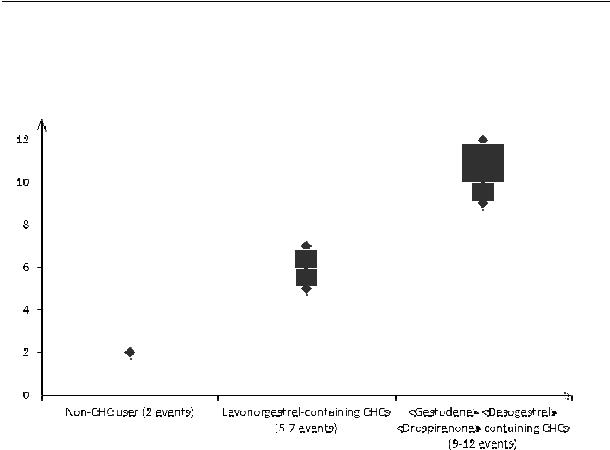
2 Levonorgestreeli sisaldavate
VTE juhtude arv 10 000 naise kohta ühes aastas
VTE
 juhtude arv
juhtude arv
|
Levonorgestreeli sisaldavad |
|
Drospirenooni sisaldavad |
|
|
|
(5…7 juhtu) |
|
(9…12 juhtu) |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
Väga harva on
VTE riskifaktorid
KHK kasutajatel võib venoosse trombemboolia tüsistuste risk märkimisväärselt suureneda naistel, kellel esinevad täiendavad riskifaktorid, eriti, kui neid on mitu (vt tabel).
Cleodette on vastunäidustatud, kui naisel on mitu riskifaktorit, mille tõttu on risk venoosse tromboosi tekkeks kõrge (vt lõik 4.3). Kui naisel on riskifaktoreid rohkem kui üks, võib riski suurenemine olla suurem kui üksikute riskifaktorite summa. Sellisel juhul tuleb arvestada naise VTE koguriskiga. Kui ravimi kasu/riski suhet peetakse negatiivseks, ei tohi
Tabel: VTE riskifaktorid
Riskifaktor |
Märkus |
Rasvumine (kehamassiindeks üle 30 |
KMI tõusuga suureneb risk märkimisväärselt. |
kg/m²) |
Eriti oluline on seda arvestada juhul, kui esineb ka teisi |
|
riskifaktoreid. |
Riskifaktor |
Märkus |
Pikaajaline liikumatus, suurem |
Nendel juhtudel on soovitatav plaastri/pilli/rõnga kasutamine |
kirurgiline protseduur, mis tahes |
katkestada (plaanilise kirurgilise protseduuri korral vähemalt |
jalgade või vaagnapiirkonna |
neli nädalat varem) ja mitte taasalustada enne, kui täielikust |
operatsioon, neurokirurgia või |
liikumisvõime taastumisest on möödunud kaks nädalat. |
ulatuslik trauma |
Soovimatu raseduse vältimiseks tuleb kasutada muud |
|
rasestumisvastast vahendit. |
|
Kui Cleodette kasutamist ei ole eelnevalt katkestatud, tuleb |
|
kaaluda tromboosivastast ravi. |
Märkus: ajutine liikumatus, sh |
|
lennureis kestusega üle 4 tunni, võib |
|
samuti olla VTE riskifaktoriks, eriti |
|
naistel, kellel esineb ka teisi |
|
riskifaktoreid |
|
Esinemine perekonnas (venoosne |
Päriliku eelsoodumuse kahtlusel tuleb enne mis tahes KHK |
trombemboolia õdedel/vendadel või |
määramise otsust saata naine eriarsti konsultatsioonile. |
vanematel, eriti just suhteliselt |
|
noores eas, nt enne 50. eluaastat) |
|
Teised |
Vähkkasvaja, süsteemne erütematoosluupus, hemolüütilis- |
haigusseisundid |
ureemiline sündroom, krooniline põletikuline soolehaigus |
|
(Crohni tõbi või haavandiline koliit) ja sirprakuline aneemia. |
Vanuse tõus |
Eriti üle 35 aasta. |
Puudub üksmeel varikoossete veenide ja pindmise tromboflebiidi võimaliku rolli kohta venoosse tromboosi tekkimisel või progresseerumisel.
Arvestada tuleb trombemboolia tekkeriski suurenemist raseduse ajal ja eriti 6 nädala vältel pärast sünnitust (teavet raseduse ja imetamise kohta vt lõigust 4.6).
VTE sümptomid (süvaveenitromboos ja kopsuemboolia)
Sümptomite ilmnemisel tuleb soovitada naistele kohest arsti poole pöördumist ning tervishoiutöötajate teavitamist sellest, et ta kasutab
Süvaveenitromboosi sümptomid võivad olla:
−ühepoolne jala ja/või jalalaba paistetus või paistetus piki jalaveeni;
−valu või tundlikkus jalas, mis võib tunda anda ainult seistes või kõndides;
−haige jala kõrgem temperatuur, jalanaha punetus või värvimuutus.
Kopsuemboolia sümptomid võivad olla:
–äkki tekkinud ebaselge põhjusega õhupuudus või kiire hingamine;
–äkki tekkinud köha, millega võib kaasneda veriköha;
–terav valu rindkeres;
–tugev peapööritus või pearinglus;
–kiire või ebakorrapärane südamerütm.
Mõned nendest sümptomitest (nt õhupuudus, köha) on mittespetsiifilised ja neid võidakse ekslikult tõlgendada tavalisemate või vähemtõsiste haigustena (nt hingamisteede nakkused).
Veresoone sulgusele viitavad teised nähud võivad olla jäseme äkiline valu, paistetus ja kergelt sinine värvus.
Kui veresoone sulgus tekib silmas, võivad sümptomid varieeruda valutust hägustunud nägemisest kuni nägemiskaotuseni. Mõnikord võib nägemiskaotus tekkida peaaegu kohe.
Arteriaalse trombemboolia (ATE) risk
Epidemioloogilised uuringud on seostanud
ATE riskifaktorid
Riskifaktoritega
Tabel: ATE riskifaktorid
Riskifaktor |
Märkus |
Vanuse tõus |
Eriti üle 35 aasta. |
Suitsetamine |
Naistel tuleb soovitada mitte suitsetada, kui nad soovivad |
|
kasutada |
|
suitsetamist, tuleb tungivalt soovitada kasutada mõnda teist |
|
rasestumisvastast meetodit. |
Hüpertensioon |
|
Rasvumine (kehamassiindeks üle |
KMI tõusuga suureneb risk märkimisväärselt. |
30 kg/m²) |
Eriti oluline naistel, kellel esineb ka teisi riskifaktoreid. |
Esinemine perekonnas (arteriaalne |
Päriliku eelsoodumuse kahtluse korral tuleb enne mis tahes |
trombemboolia õdedel/vendadel või |
KHK määramise otsust saata naine eriarsti konsultatsioonile. |
vanematel, eriti just suhteliselt |
|
noores eas, nt enne 50. eluaastat) |
|
Migreen |
Migreeni esinemissageduse või raskusastme suurenemine (mis |
|
võib olla tserebrovaskulaarse häire varajaseks sümptomiks) |
|
KHK kasutamise ajal võib olla ravimi kasutamise kohese |
|
katkestamise põhjuseks. |
Teised vaskulaarsete häiretega |
Suhkurtõbi, hüperhomotsüsteineemia, südameklapi kahjustus |
seotud haigusseisundid |
ja kodade virvendus, düslipoproteineemia ja süsteemne |
|
erütematoosluupus. |
ATE sümptomid
Sümptomite ilmnemisel tuleb naistele soovitada kohest arsti poole pöördumist ning tervishoiutöötajate teavitamist sellest, et ta kasutab
Tserebrovaskulaarse haiguse sümptomid võivad olla:
–äkki tekkinud tuimus või nõrkus näos, käsivarres või jalas, eriti ühel kehapoolel;
–äkki tekkinud kõndimisraskus, pearinglus, tasakaalu- või koordinatsioonihäired;
–äkki tekkinud segasusseisund, rääkimis- või mõistmisraskus;
–äkki tekkinud nägemishäire ühes või mõlemas silmas;
–äkki tekkinud, tugev või pikaajaline teadmata põhjusega peavalu;
–teadvusekaotus või minestamine krampidega või ilma.
Ajutised sümptomid viitavad mööduvale isheemilisele atakile (TIA, transient ischaemic attack).
Müokardiinfarkti sümptomid võivad olla:
–valu, ebamugavustunne, survetunne, raskustunne, pigistus- või täistunne rindkeres, käsivarres või rinnaku all;
–ebamugavustunne, mis kiirgub selga, lõuga, kõripiirkonda, käsivarde, kõhtu;
–täistunne, seedehäired või lämbumistunne;
–higistamine, iiveldus, oksendamine või pearinglus;
–äärmine nõrkus, ärevus või õhupuudus;
–kiire või ebakorrapärane südamerütm.
Kasvajad
Mõnedes epidemioloogilistes uuringutes on pikaaegsetel (>5 aasta)
54 epidemioloogilise uuringu metaanalüüs näitas, et hetkel
diagnoositud rinnavähi juhud kalduvad olema kliiniliselt varasemas arengustaadiumis kui mitte kunagi kasutajatel.
Harvadel juhtudel on
Suureannuseliste
Kliinilistes uuringutes
Muud seisundid
Cleodette’s sisalduv progestogeen on kaaliumi säästvate omadustega aldosterooni antagonist. Enamikul juhtudest ei esine kaaliumitaseme tõusu. Ühes kliinilises uuringus suurenes siiski kerge või mõõduka neerukahjustusega patsientidel vähesel määral, kuid mitte märkimisväärselt seerumi kaaliumitase kui drospirenooni võeti samaaegselt kaaliumi säästvate ravimitega. Seetõttu soovitatakse neerupuudulikkusega patsientidel, kellel seerumi kaaliumitase on enne ravi alustamist normi ülemisel piiril, kontrollida seerumi kaaliumitaset esimese ravitsükli ajal, seda eriti juhul, kui samaaegselt kasutatakse kaaliumisäästvaid ravimeid. Vt ka lõik 4.5.
Kuigi paljudel
Järgnevate seisundite ilmnemisest või ägenemisest on teatatud nii raseduse kui ka
Päriliku angioödeemiga naistel võivad eksogeensed östrogeenid esile kutsuda või ägestada angioödeemi sümptomeid.
Ägedate või krooniliste maksafunktsiooni häirete puhul võib ilmneda vajadus
Kuigi
See ravim sisaldab 44 mg laktoosi ühes tabletis. Patsiendid, kellel on harvaesinev pärilik galaktoositalumatus, laktaasi puudulikkus või
Meditsiiniline läbivaatus/nõustamine
Enne Cleodette kasutamise alustamist või taasalustamist tuleb võtta täielik meditsiiniline anamnees (sh perekonna anamnees) ja välistada rasedus. Vastunäidustustest (vt lõik 4.3) ja hoiatustest (vt lõik 4.4) lähtuvalt tuleb mõõta vererõhku ning teostada füüsiline läbivaatus. Oluline on juhtida naise tähelepanu venoosse ja arteriaalse tromboosiga seotud teabele, sh Cleodette riskile võrreldes teiste
Naisi tuleb teavitada pakendi infolehe hoolika läbilugemise ja selles esitatud nõuannete järgimise vajadusest. Läbivaatuste sagedus ja iseloom peavad põhinema kehtivatel ravijuhistel ning need tuleb kohandada igale naisele individuaalselt.
Naisi tuleb teavitada sellest, et suukaudsed rasestumisvastased vahendid ei kaitse
Efektiivsuse vähenemine
Vähenenud tsükli kontroll
Kõikide
Kui veritsused jäävad ebakorrapärasteks või muutuvad ebakorrapärasteks pärast eelnevalt korrapäraseid tsükleid, tuleb arvestada mittehormonaalseid põhjuseid ja rakendada kohaseid diagnostilisi meetmeid halvaloomulise seisundi või raseduse välistamiseks. Kõne alla tuleb ka emakaõõne puhastus.
Mõnel naisel ei pruugi tabletivaba intervalli ajal menstruatsioonilaadset vereeritust esineda. Juhul kui naine on võtnud
4.5Koostoimed teiste ravimitega ja muud koostoimed
Märkus: Võimalike koostoimete tuvastamiseks tuleb tutvuda samaaegselt manustatavate ravimite omaduste kokkuvõtetega.
-Teiste ravimite toimed Cleodette’le
Koostoimed võivad ilmneda ravimitega, mis indutseerivad maksaensüüme ning mille tulemusena võib kiireneda suguhormoonide kliirens, mis võib omakorda põhjustada nn läbimurdeveritsust ning/või rasestumisvastase toime ebaõnnestumist.
Kuidas toimida
Ensüümide induktsioon on märgatav juba mõnepäevase ravi järel. Maksimaalne ensüümide induktsioon ilmneb tavaliselt mõne nädala jooksul. Pärast ravikuuri lõppu võib ensüümide induktsioon püsida kuni 4 nädalat.
Lühiajaline ravi
Naised, kes võtavad samaaegselt ensüüme indutseerivaid ravimeid, peavad lisaks KSK’le kasutama ajutiselt barjäärimeetodit või mõnda muud rasestumisvastast meetodit. Barjäärimeetodit tuleb kasutada ravimite koosmanustamise vältel ning 28 päeva pärast ravi lõpetamist.
Kui ravimi võtmise aeg jätkub ka pärast toimeaineid sisaldavate tablettide lõppemist KSK pakendist, tuleb platseebotabletid hävitada ja kohe alustada uue KSK pakendiga.
Pikaajaline ravi
Kui naine saab pikaajalist ravi maksaensüüme indutseerivate toimeainetega, on soovitatav kasutada mõnda teist usaldusväärset, mittehormonaalset kontratseptsiooni meetodit.
Kirjanduses on kirjeldatud alljärgnevaid koostoimeid.
KSK’de kliirensit suurendavad ained (ensüümide induktsiooni tagajärjel väheneb KSK’de efektiivsus), nt:
barbituraadid, bosentaan, karbamasepiin, fenütoiin, primidoon, rifampitsiin ja
Ained, millel on erinevad toimed KSK’de kliirensile
KSK’dega koosmanustamisel võivad mitmed
Seetõttu tuleb võimalike koostoimete ja kaasuvate soovituste väljaselgitamiseks lugeda samaaegselt manustatavate
Drospirenooni peamised metaboliidid inimese vereseerumis moodustuvad ilma tsütokroom P450 süsteemi osaluseta. Seetõttu on ebatõenäoline, et selle ensüümsüsteemi inhibiitorid võiksid mõjutada drospirenooni metabolismi.
-Cleodette toimed teistele ravimitele
Suukaudsed rasestumisvastased ravimid võivad mõjutada teatud teiste toimeainete metabolismi. Kontsentratsioonid plasmas ja kudedes võivad vastavalt kas suureneda (nt tsüklosporiin) või väheneda (nt lamotrigiin).
Tuginedes in vitro inhibitsiooniuuringutele ja in vivo koostoimete uuringutele vabatahtlike naispatsientidega, kes kasutasid markersubstraatidena omeprasooli, simvastatiini ja midasolaami, ei ole tõenäoline, et drospirenoon annuses 3 mg mõjutaks teiste toimeainete metabolismi.
Farmakodünaamilised koostoimed
Samaaegne kasutamine koos ombitasviiri/ paritapreviiri/ ritonaviiri ja dasabuviiri sisaldavate ravimitega koos ribaviriiniga või ilma, võib suurendada transaminaaside (ALAT) aktiivsuse suurenemise riski (vt lõigud 4.3 ja 4.4). Seetõttu peavad Cleodette kasutajad enne nimetatud kombinatsioonravi alustamist üle minema alternatiivsele kontratseptsiooni meetodile (nt ainult progesterooni sisaldav kontratseptiiv või mittehormonaalne vahend). Cleodette kasutamist võib uuesti alustada 2 nädalat pärast nimetatud kombinatsioonravi lõpetamist.
-Muud koostoimed
Neerupuudulikkuseta patsientidel ei ilmnenud drospirenooni ja
-Laboratoorsed analüüsid
Rasestumisvastaste steroidide kasutamine võib mõjutada teatud laboratoorsete analüüside tulemusi, sh
4.6Fertiilsus, rasedus ja imetamine
Rasedus
Cleodette ei ole näidustatud raseduse ajal.
Kui naine rasestub Cleodette kasutamise ajal, tuleb ravimi manustamine viivitamatult lõpetada. Ulatuslikud epidemioloogilised uuringud ei ole näidanud sünnidefektide riski suurenemist lastel, kelle emad kasutasid
Loomkatsetes on näidatud tiinuse ja imetamise ajal esinenud kõrvaltoimeid (vt lõik 5.3). Nendest loomkatsetest saadud andmete põhjal ei saa välistada toimeainete hormonaalsest aktiivsusest põhjustatud kõrvaltoimete olemasolu. Siiski, üldine kogemus
Saadaolevad andmed Cleodette kasutamise kohta raseduse ajal on liiga piiratud ega võimalda seetõttu teha järeldusi Cleodette kahjulike mõjude kohta rasedusele, loote või vastsündinu tervisele. Praeguseks ei ole asjakohased epidemioloogilised andmed saadaval.
Sünnitusjärgsel perioodil tuleb arvesse võtta suurenenud VTE riski, kui taasalustatakse Cleodette kasutamist (vt lõigud 4.2 ja 4.4).
Imetamine
4.7Toime reaktsioonikiirusele
Uuringuid ravimi toime kohta autojuhtimise ja masinate käsitsemise võimele ei ole läbi viidud. KSK- de kasutajatel ei ole täheldatud toimet autojuhtimise ja masinate käsitsemise võimele.
4.8Kõrvaltoimed
Seoses Cleodette kasutamisega on teatatud järgnevatest kõrvaltoimetest.
Alljärgnevas tabelis on kõrvaltoimed esitatud MedDRA organsüsteemi klasside järgi. Esinemissagedused põhinevad kliiniliste uuringute andmetel.
Väga sage (≥1/10)
Sage (≥1/100 kuni <1/10)
Harv (≥1/10000 kuni <1/1000)
Väga harv (<1/10000)
Teadmata (ei saa hinnata olemasolevate andmete alusel)
Organsüsteemi klass |
Kõrvaltoimete esinemissagedus |
|||
|
Sage |
Harv |
||
|
≥1/100 kuni <1/10 |
≥1/1000 kuni <1/100 |
≥10000 kuni <1/1000 |
|
Infektsioonid ja |
|
Kandidiaas |
|
|
infestatsioonid |
|
Herpes simplex |
|
|
Immuunsüsteemi |
|
Allergilised reaktsioonid |
Astma |
|
häired |
|
|
|
|
Ainevahetus- ja |
|
Söögiisu suurenemine |
|
|
toitumishäired |
|
|
|
|
Psühhiaatrilised häired |
Emotsionaalne |
Depressioon |
|
|
|
labiilsus |
Närvilisus |
|
|
|
|
Unehäired |
|
|
Närvisüsteemi häired |
Peavalu |
Paresteesia |
|
|
|
|
Vertiigo |
|
|
Kõrva ja labürindi |
|
|
Kuulmise langus |
|
kahjustused |
|
|
|
|
Silma kahjustused |
|
Nägemishäired |
|
|
Südame häired |
|
Ekstrasüstoolia |
|
|
|
|
Tahhükardia |
|
|
Vaskulaarsed häired |
|
Hüpertensioon |
Venoosne |
|
|
|
Hüpotensioon |
trombemboolia |
|
|
|
Migreen |
Arteriaalne |
|
|
|
Veenilaiendid |
trombemboolia |
|
Respiratoorsed, |
|
Farüngiit |
|
|
rindkere ja |
|
|
|
|
mediastiinumi häired |
|
|
|
|
Seedetrakti häired |
Kõhuvalu |
Iiveldus |
|
|
|
|
Oksendamine |
|
|
|
|
Gastroenteriit |
|
|
|
|
Kõhulahtisus |
|
|
|
|
Kõhukinnisus |
|
|
|
|
Seedetrakti häired |
|
|
Naha ja nahaaluskoe |
Akne |
Angioödeem |
Nodoosne erüteem |
|
kahjustused |
|
Alopeetsia |
Multiformne erüteem |
|
|
|
Ekseem |
|
|
|
|
Kihelus |
|
|
|
|
Lööve |
|
|
|
|
Naha kuivus |
|
|
|
|
Seborröa |
|
|
|
|
Naha häired |
|
|
|
Kaelavalu |
|
|
|
kahjustused |
|
Valu jäsemetes |
|
|
|
|
Lihaskrambid |
|
|
Neerude ja kuseteede |
|
Tsüstiit |
|
|
häired |
|
|
|
|
Reproduktiivse |
Rindade valulikkus |
Rinnanäärme kasvaja |
|
|
süsteemi ja |
Rindade suurenemine |
Fibrotsüstiline |
|
|
rinnanäärme häired |
Rindade hellus |
rinnanääre |
|
|
|
Düsmenorröa |
Galaktorröa |
|
|
|
Metrorraagia |
Munasarjatsüst |
|
|
|
Kuumahood |
|
|
|
Menstruatsiooni häired |
|
|
|
Amenorröa |
|
|
|
Menorraagia |
|
|
|
Vaginaalne kandidiaas |
|
|
|
Vaginiit |
|
|
|
Voolus suguteedest |
|
|
|
Vulvovaginaalne häire |
|
|
|
Tupe kuivus |
|
|
|
Vaagnavalu |
|
|
|
Kahtlane Papanicolaou |
|
|
|
testi tulemus |
|
|
|
Libiido langus |
|
Üldised häired ja |
|
Turse |
|
manustamiskoha |
|
Asteenia |
|
reaktsioonid |
|
Valu |
|
|
|
Liigne janu |
|
|
|
Suurenenud higistamine |
|
Uuringud |
Kehakaalu tõus |
Kehakaalu langus |
|
Kasutatud on kõige sobivamat MedDRA terminit konkreetse kõrvaltoime, selle sünonüümide ja seotud seisundite kirjeldamiseks.
Valitud kõrvaltoimete kirjeldus
−Suurem risk arteriaalsete ning venoossete trombootiliste ja trombembooliliste seisundite, sh müokardiinfarkti, insuldi, mööduva isheemilise ataki, venoosse tromboosi ja kopsuemboolia tekkeks. Neid seisundeid on põhjalikumalt kirjeldatud lõigus 4.4.
−Hüpertoonia.
−Maksakasvajad.
−Haigusseisundite ilmnemine või süvenemine, mille korral seost
−Kloasmid.
−Maksafunktsiooni ägedate või krooniliste häirete ilmnemisel võib olla vajalik
−Päriliku angioödeemiga naistel võivad eksogeensed östrogeenid esile kutsuda või ägestada angioödeemi sümptomeid.
Suukaudsete rasestumisvastaste ravimite kasutajate seas diagnoositakse rinnavähki veidi sagedamini. Kuivõrd rinnavähki esineb alla
Koostoimed
Suukaudsete kontratseptiivide ja teiste ravimite (ensüümide indutseerijad) koostoimete tulemusena võib tekkida tsüklivälist verejooksu ja/või kontratseptsiooni ebaõnnestumist (vt lõik 4.5).
Võimalikest kõrvaltoimetest teavitamine
Ravimi võimalikest kõrvaltoimetest on oluline teavitada ka pärast ravimi müügiloa väljastamist. See võimaldab jätkuvalt hinnata ravimi kasu/riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest www.ravimiamet.ee kaudu.
4.9Üleannustamine
Praeguseks puuduvad teated Cleodette üleannustamise kohta. Kombineeritud suukaudsete kontratseptiivide kasutamisel saadud üldiste kogemuste alusel võivad tablettide üleannustamisel tekkida järgmised sümptomid: iiveldus, oksendamine ja noortel tüdrukutel vähene tupekaudne verejooks. Antidoodid puuduvad, edasine ravi on sümptomaatiline.
5.FARMAKOLOOGILISED OMADUSED
5.1Farmakodünaamilised omadused
Farmakoterapeutiline rühm: hormonaalsed kontratseptiivid süsteemseks kasutamiseks, gestageenide ja östrogeenide fikseeritud kombinatsioonid;
Meetodi ebaõnnestumise Pearli indeks: 0,11 (ülemine kahepoolne 95% usalduspiir: 0,60). Üldine Pearli indeks (meetodi viga + patsiendi viga): 0,31 (ülemine kahepoolne 95 % usalduspiir: 0,91).
Cleodette rasestumisvastane toime põhineb erinevate tegurite koostoimel, millest tähtsaimateks on ovulatsiooni pärssimine ja emaka limaskesta muutused.
Cleodette on kombineeritud suukaudne rasestumisvastane ravim, mis sisaldab etünüülöstradiooli ja drospirenooni (progestageen). Terapeutilistes annustes on drospirenoonil ka antiandrogeensed ja kerged antimineralokortikoidsed omadused. Drospirenoonil puudub östrogeenne, glükokortikoidne ja antiglükokortikoidne toime. Sellest tulenevalt sarnaneb drospirenooni farmakoloogiline profiil suuresti loodusliku progesterooni omaga.
Kliiniliste uuringute tulemused viitavad, et Cleodette kerged antimineralokortikoidsed omadused põhjustavad kergeid antimineralokortikoidseid toimeid.
5.2 Farmakokineetilised omadused
Drospirenoon
Imendumine
Suukaudsel manustamisel imendub drospirenoon kiirelt ja peaaegu täielikult. Toimeaine maksimaalsed kontsentratsioonid seerumis (ligikaudu 38 ng/ml) saavutatakse preparaadi ühekordse manustamise järel ligikaudu 1...2 tunniga. Biosaadavus on vahemikus 76...85%. Toidu samaaegne manustamine drospirenooni biosaadavust ei mõjuta.
Jaotumine
Suukaudse manustamise järgselt langevad drospirenooni tasemed seerumis lõpliku poolestusajaga 31 tundi. Drospirenoon seotakse seerumi albumiiniga ja see ei seondu suguhormooni siduva globuliini (SHBG, sex hormone binding globulin) ega kortikoidi siduva globuliiniga (CBG, corticoid binding globulin). Vaid 3...5% kogu toimeaine seerumi kontsentratsioonist esineb vaba steroidina. Etünüülöstradiooli poolt põhjustatud SHBG tõus ei mõjuta drospirenooni seondumist seerumi valguga. Drospirenooni keskmine näiline jaotusruumala on 3,7 ± 1,2 l/kg.
Biotransformatsioon
Suukaudse manustamise järel metaboliseerub drospirenoon ulatuslikult. Põhilised metaboliidid plasmas on drospirenooni happelised vormid, mis tekivad laktoonringi avanemisel, ja
Eritumine
Drospirenooni metaboolne kliirens seerumis on 1,5 ± 0,2 ml/min/kg. Drospirenoon eritub muutumatul kujul vaid tühistes kogustes. Drospirenooni metaboliidid erituvad rooja ja uriiniga vahekorras ligikaudu 1:2 kuni 1:4. Uriini ja roojaga erituvate metaboliitide poolväärtusaeg on ligikaudu 40 tundi.
Tasakaalukontsentratsioon
Ravitsükli ajal saavutatakse drospirenooni maksimaalsed tasakaalukontsentratsioonid seerumis ligikaudu 70 ng/ml, mis saavutatakse ligikaudu
Patsientide erirühmad
Neerufunktsiooni häire mõju
Kerge neerukahjustusega naistel (kreatiniini kliirens CLcr 50...80 ml/min) olid drospirenooni püsikontsentratsioonid seerumis võrreldavad normaalse neerufunktsiooniga naiste omadega. Mõõduka neerukahjustusega naistel (CLcr 30...50 ml/min) olid drospirenooni kontsentratsioonid seerumis normaalse neerufunktsiooniga naiste omadega võrreldes keskmiselt 37% võrra kõrgemad. Samuti oli drospirenoonravi kerge ja mõõduka neerukahjustusega naistele hästi talutav. Drospirenoonravi ei avaldanud seerumi kaaliumi kontsentratsioonile kliiniliselt olulist mõju.
Maksafunktsiooni häire mõju
Normaalse maksafunktsiooniga isikutega võrreldes vähenes üksikannusega uuringus osalevate mõõduka maksakahjustusega vabatahtlikel kliirens suukaudsel manustamisel (CL/F) ligikaudu 50% võrra. Mõõduka maksakahjustusega vabatahtlikel täheldatud drospirenooni kliirensi langus ei põhjustanud nähtavaid erinevusi seerumi kaaliumikontsentratsioonides. Isegi diabeedi ja samaaegse spironolaktoonravi korral (need kaks tegurit võivad soodustada hüperkaleemia teket) ei täheldatud seerumi kaaliumikontsentratsioonide tõusu üle normaalse vahemiku ülempiiri. Sellest võib järeldada, et kerge ja mõõduka maksakahjustusega
Etnilised rühmad
Kliiniliselt olulisi erinevusi drospirenooni või etünüülöstradiooli farmakokineetikas Jaapani ja heledanahaliste naiste vahel ei ole täheldatud.
Etünüülöstradiool
Imendumine
Suukaudsel manustamisel imendub etünüülöstradiool kiirelt ja täielikult. Pärast ühekordset suukaudset manustamist saavutatakse maksimaalne kontsentratsioon seerumis (ligikaudu 33 pikogrammi/ml) 1...2 tunniga. Presüsteemse konjugatsiooni ja esmase maksapassaaži tulemusena on absoluutne biosaadavus ligikaudu 60%. Koos toiduga manustamisel vähenes etünüülöstradiooli biosaadavus ligikaudu 25% uuringus osalejatest, samas kui ülejäänutel vastavaid muutusi ei täheldatud.
Jaotumine
Seerumi etünüülöstradiooli tase väheneb kahefaasiliselt, lõplikku dispositsioonifaasi iseloomustab ligikaudu
Biotransformatsioon
Etünüülöstradiooli presüsteemne konjugatsioon leiab aset nii peensoole limaskestas kui ka maksas. Etünüülöstradiooli esmane metabolism toimub aromaatse hüdroksüülimise kaudu, kuid moodustub ka mitmesuguseid hüdroksüülitud ja metüülitud metaboliite, mis esinevad nii vabade metaboliitide kui ka glükuroniidide ning sulfaatide konjugaatidena. Etünüülöstradiooli metaboolne kliirens on ligikaudu 5 ml/min/kg.
Eritumine
Etünüülöstradiool ei eritu olulisel määral muutumatul kujul. Etünüülöstradiooli metaboliidid erituvad uriini ja sapiga vahekorras 4:6. Metaboliitide eritumise poolväärtusaeg on ligikaudu 1 päev.
Tasakaalukontsentratsioon
Püsiv ravimi plasmakontsentratsioon saavutatakse ravitsükli teises pooles ning etünüülöstradiooli seerumitase tõuseb ligikaudu 2,0...2,3 korda.
5.3Prekliinilised ohutusandmed
Laboriloomadel piirdusid drospirenooni ja etünüülöstradiooli toimed teadaolevate farmakoloogiliste toimetega. Eelkõige näitasid reproduktiivtoksilisuse uuringud loomadel embrüotoksilist ja lootetoksilist toimet. Neid toimeid peetakse liigispetsiifiliseks. Annustel, mis ületasid Cleodette 0,02 mg/3 mg kasutajate annuseid, kirjeldati toimet seksuaalsele diferentseerumisele roti lootel, kuid mitte ahvi lootel.
6.FARMATSEUTILISED ANDMED
6.1Abiainete loetelu
Tableti sisu:
Laktoosmonohüdraat
Eelželatiniseeritud (maisi)tärklis
Povidoon
Naatriumkroskarmelloos
Polüsorbaat 80
Magneesiumstearaat (E572)
Tableti kate:
Osaliselt hüdrolüüsitud polüvinüülalkohol
Titaandioksiid (E 171)
Makrogool 3350
Talk (E 553b)
Kollane raudoksiid (E 172)
Punane raudoksiid (E 172)
Must raudoksiid (E 172)
6.2Sobimatus
Ei kohaldata.
6.3Kõlblikkusaeg
3 aastat.
6.4Säilitamise eritingimused
See ravimpreparaat ei vaja säilitamisel eritingimusi.
6.5Pakendi iseloomustus ja sisu
Alumiiniumist
Pakendi suurused:
1 x 21 õhukese polümeerikattega tabletti.
2 x 21 õhukese polümeerikattega tabletti.
3 x 21 õhukese polümeerikattega tabletti.
6 x 21 õhukese polümeerikattega tabletti.
13 x 21 õhukese polümeerikattega tabletti.
Kõik pakendi suurused ei pruugi olla müügil.
6.6Erihoiatused ravimpreparaadi hävitamiseks ja käsitlemiseks
Kasutamata ravimpreparaat või jäätmematerjal tuleb hävitada vastavalt kohalikele nõuetele.
7.MÜÜGILOA HOIDJA
Actavis Group PTC ehf
Reykjavíkurvegi
Island
8.MÜÜGILOA NUMBER
9.ESMASE MÜÜGILOA VÄLJASTAMISE/MÜÜGILOA UUENDAMISE KUUPÄEV
Müügiloa esmase väljastamise kuupäev: 28.02.2014
10.TEKSTI LÄBIVAATAMISE KUUPÄEV
November 2017
