Strattera - suukaudne lahus (4mg 1ml)
Artikli sisukord
suukaudne lahus (4mg 1ml)
Pakendi infoleht: teave kasutajale
Strattera, 4 mg/ml suukaudne lahus
Atomoksetiin
Olulised asjad, mida te peate oma ravimi kohta teadma.
Seda ravimit kasutatakse ADHD raviks
•ADHD täielik nimi on aktiivsus- ja tähelepanuhäire.
•Ravim parandab teie ajutegevust. See võib aidata parandada teie tähelepanu, keskendumist ja vähendada impulsiivsust.
•Lisaks sellele ravimile vajate te ADHD raviks ka muud abi.
Lisainformatsiooniks lugege lõiku 1.
Rääkige enne selle ravimit võtmist oma arstiga:
•kui teil on probleeme vaimse tervisega,
•kui teil on probleeme südamega või vereringehäireid,
•kui teil on tõsiseid probleeme ajuveresoontega, nt insult.
Lisainformatsiooniks lugege lõiku 2.
Selle ravimi võtmise ajal:
•Külastage korrapäraselt oma arsti. See on sellepärast, et teie arst soovib kontrollida, kuidas ravim teile toimib.
•Ärge lõpetage ravimi võtmist ilma oma arstiga seda eelnevalt arutamata.
•Kui te olete ravimit juba rohkem kui aasta võtnud, võib teie arst teil paluda ravimi võtmise peatada, et näha, kas seda veel vaja on.
•Kõige sagedamini esinevad kõrvaltoimed lastel ja noorukitel on:
peavalu, kõhuvalu, näljatunde puudumine, iiveldus või oksendamine, unisus, vererõhu tõus, südame löögisageduse (pulsi) sagenemine.
•Kõige sagedamini esinevad kõrvaltoimed täiskasvanutel on:
iiveldus, suukuivus, peavalu, näljatunde puudumine, unetus, vererõhu tõus, südame löögisageduse (pulsi) sagenemine.
Lisainformatsiooniks lugege lõike 3 ja 4.
Rääkige koheselt oma arstile, kui teil juhtub midagi järgnevast:
•tekivad muutused meeleolus ja tunnetes,
•tunnete mingeid probleeme südamega, nt kiire või ebakorrapärane südamerütm.
Lisainformatsiooniks lugege lõike 2 ja 4.
Infolehe ülejäänud osa sisaldab rohkem üksikasju ja muud olulist informatsiooni selle ravimi ohutuse ja efektiivsuse kohta.
Enne ravimi võtmist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet.
•Hoidke infoleht alles, et seda vajadusel uuesti lugeda.
•Kui teil on lisaküsimusi, pidage nõu oma arsti või apteekriga.
•Ravim on välja kirjutatud üksnes teile. Ärge andke seda kellelegi teisele. Ravim võib olla neile kahjulik, isegi kui haigusnähud on sarnased.
•Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga. Kõrvaltoime võib olla ka selline, mida selles infolehes ei ole nimetatud. Vt lõik 4.
Infoleht koosneb lõikudest:
Lõigud 1...6 on mõeldud vanematele ja hooldajatele (mõnikord nimetatakse „teie eestkostja“). Viimane lõik on erilõik lugemiseks lastele või noorukitele.
Siiski on kõik lõigud kirjutatud selliselt nagu loeksid neid ravimit võtvad lapsed või noorukid.
Infolehe sisukord
1.Mis ravim on Strattera ja milleks seda kasutatakse
2.Mida on vaja teada enne Strattera võtmist
3.Kuidas Strattera’t võtta
4.Võimalikud kõrvaltoimed
5.Kuidas Strattera’t säilitada
6.Pakendi sisu ja muu teave
1.Mis ravim on Strattera ja milleks seda kasutatakse
Milleks seda kasutatakse
Strattera sisaldab atomoksetiini ja seda kasutatakse aktiivsus- ja tähelepanuhäire (ADHD) raviks. Seda kasutatakse:
-üle 6 aasta vanustel lastel
-noorukitel
-täiskasvanutel.
Seda kasutatakse ainult osana haiguse täisravist, mis nõuab ka raviviise, mis ei sisalda ravimeid, nt nõustamine ja käitumisravi.
Ravimit ei kasutata ADHD raviks alla
Täiskasvanutel kasutatakse Strattera’t ADHD raviks kui sümptomid on äärmiselt murettekitavad ja häirivad teie tööd ja ühiskondlikku elu ning kui teil on esinenud haiguse sümptomeid juba lapsena.
Kuidas see toimib
Strattera suurendab noradrenaliini taset ajus. Noradrenaliin on aine, mida toodab inimorganism ning suurendab
Pärast selle ravimi kasutamise algust võib mööduda mitu nädalat, enne kui teie sümptomid täielikult paranevad.
ADHD kohta
ADHD’ga lapsed ja noorukid kogevad:
•raskusi paigalistumisega ja
•raskusi keskendumisel.
See, et nad ei suuda selliseid asju teha, ei ole nende süü. Paljud lapsed ja noorukid näevad vaeva, et teha neid asju. ADHD’ga võib siiski igapäevaelus muresid tekkida. ADHD’ga lastel ja noorukitel võib olla raskusi õppimise ja kodutööde tegemisega. Nad avastavad, et neil on kodus, koolis ja mujal raske hästi käituda. ADHD ei mõjuta lapse või nooruki intelligentsust.
ADHD’ga täiskasvanud kogevad raskusi kõigi nende asjade tegemisel, mis lapsedki, kuigi see võib tähendada, et neil on muresid:
•tööga
•suhetega
•madala enesehinnanguga
•hariduse omandamisega.
2. Mida on vaja teada enne Strattera võtmist
ÄRGE kasutage Strattera’t:
-kui olete atomoksetiini või selle ravimi mis tahes koostisosade (loetletud lõigus 6) suhtes allergiline;
-kui te olete viimase kahe nädala jooksul kasutanud ravimit, mis kuulub monoaminooksüdaasi inhibiitorite (MAOI) rühma, nt fenelsiini.
-kui te põete silmahaigust, mida nimetatakse suletudnurga glaukoomiks (suurenenud rõhk silmas);
-kui teil on tõsiseid probleeme südamega, mis võib väljenduda kiiremas pulsisageduses ja/või kõrgenenud vererõhus, sest see võib olla tingitud Strattera’st;
-kui teil on tõsiseid probleeme ajuveresoontega – nagu nt ajuinsult, veresoone osa turse ja nõrgenemine (aneurüsm) või kitsad või ummistunud veresooned;
-kui teil on neerupealise kasvaja (feokromotsütoom).
Ärge võtke Strattera’t kui midagi ülalmainitust teie puhul kehtib. Kui te ei ole kindel, rääkige enne Strattera võtmist oma arsti või apteekriga. See on sellepärast, et Strattera võib neid probleeme süvendada.
Hoiatused ja ettevaatusabinõud
Nii lapsed kui täiskasvanud peavad olema teadlikud järgnevatest hoiatustest ja ettevaatusabinõudest. Rääkige enne Strattera võtmist oma arsti või apteekriga, kui teil esineb:
-mõtteid enese tapmisest või enesetapukatseid.
-probleeme südamega (sh südamerikked) või kiirenenud südamerütm. Strattera võib suurendada südame löögisagedust (pulss). Südamerikkega patsientide puhul on teatatud äkksurmast.
-kõrge vererõhk. Strattera võib tõsta vererõhku.
-madal vererõhk. Madala vererõhuga inimestel võib Strattera põhjustada pearinglust või minestamist.
-probleeme vererõhu või südame löögisageduse kiire muutusega.
-
-maksaprobleeme. Te võite vajada väiksemat annust.
-psühhootilisi sümptomeid, sh hallutsinatsioonid (olematute asjade kuulmine või nägemine), mittetõeste asjade uskumine või umbusklikkus.
-mania (kõrgendatud või ülev meeleolu, mis põhjustab ebatavalist käitumist) ja ärevus.
-agressiivsust.
-ebasõbralikke ja vihaseid (vaenulikke) tundeid.
-haigusloos epilepsiat või on esinenud krampe mingil muul põhjusel. Strattera võib põhjustada krampide esinemissageduse suurenemist.
-tavapärasest erinevaid tujusid (tujukõikumised) või väga õnnetut enesetunnet.
-raskesti kontrollitavaid korduvaid tõmblusi suvalistes kehaosades või te kordate helisid ja sõnu.
Öelge oma arstile või apteekrile enne ravi alustamist, kui midagi ülalmainitust kehtib teie puhul. See on sellepärast, et Strattera võib neid probleeme süvendada. Teie arst soovib jälgida, kuidas ravim teid mõjutab.
Uuringud, mida teie arst teeb, enne kui te hakkate Strattera’t võtma
Need uuringud on abiks otsustamisel, kas Strattera on teile õige ravim.
Teie arst mõõdab teie
-vererõhku ja südamerütmi (pulss) enne Strattera võtmist ja selle ajal
-pikkust ja kehakaalu Strattera võtmise ajal, kui te olete laps või nooruk.
Teie arst räägib teiega:
-teistest ravimitest, mida te võtate
-kas teil on perekonna haigusloos esinenud seletamatuid surmajuhtumeid
-teistest meditsiinilistest probleemidest (nt südameprobleemid), mis teil või teie peres esineda võivad.
On oluline, et te annaksite arstile nii palju informatsiooni kui te saate. See aitab teie arstil otsustada, kas Strattera on teile õige ravim. Teie arst võib otsustada, et enne kui te seda ravimit võtma hakkate, on vajalikud veel teised meditsiinilised uuringud.
Muud ravimid ja Strattera
Teatage oma arstile või apteekrile, kui te võtate, olete hiljuti võtnud või kavatsete võtta mis tahes muid ravimeid. Siia kuuluvad ka retseptita ostetavad ravimid. Teie arst otsustab, kas te tohite Strattera’t koos oma teiste ravimitega võtta ja mõningatel juhtudel võib arst teie annust kohandada või suurendada annust palju aeglasemalt.
Ärge võtke Strattera`t koos ravimitega, mida nimetatakse
Kui te võtate teisi ravimeid, võib Strattera mõjutada nende toimimist või põhjustada kõrvaltoimeid. Kui te võtate mõnda järgnevatest ravimitest, küsige enne Strattera võtmist nõu oma arstilt või apteekrilt:
-ravimid, mis tõstavad vererõhku või mida kasutatakse vererõhu kontrolli all hoidmiseks.
-ravimid, nagu depressioonivastased ravimid, näiteks imipramiin, venlafaksiin, mirtasapiin, fluoksetiin ja paroksetiin.
-mõningad köha ja külmetuse ravimid, mis sisaldavad aineid, mis võivad mõjutada vererõhku. On oluline, et te peaksite enne mõne sellise preparaadi võtmist nõu oma apteekriga.
-mõned ravimid, millega ravitakse vaimse tervise häireid.
-ravimid, mis teadaolevalt suurendavad krambiriski.
-mõned ravimid, mis põhjustavad Strattera püsimise organismis tavalisest pikemat aega (nt kinidiin ja terbinafiin).
-salbutamool (astmaravim), kui seda manustatakse suukaudu või süstina, võite te tunda südametöö kiirenemist, aga see ei tee teie astmat halvemaks.
Allpool loetletud ravimid võivad koos Strattera’ga võetult põhjustada südame rütmihäirete riski suurenemist:
-ravimid, mida kasutatakse südamerütmi kontrollimiseks.
-ravimid, mis muudavad soolade sisaldust veres.
-ravimid malaaria ärahoidmiseks ja raviks.
-mõned antibiootikumid (nagu nt erütromütsiin ja moksifloksatsiin).
Kui te ei ole kindel, kas mõni ravim, mida te võtate kuulub ülaltoodud loetellu, küsige enne Strattera võtmist nõu oma arstilt või apteekrilt.
Rasedus ja imetamine
Ei ole teada, kas see ravim võib mõjutada teie sündimata last või erituda rinnapiima.
-Seda ravimit ei tohi raseduse ajal kasutada, välja arvatud juhul kui teie arst seda soovitab.
-Te peate hoiduma selle ravimi võtmisest imetamise ajal või katkestama imetamise.
Kui te:
•olete rase või imetate,
•kahtlustate endal rasedust või planeerite rasestuda,
•kavatsete last rinnaga toita
pidage enne selle ravimi võtmist nõu oma arsti või apteekriga.
Autojuhtimine ja masinatega töötamine
Pärast Strattera võtmist võite tunda väsimust, unisust või pearinglust. Seni kuni te ei tea, kuidas Strattera teile toimib, peate olema autojuhtimisel või masinate käsitsemisel ettevaatlik. Kui te tunnete ennast väsinuna, unisena või esineb pearinglust, ei tohi te autot juhtida ega käsitseda masinaid.
Oluline informatsioon suukaudse lahuse kohta
Sellel suukaudsel lahusel on silma ärritav toime. Kui suukaudne lahus satub silma, tuleb kahjustatud silma otsekohe loputada veega ning küsida meditsiinilist nõuannet. Käsi ja mis tahes muid kehaosi, mis võisid suukaudse lahusega kokku puutuda, tuleb samuti esimesel võimalusel pesta.
Strattera suukaudne lahus sisaldab sorbitooli. Kui arst on teile öelnud, et te ei talu teatud suhkruid, peate te enne selle ravimi kasutamist konsulteerima oma arstiga.
3.Kuidas Strattera’t võtta
-Võtke seda ravimit alati täpselt nii, nagu arst või apteeker on teile selgitanud. Kui te ei ole milleski kindel, pidage nõu oma arsti või apteekriga. Soovitatav annus on üks või kaks korda ööpäevas (hommikul ja hilisel pärastlõunal või varajasel õhtul).
-Lapsed ei tohi seda ravimit võtta ilma täiskasvanu abita.
-Kui te võtate Strattera`t üks kord ööpäevas ning kogete unisust või iiveldust, võib teie arst muuta teie ravimi võtmise aega kuni kahe korrani ööpäevas.
-Ravimit võib võtta koos toiduga või ilma.
-Suukaudset lahust ei tohi segada toiduga või veega, sest siis võib väheneda saadava ravimi kogus või maitse võib olla ebameeldiv.
-Ravimi võtmist on kergem meeles pidada, kui võtate ravimit alati samal kellaajal.
Strattera suukaudset lahust turustatakse pudelis. See on üks pakendi osa, veel kuulub pakendisse annustamise seade, mis koosneb 10 ml suusüstlast, mis on gradueeritud 1 ml kaupa ja pudeli kaelale surutavast adapterist. Kasutamisjuhiseid lugege kaasas olevast voldikust, mis on karbis koos adapteri ja süstla kasutamisjuhisega.
Kui palju võtta
Kui te olete laps
Teie arst räägib teile, kui palju Strattera`t te peate võtma ning arvutab selle teie kehakaalu arvestades välja. Tavaliselt käsib arst teil alustada väiksema annusega enne teile vajaliku Strattera annuse suurendamist vastavalt teie kehakaalule.
-Kehakaaluga kuni 70 kg: alustatakse päevase koguannusega 0,5 mg/kg kehakaalu kohta minimaalselt 7 päeva jooksul. Seejärel võib teie arst otsustada annust suurendada tavalise säilitusannuseni, mis on ligikaudu 1,2 mg/kg kehakaalu kohta ööpäevas.
-Kehakaaluga üle 70 kg: alustatakse päevase koguannusega 40 mg minimaalselt 7 päeva jooksul. Seejärel võib teie arst otsustada annust suurendada tavalise säilitusannuseni, mis on 80 mg ööpäevas. Maksimaalne ööpäevane annus, mis teie arst võib määrata, on 100 mg.
Täiskasvanud
-Strattera’t tuleb alustada päevase koguannusega 40 mg minimaalselt 7 päeva jooksul. Seejärel võib teie arst otsustada annust suurendada tavalise säilitusannuseni, mis on 80...100 mg ööpäevas. Maksimaalne ööpäevane annus, mis teie arst võib määrata, on 100 mg.
Kui teil esineb probleeme maksaga, võib arst määrata teile väiksema annuse.
Kui te võtate Strattera’t rohkem kui ette nähtud
Võtke otsekohe ühendust oma arstiga või minge lähima haigla vastuvõtuosakonda ning rääkige kui palju ravimit te võtsite. Kõige sagedamini teatatud kõrvaltoimeteks seoses üleannustamistega on seedetrakti nähud, unisus, pearinglus, värinad, ja ebanormaalne käitumine.
Kui te unustate Strattera’t võtta
Kui te jätsite annuse vahele, siis tuleb see võtta niipea kui võimalik, kuid 24 tunni jooksul ei tohi manustada rohkem kui ööpäevane koguannus. Ärge võtke kahekordset annust, kui annus jäi eelmisel korral võtmata.
Kui te lõpetate Strattera kasutamise
Kui te lõpetate Strattera kasutamise, ei ilmne tavaliselt mingeid kõrvalnähte, kuid teie ADHD sümptomid võivad taastuda. Konsulteerige enne ravi lõpetamist kõigepealt oma arstiga.
Asjad, mida teie arst teeb, kui te saate ravi
Teie arst teeb mõningaid uuringuid
-enne kui te ravi alustate – veendumaks, et Strattera on ohutu ja temast on kasu.
-pärast ravi alustamist – neid tehakse vähemalt iga 6 kuu järel, kuid võimalik on, et sagedamini.
Uuringuid tehakse ka siis, kui teie annust muudetakse. Need uuringud sisaldavad:
-kehakaalu ja pikkuse määramist lastel ja noorukitel
-vererõhu ja pulsisageduse mõõtmist
-kontrollimist, kas teil on Strattera võtmise ajal mingeid probleeme või kas kõrvaltoimed on halvenenud.
Pikaajaline ravi
Strattera’t ei ole vaja igavesti võtta. Kui te võtate Strattera’t kauem kui aasta, vaatab teie arst teie ravi uuesti üle, et näha kas ravim on ikka vajalik.
Kui teil on lisaküsimusi selle ravimi kasutamise kohta, pidage nõu oma arsti või apteekriga.
4.Võimalikud kõrvaltoimed
Nagu kõik ravimid, võib ka see ravim põhjustada kõrvaltoimeid, kuigi kõigil neid ei teki. Kuigi mõnedel inimestel tekivad kõrvaltoimed, leiab enamik, et Strattera on neile abiks. Teie arst rääib teile neist kõrvaltoimetest.
Mõned kõrvaltoimed võivad olla tõsised. Kui teil esineb mõni allpool toodud kõrvaltoimetest, pöörduge koheselt arsti poole.
-tunne, et teie süda lööb väga kiiresti, südame rütmihäired
-mõte või tunne, et tahaks ennast tappa
-agressiivsus
-ebasõbralikkus ja viha (vaenulikkus)
-meeleolukõikumised või tujumuutused
-tõsine allergiline reaktsioon, mille sümptomiteks on:
-näo ja kõri turse
-hingamisraskused
-nõgeslööve (väikesed nahapinnast kõrgemad sügelevad laigud)
-krambid
-psühhootilised sümptomid, sh hallutsinatsioonid (olematute asjade kuulmine või nägemine), mittetõeste asjade uskumine või umbusklikkus.
Lastel ja alla
-mõte või tunne, et tahaks ennast tappa (võib ilmneda kuni ühel inimesel
-meeleolukõikumised või tujumuutused (võib ilmneda kuni ühel inimesel
Täiskasvanutel on vähenenud risk (võib ilmneda kuni 1 inimesel
-krambid

-psühhootilised sümptomid, sh hallutsinatsioonid (olematute asjade kuulmine või nägemine), mittetõeste asjade uskumine või umbusklikkus.
Harva (võib ilmneda kuni
-maksakahjustus.
Te peate Strattera võtmise lõpetama ja informeerima koheselt oma arsti, kui teil esineb ükskõik milline järgmistest sümptomitest:
-tume uriin
-naha või silmade kollasus
-kõhuvalu, mis on tunda, kui te surute paremale poole roiete alla (hellus)
-seletamatu iiveldustunne
-väsimus
-sügelus
-gripitaolised sümptomid.
Teised teatatud kõrvaltoimed on järgmised. Kui need muutuvad tõsiseks, rääkige oma arsti või apteekriga.
Väga sageli esinevad kõrvaltoimed (võivad esineda rohkem kui 1 inimesel
|
LAPSED (üle |
|
TÄISKASVANUD |
- |
peavalu |
- |
iiveldus |
- |
kõhuvalu |
- |
suukuivus |
- |
söögiisu vähenemine (näljatunde |
- |
peavalu |
|
puudumine) |
- söögiisu vähenemine (näljatunde puudumine) |
|
- |
iiveldus või oksendamine |
- raskused uinumisega, magamisega ja varajane |
|
- |
unisus |
|
ärkamine |
- |
vererõhu tõus |
- |
vererõhu tõus |
- |
südame löögisageduse (pulsi) sagenemine |
- südame löögisageduse (pulsi) sagenemine |
|
Need toimed võivad enamikel patsientidel |
|
|
|
ajapikku kaduda. |
|
|
|
|
|
|
|

Sageli esinevad kõrvaltoimed (võivad esineda kuni 1 inimesel
|
LAPSED (üle |
|
TÄISKASVANUD |
- |
ärrituvus või ärevus |
- |
ärevus |
- |
magamisraskused, sh varajane ärkamine |
- |
seksuaalse huvi vähenemine |
- |
depressioon |
- |
unehäired |
- |
õnnetu või lootusetuse tunne |
- |
depressioon |
- |
rahutus |
- |
õnnetu või lootusetuse tunne |
- |
tikid |
- |
rahutus |
- |
suured pupillid (silma tume keskosa) |
- |
pearinglus |
- |
pearinglus |
- |
ebatavaline maitse suus või maitsetundlikkuse |
- |
kõhukinnisus |
|
muutused, mis ei ole mööduvad |
- |
söögiisu kadumine |
- |
värinad |
- |
maoärritus, seedehäired |
- |
käte või jalgade kihelus või tuimus |
- |
tursunud, punane ja sügelev nahk |
- |
unisus, uimasus, väsimus |
- |
nahalööve |
- |
kõhukinnisus |
- |
laiskustunne (letargia) |
- |
kõhuvalu |
- |
valu rinnus |
- |
seedehäired |
- |
väsimus |
- |
kõhugaasid (puhitus) |
- |
kehakaalu vähenemine |
- |
oksendamine |
|
|
- |
kuumahood või nahaõhetus |
|
|
- tunne, et teie süda lööb väga kiiresti |
|
|
|
- tursunud, punane ja sügelev nahk |
|
|
|
- |
suurenenud higistamine |
|
|
- |
nahalööve |
|
|
- raskused tualetis käimisel, nt võimetus |
|
|
|
|
urineerida, sagedane või ebakindel |
|
|
|
urineerimine, valulik urineerimine |
|
|
- |
eesnäärmepõletik (prostatiit) |
|
|
- |
kubemevalu meestel |
|
|
- |
erektsioonihäired |
|
|
- |
orgasmi ärajäämine |
|
|
- |
raskused erektsiooni hoidmisel |
|
|
- |
menstruaalkrambid |
|
|
- jõu või energia vähesus |
|
|
|
- |
väsimus |
|
|
- |
laiskustunne (letargia) |
|
|
- |
külmavärinad |
|
|
- |
ärrituvus, närvilisus |
|
|
- |
janutunne |
|
|
- |
kehakaalu vähenemine |

|
LAPSED (üle |
|
TÄISKASVANUD |
- |
minestamine |
- |
rahutus |
- |
värinad |
- |
tikid |
- |
migreen |
- |
minestamine |
- |
hägune nägemine |
- |
migreen |
- |
ebatavalised nahareaktsioonid, nagu |
- |
hägune nägemine |
|
- |
südame rütmihäired |
|
- |
käte või jalgade kihelus või tuimus |
|
pikenemine) |
- |
krambihood |
- |
sõrmede ja varvaste külmatunne |
- |
tunne, et teie süda lööb väga kiiresti (QT- |
- |
valu rinnus |
|
intervalli pikenemine) |
- |
hingeldus |
- |
hingeldus |
- |
punased sügelevad kupladega lööbed |
- |
suurenenud higistamine |
|
(nõgestõbi) |
- |
naha sügelus |
- |
lihasspasmid |
- |
jõu või energia vähesus |
- |
urineerimisvajadus |
|
|
- ebatavaline orgasm või orgasmi puudumine |
|
|
|
- |
ebakorrapärane menstruatsioon |
|
|
- |
ejakuleerimishäired |
|
|
||
|
Harva esinevad kõrvaltoimed (võivad esineda kuni 1 inimesel |
||
|
LAPSED (üle |
|
TÄISKASVANUD |
- |
vereringehäire, mis muudab varbad ja |
- |
vereringehäire, mis muudab varbad ja sõrmed |
|
sõrmed tuimaks ja kahvatuks (Raynaud’ |
|
tuimaks ja kahvatuks (Raynaud’ tõbi) |
|
tõbi) |
- |
pikenenud ja valulikud erektsioonid |
-raskused tualetis käimisel, nt sagedane või ebakindel urineerimine, valulik urineerimine
-pikenenud ja valulikud erektsioonid
-kubemevalu poistel
Toime kasvule
Mõnedel lastel esineb kasvupeetust (kehakaalus ja pikkuses), kui nad hakkavad Strattera’t võtma. Kuid pikaajalise ravi korral jõuavad lapsed siiski oma eakaaslastele kasvus ja kehakaalus järele. Teie arst jälgib ravi jooksul teie lapse kehakaalu ja pikkust. Kui teie laps ei arene kaalu ja pikkuse
poolest nii nagu eeldatud, võib arst muuta teie lapse ravimi annust või otsustab mõneks ajaks Strattera- ravi katkestada.
Kõrvaltoimetest teavitamine
Kui teil tekib ükskõik milline kõrvaltoime, pidage nõu oma arsti või apteekriga. Kõrvaltoime võib olla ka selline, mida selles infoelehes ei ole nimetatud. Kõrvaltoimetest võite ka ise teavitada www.ravimiamet.ee kaudu. Teavitades aitate saada rohkem infot ravimi ohutusest.
5.Kuidas Strattera’t säilitada
Hoidke seda ravimit laste eest varjatud ja kättesaamatus kohas.
Ärge kasutage seda ravimit pärast kõlblikkusaega, mis on märgitud karbil ja pudelil pärast „Kõlblik kuni“. Kõlblikkusaeg viitab selle kuu viimasele päevale.
Ärge kasutage suukaudset lahust hiljem, kui 45 päeva pärast pudeli esmast avamist.
See ravimpreparaat ei vaja säilitamisel eritingimusi.
Ärge visake ravimeid kanalisatsiooni ega olmejäätmete hulka. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. Need meetmed aitavad kaitsta keskkonda.

6.Pakendi sisu ja muu teave
Mida Strattera 4 mg/ml suukaudne lahus sisaldab
-Toimeaine on atomoksetiinvesinikkloriid. Üks ml suukaudset lahust sisaldab atomoksetiinvesinikkloriidi, mis vastab 4 mg atomoksetiinile.
-Teised abiained on naatriumbensoaat, naatriumdivesinikfosfaatdihüdraat, fosforhape, vedel sorbitool (kristalliseeruv) E420, ksülitool, kunstlik vaarika maitseaine, sukraloos, naatriumhüdroksiid, puhastatud vesi.
Kuidas Strattera välja näeb ja pakendi sisu
Suukaudne lahus, 4 mg/ml (selge värvitu)
Strattera suukaudset lahust turustatakse lapsekindla turvakorgiga pudelis, mis sisaldab 100 ml lahust. Pakendis on ka annustamise seade, mis koosneb 10 ml suusüstlast, mis on gradueeritud 1 ml kaupa ja pudeli kaelale surutavast adapterist.
Strattera suukaudne lahus on saadaval ühe pudeliga pakendis ja multipakendis, mis sisaldab 3 pudelit. Kõik pakendi suurused ei pruugi olla müügil.
Müügiloa hoidja ja tootja
Müügiloa hoidja:
Eli Lilly Holdings Limited Lilly House,
Priestley Road,
Basingstoke,
Hampshire,
RG24 9NL Ühendkuningriik
Tootja: Patheon France,
40 Boulevard de Champaret, 38300
Strattera on Eli Lilly and Company Limited kaubamärk.
See ravimpreparaat on saanud müügiloa Euroopa Majanduspiirkonna liikmesriikides järgmiste nimetustega:
Austria, Küpros, Tšehhi, Taani, Eesti, Soome, Saksamaa, Kreeka, Ungari, Island, Iirimaa, Itaalia, Leedu, Malta, Holland, Norra, Portugal, Rumeenia, Slovakkia, Sloveenia, Hispaania, Rootsi ja Ühendkuningriik: Strattera.
Lisaküsimuste tekkimisel selle ravimi kohta pöörduge palun müügiloa hoidja kohaliku esindaja poole. Eli Lilly Holdings Limited Eesti filiaal
Tammsaare tee 47 Tallinn 11316 Tel: +3726817280
Infoleht on viimati uuendatud juunis 2015.
Täpne teave selle ravimi kohta on Ravimiameti kodulehel.
Teave lastele ja noortele inimestele
See teave aitab sul teada saada peamistest asjadest sinu ravimi kohta, mida nimetatakse Strattera’ks. Kui sulle lugemine ei meeldi, võib keegi, näiteks su ema, isa või hooldaja (mõnikord nimetatakse „eestkostja”) sulle seda ette lugeda ja sinu küsimustele vastata.
See võib aidata, kui sa loed ise korraga väga vähe.
Miks mulle seda ravimit antakse?
See ravim aitab lapsi ja noori inimesi, kellel on „ADHD“.
•ADHD võib panna sind:
-liiga palju ringi jooksma
-mitte tähele panema
-tegutsema liiga kiiresti, ilma, et sa mõtleksid, mis järgmisena juhtub (impulsiivsus)
•See mõjutab õppimist, sõbrustamist ja seda, mida sa endast arvad. See ei ole sinu süü.
Selle ravimi võtmise ajal
•Lisaks selle ravimi võtmisele, saad sa oma
•See ravim peaks sind aitama. Kuid see ei ravi
•Sa pead mitu korda aastas käima oma arsti juures ennast näitamas. Seda on vaja selleks, et olla kindel, et sinu ravim toimib nii nagu vaja ja et sina kasvad ja arened korralikult.
•Tüdrukud peavad otsekohe oma arstile ütlema, kui nad arvavad, et nad on rasedaks jäänud. Meie ei tea veel, kuidas see ravim mõjub sündimata lapsele. Kui sa elad suguelu, pea palun arstiga nõu, kuidas rasedust vältida.
Mõned inimesed ei tohi seda ravimit võtta
Sa ei tohi seda ravimit võtta, kui:
•sa oled kahe viimase nädala jooksul võtnud ravimeid, mida nimetatakse monoaminooksüdaasi inhibiitoriteks (MAOI), näiteks fenelsiin;
•sul on silmahaigus, mida nimetatakse suletudnurgaga glaukoomiks (silmasisene rõhk on suurenenud);
•sul on tõsised probleemid oma südamega;
•sul on tõsised probleemid ajus olevate veresoontega;
•sul on neerupealiste kasvaja.
Mõned inimesed peavad enne selle ravimi võtma hakkamist rääkima oma arstiga
Sa pead arstile ütlema, kui sa:
•oled rase või toidad last rinnaga;
•võtad teisi ravimeid – sinu arst peab teadma kõikidest ravimitest, mida sa võtad;
•sul on mõtted endale või teistele viga tegemisest;
•on probleemid liiga kiirete südamelöökidega või südamelöökide vahelejäämine, ilma kehalise koormuseta;
•kuuled hääli või näed asju, mida teised ei näe;
•oled hädas probleemiga, et sa vihastad väga kergesti.
Kuidas ma pean oma ravimit võtma?
•Palu abi oma emalt, isalt või hooldajalt (mõnikord nimetatakse ”eestkostja”) ravimi võtmisel.
•Ravimit võib võtta koos söögiga või ilma söögita. Ravimit ei tohiks segada toidu või veega.
•Kui lahus on sinu naha või silmadega kokku puutunud, pöördu abi saamiseks vanemate poole.
•Arst ütleb sulle, mitu korda päevas sa pead oma ravimit võtma.
•Võta oma ravimit iga päev ühel ja samal ajal, see aitab sul ravimi võtmist meeles pidada.
•Ära lõpeta ravimi võtmist ilma, et sa sellest kõigepealt arstile räägiksid.
•Lahuse õige kogus mõõdetakse süstlasse ja süstal tühjendatakse sulle suhu. Ära hammusta süstalt.
Võimalikud kõrvaltoimed
Kõrvaltoimed on tahtmatud asjad, mis võivad ravimi võtmisel juhtuda. Kui midagi järgnevast sinuga juhtub, räägi sellest otsekohe mõnele täiskasvanule, keda sa usaldad. Nemad saavad siis sellest arstile rääkida. Kõige olulisemad asjad, mis sinuga juhtuda võivad, on:
•sinu süda hakkab lööma kiiremini, kui muidu;
•oled väga masendunud ja õnnetu või tahad endale viga teha;
•tunned agressiivsust;
•oled väga õnnetu või teistsuguses meeleolus kui tavaliselt (meeleolu kõigub);
•tekivad allergiale viitavad nähud, nt nahal tekib lööve, sügelemine või kublad, näo, huulte, keele või teiste kehaosade turse, hingeldus, vilistav hingamine või hingamisraskused;
•tekivad tõmblused (krambid);
•selliste asjade nägemine, tundmine või kuulmine, mida teised ei näe, tunne ega kuule;
•maksakahjustus: kõhuvalu, mis on tunda (kõht on hell ja tundlik), kui sa vajutad kõhu peale paremal pool, just roiete all.
Kuna see ravim võib muuta sind uniseks, on oluline, et sa ei teeks välisporti, näiteks ei lähe ratsutama või rattaga sõitma, ujuma või puude otsa ronima. Sa võid endale ja teistele haiget teha.
Kui sa tunned end selle ravimi võtmise ajal halvasti, räägi sellest otsekohe mõnele täiskasvanule, keda sa usaldad.
Muud asjad, mis tuleb meeles pidada
•Hoida kindlasti oma ravimit ohutus kohas, nii, et keegi teine seda võtta ei saaks, eriti su nooremad õed või vennad.
•See ravim on ainult sinu jaoks – ära luba kellelgi teisel seda võtta. See ravim võib aidata sind, kuid olla kellelegi teisele kahjulik.
•Kui sa unustasid ravimit võtta, ära võta järgmine kord kahte annust. Võtta ikka üks annus järgmisel, õigel võtmise ajal.
•Kui sa võtsid liiga palju ravimit, ütle seda otsekohe emale, isale või hooldajale.
•See on väga oluline, et sa ei võtaks liiga palju ravimit, sest see teeb sind haigeks.
•Ära lõpeta oma ravimi võtmist enne, kui arst ütleb, et see on OK.
Kelle käest ma saan küsida, kui on midagi, millest ma aru ei saa?
Sinu ema, isa, hooldaja, sinu arst, meditsiiniõde või apteeker oskavad sind aidata.

Strattera atomoksetiin suukaudne lahus
Kasutusjuhend
Üksikasjalik juhis STRATTERA kasutamiseks
KUI TE HAKKATE STRATTERA’t kasutama, lugege ja järgige hoolikalt kõiki juhise punkte.
 HOIATUS: Adapter võib tekitada LÄMBUMISOHU – sisaldab väikesi osi. Ärge ühendage süstalt adapteriga enne, kui see on täielikult pudelile kinnitatud. Ohutu kasutamise tagamiseks peab see olema korralikult pudelile kinnitatud. Kasutada ainult täiskasvanu järelvalve all.
HOIATUS: Adapter võib tekitada LÄMBUMISOHU – sisaldab väikesi osi. Ärge ühendage süstalt adapteriga enne, kui see on täielikult pudelile kinnitatud. Ohutu kasutamise tagamiseks peab see olema korralikult pudelile kinnitatud. Kasutada ainult täiskasvanu järelvalve all.
OSAD
 Lastekindel
Lastekindel
Kolb |
kork |
|
Adapter
 Ravim
Ravim
Süstla ots
Suusüstal Ravimi
pudel
TÄHTIS
ÄRGE lubage lapsel üksi, ilma teie abita ravimit võtta.
ÄRGE kasutage aegunud ravimit. (Kontrollige kõlblikkusaega etiketilt.)
ÄRGE kasutage ravimit kauem kui 45 päeva jooksul pärast pudeli esmakordset avamist. Vaata lõiku “Hävitamine”, kuidas toimida ravimiga, mida te enam ei kasuta.
ÄRGE peske suusüstalt seebi või detergendiga. ÄRGE pange suusüstalt nõudepesumasinasse. Kui te seda teete, ei pruugi süstal enam nii hästi töötada, kui peaks. Puhastamise juhisteks vaata tegevused N kuni P.
STRATTERA suukaudset lahust ei soovitata söögi ega veega segada, sest see võib muuta ravimi maitset või takistada kogu vajaliku annuse manustamist.
STRATTERA põhjustab silmade ärritust. Hoiduge silma sattumise eest. Kui ravimit satub silma, loputage silma kohe veega ja võtke arstiga ühendust. Peske niipea kui võimalik käsi ja kõiki pindu, mis võivad ravimiga kokku puutuda.
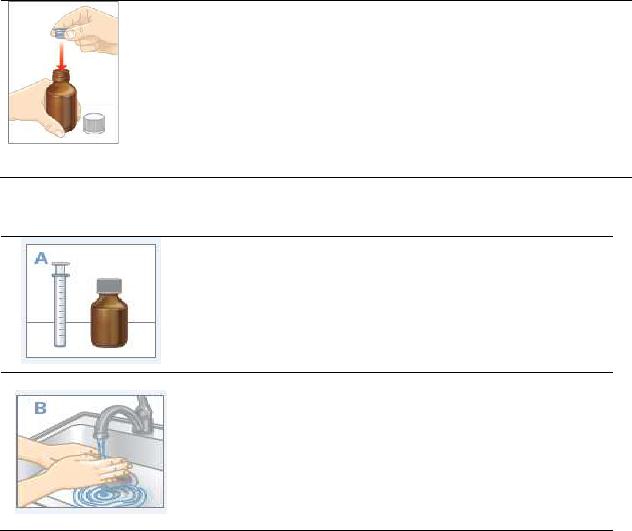
ESIMENE SAMM: PUDELI ALGNE ETTEVALMISTAMINE
Enne esmakordset kasutamist lükake adapter kogu pikkuses pudeli suule. Ärge ühendage süstalt enne kui adapter on täielikult pudelile kinnitatud.
ÄRGE adapterit keerake.
 HOIATUS: Adapter võib tekitada LÄMBUMISOHU – sisaldab väikesi osi. Ohutu kasutamise tagamiseks peab see olema korralikult pudelile kinnitatud.
HOIATUS: Adapter võib tekitada LÄMBUMISOHU – sisaldab väikesi osi. Ohutu kasutamise tagamiseks peab see olema korralikult pudelile kinnitatud.
TEINE SAMM: VALMISSEADMINE
Pange vajalikud osad valmis:
Ravimi pudel
Suusüstal
Peske oma käed vee ja seebiga.
Kirjutage siia oma lapse annus:
________ ml
Veenduge, et te kasutate just seda annust, mis arst teie lapsele määras.
Kui teie lapse ravimi annus on 10 ml VÕI VÄHEM, kasutate te süstalt üks kord.
Kui teie lapse ravimi annus on ROHKEM KUI 10 ml, aga vähem kui 20 ml, kasutate te seda sama süstalt 2 korda.
Kui teie lapse ravimi annus on ROHKEM KUI 20 ml, kasutate te seda sama süstalt 3 korda.
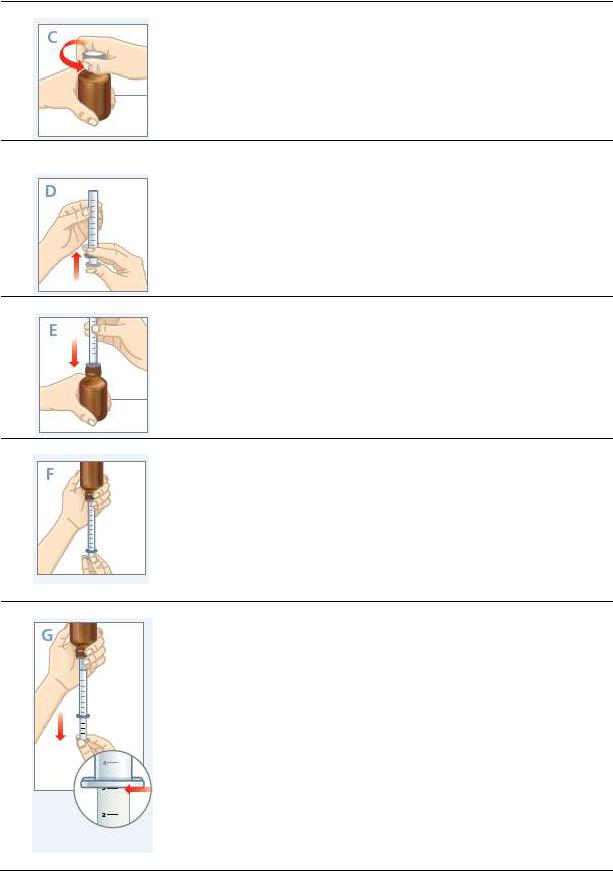
KOLMAS SAMM: ANNUSE ETTEVALMISTAMINE
Suruge korki alla ja keerake samal ajal päripäeva.
Keerake kork pudelilt ära.
Suruge kolb kogu pikkuses süstla otsani.
Pange süstla ots adapteri avale.
Veenduge, et süstla ots on täiesti adapteri sees.
Keerake pudel ja süstal teistpidi.
Hoidke pudelit ja süstalt ühe käega. Teise käega tõmmake kolbi allapoole, et vajalik kogus ravimit satuks süstlasse.
Kontrollige, kas õige kogus ravimit on süstlas.

Keerake pudel tagasi õiget pidi ja pange see tasasele alusele.
Kontrollige, ega süstlas pole õhumulle. Kui õhumull on sees, tühjendage süstla sisu tagasi pudelisse ja korrake tegevusi D kuni H. Õhumulli tõttu võite saada vale annuse.
Eemaldage süstal pudelilt.
ÄRGE puutuge kolbi.

NELJAS SAMM: RAVIMI MANUSTAMINE
Asetage süstla ots lapse suunurka. Öelge lapsele, et ta ei tohi süstalt hammustada.
Suruge kolb alla kuni KÕIK ravim on lapse suus.
ÄRGE pritsige ravimit kurgu tagaossa. Veenduge, et laps neelab kogu ravimi alla.
Kui teie lapse ravimi annus on ROHKEM KUI 10 ml, korrake tegevusi D kuni K, et anda lapsele annuse järgmine osa. Kasutage seda sama süstalt. Vaadake annustamise skeemi selle juhise teiselt küljelt.
Veenduge, et te kasutate just seda annust, mis arst teie lapsele määras.
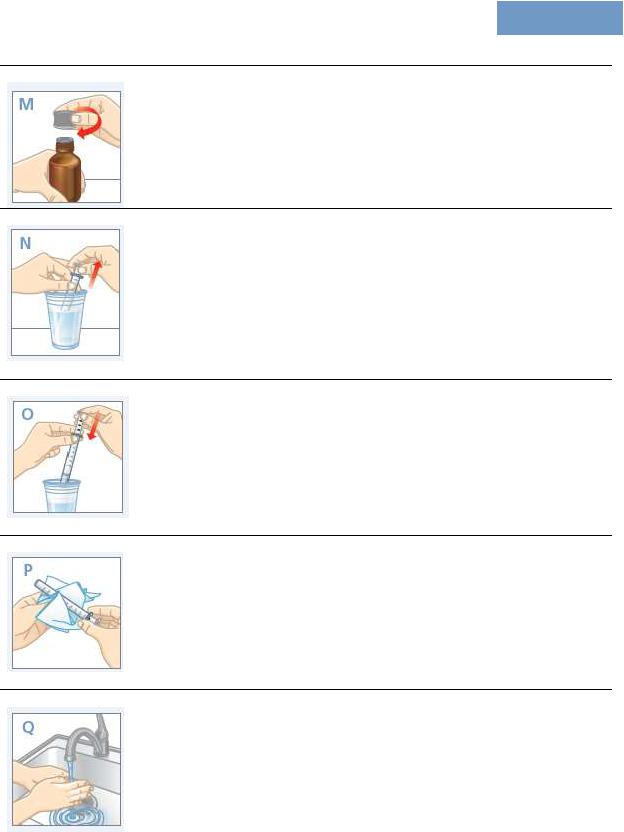
LEHEKÜLG 1
VIIES SAMM: PUHASTAMINE
Keerake kork tihedalt pudelile tagasi.
ÄRGE eemaldage adapterit. Kork katab selle ära.
Täitke tass puhta veega.
ÄRGE peske suusüstalt seebi või detergendiga.
ÄRGE eemaldage suusüstlast kolbi. Pange süstla ots vette. Tõmmake kolbi ja täitke süstal veega.
Suruge kolbi alla ja pritsige vett tassi või kraanikaussi.
Raputage liigne vesi süstlast.
Kuivatage süstal salvrätiga.
Peske oma käed ja lapse käed vee ja seebiga.
ÄRGE puudutage silmi pärast STRATTERA käsitsemist. STRATTERA võib ärritada silmi.
Teiselt küljelt leiate sagedamini esitatud küsimused, annustamise skeemi ja muud olulist teavet.

ANNUSTAMISE SKEEM 10 ML ÜLETAVATE ANNUSTE KORRAL |
LEHEKÜLG 2 |
|
|
|
|
Selle skeemi abil leiate, kuidas ravimi õiget kogust lapsele anda. Leidke esimesest tulbast õige annus. Rääkige oma arsti või apteekriga, kuidas lapsele õiget annust anda.
|
|
|
|
|
|
|
|
|
Võtke teisel korral |
|
|
Võtke kolmandal |
||
|
|
|
|
|
|
|
|
|
|
|
||||
|
Kui see on teie |
|
|
|
Võtke esimesel korral |
|
|
|
niipalju |
|
|
korral niipalju |
||
|
lapse annus |
|
|
|
niipalju STRATTERA’t |
|
|
|
STRATTERA’t |
|
|
STRATTERA’t |
||
|
|
|
|
|
süstlasse |
|
|
|
süstlasse |
|
|
süstlasse |
||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
11 ml |
|
|
|
10 ml |
|
|
|
1 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
12 ml |
|
|
|
10 ml |
|
|
|
2 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
13 ml |
|
|
|
10 ml |
|
|
|
3 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
14 ml |
|
|
|
10 ml |
|
|
|
4 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
15 ml |
|
|
|
10 ml |
|
|
|
5 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
16 ml |
|
|
|
10 ml |
|
|
|
6 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
17 ml |
|
|
|
10 ml |
|
|
|
7 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
18 ml |
|
|
|
10 ml |
|
|
|
8 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
19 ml |
|
|
|
10 ml |
|
|
|
9 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
20 ml |
|
|
|
10 ml |
|
|
|
10 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
21 ml |
|
|
|
10 ml |
|
|
|
10 ml |
|
|
|
1 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
22 ml |
|
|
|
10 ml |
|
|
|
10 ml |
|
|
|
2 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
23 ml |
|
|
|
10 ml |
|
|
|
10 ml |
|
|
|
3 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
24 ml |
|
|
|
10 ml |
|
|
|
10 ml |
|
|
|
4 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
25 ml |
|
|
|
10 ml |
|
|
|
10 ml |
|
|
|
5 ml |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Sageli esitatud küsimused
K. Mis sellest on, kui suusüstlas on õhumull?
V. ÄRGE andke ravimit oma lapsele. Õhumullid võivad põhjustada vale annuse manustamist. Tühjendage süstal pudelisse ja korrage tegevusi D kuni H.
K. Mis siis saab, kui süstlas on liiga palju ravimit?
V. Hoidke süstla ots pudelis. Hoidke pudel püsti. Suruge kolbi alla kuni süstlasse jääb õige kogus ravimit.
K. Mida teha, kui süstlas ei ole piisavalt ravimit?
V. Hoidke süstla ots pudelis. Keerake pudel teisipidi. Tõmmake kolbi niikaua kuni saate süstlasse õige annuse.
K. Mis siis juhtub, kui ravim satub minu või lapse silma?
V. Loputage silma kohe veega ja helistage arstile. Peske käsi ja kõiki kohti, mis võisid ravimiga kokku puutuda, niipea kui võimalik.
K. Kuidas ma saan selle ravimiga reisile minna?
V. Veenduge, et teil on kogu reisi jaoks piisavalt STRATTERA’t. Hoide ravimit ohutus kohas, püstises asendis ja toatemperatuuril.
K. Kas ma tohin STRATTERA’t enne lapsele andmist segada söögi või veega?
V. STRATTERA suukaudset lahust ei ole soovitatav segada söögi või veega. See võib mõjutada STRATTERA suukaudse lahuse maitset või takistada täisannuse manustamist. Te võite lapsele anda klaasitäie vett pärast seda, kui ta on kogu ravimi annuse ära võtnud.
Säilitamine
See ravimpreparaat ei vaja säilitamisel eritingimusi.
Hoidke pudelit ja süstalt laste eest varjatud ja kättesaamatus kohas.
Hävitamine
Ärge visake ravimeid kanalisatsiooni ega olmejäätmete hulka. Küsige oma apteekrilt, kuidas visata ära ravimeid, mida te enam ei kasuta. Need meetmed aitavad kaitsta keskkonda.
RAVIMI OMADUSTE KOKKUVÕTE
1.RAVIMPREPARAADI NIMETUS
STRATTERA, 4 mg/ml suukaudne lahus.
2.KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Üks ml suukaudset lahust sisaldab atomoksetiinvesinikkloriidi, mis vastab 4 mg atomoksetiinile.
INN. Atomoxetinum
Abiainete täielik loetelu vt lõik 6.1.
Teadaolevat toimet omav abiaine: üks ml sisaldab 32,97 mg sorbitooli.
3.RAVIMVORM
Suukaudne lahus.
Selge, värvitu.
4.KLIINILISED ANDMED
4.1Näidustused
Aktiivsus- ja tähelepanuhäire (ADHD) ravi vähemalt
Täiskasvanutel peavad eelnevalt lapseeas esinenud ADHD sümptomid olema kinnitust leidnud. Kolmanda osapoole kinnitus on soovitav ja atomoksetiinravi ei tohi alustada kui lapseea ADHD sümptomid ei ole tõestatud. Diagnoosi ei tohi panna ainuüksi ühe või enama ADHD sümptomi olemasolu tõttu. Lähtuvalt kliinilisest otsusest peab patsientidel olema vähemalt mõõduka raskusega ADHD, mida on näidatud vähemalt kahe või enama mõõduka talitlushäirega (näiteks sotsiaalne, akadeemiline ja/või töökeskkonna toimimine), mis mõjutavad isiku elu mitmeid tahke.
Lisainformatsioon selle preparaadi ohutuks kasutamiseks:
Kompleksravi hõlmab tavaliselt psühholoogilisi, pedagoogilisi ja sotsiaalseid abinõusid ning selle eesmärgiks on käitumishäirete sündroomiga patsientide stabiliseerimine. Käitumishäirete sündroom võib sisaldada anamneesis pikaajaliselt selliseid sümptomeid nagu halb tähelepanu maht, tähelepanu hajutatavus, emotsionaalne labiilsus, impulsiivsus, mõõdukas või raskekujuline hüperaktiivsus, kergemad neuroloogilised sümptomid ja kõrvalekalle
Farmakoteraapia ei ole näidustatud kõigile selle sündroomiga patsientidele ning otsus seda ravimit kasutada peab põhinema patsiendi sümptomite ja häirete raskusastme väga põhjalikul analüüsil, arvestades patsiendi vanust ja sümptomite püsimist.
4.2Annustamine ja manustamisviis
Annustamine
Strattera’t võib manustada ööpäevase üksikannusena hommikul. Patsientidele, kel ei saavutata rahuldavat ravivastust (taluvust [nt iiveldus või somnolentsus] või efektiivsust) Strattera manustamisel
üks kord ööpäevas, võib paremini sobida ravimi manustamine kahe võrdse osana hommikul ja hilisel pärastlõunal või varajasel õhtul.
Lapsed:
Annustamine alla 70 kg kehakaaluga lastel:
1,2 mg/kg/ööpäevas korral ei ole täiendavat kasu täheldatud. Suuremate annuste kui üksikannused 1,8 mg/kg/ööpäevas ja ööpäevased koguannused 1,8 mg/kg ohutust ei ole süstemaatiliselt hinnatud. Mõnedel juhtudel võib vajalikuks osutuda ravi jätkamine täiskasvanueas.
Annustamise hõlbustamiseks on Strattera suukaudse lahuse pakendis suukaudse annustamise seade, mis koosneb 10 ml suusüstlast, mis on gradueeritud 1 ml kaupa ja pudeli kaelale surutavast adapterist. Suukaudse lahuse annused määratakse vastavalt allolevale tabelile:
Kehakaal |
Algannus |
Sihtannus |
|
|
|
(kg) |
(ml/ööpäevas) |
(ml/ööpäevas) |
|
|
|
16...18 |
||
|
|
|
20...21 |
||
22...24 |
||
25...28 |
||
29...31 |
||
32...34 |
||
|
|
|
36...38 |
||
39...41 |
||
42...44 |
||
45...48 |
||
49...51 |
||
52...54 |
||
55...58 |
||
60...61 |
||
62...64 |
||
65...67 |
||
68...69 |
||
≥70 |
Annustamine üle 70 kg kehakaaluga lastel
Maksimaalne soovituslik ööpäevane koguannus on 100 mg. Suuremate annuste kui üksikannused 120 mg ja ööpäevased koguannused 150 mg ohutust ei ole süstemaatiliselt hinnatud.
Täiskasvanud:
Lisainformatsioon selle preparaadi ohutuks kasutamiseks:
Enne ravimi määramist on vajalik võtta piisav anamnees ja anda patsiendi kardiovaskulaarse seisundi ravieelne hinnang, sh vererõhu väärtus ja pulsisagedus (vt lõigud 4.3 ja 4.4).
Jätkuv jälgimine:
Vajalik on kardiovaskulaarse seisundi regulaarne jälgimine koos vererõhu väärtuse ja pulsisageduse salvestamisega annuse igakordse kohandamise järel ning seejärel korrata seda vähemalt iga 6 kuu järel. Laste puhul on soovitatav kasutada pertsentiilide tabelit. Täiskasvanute puhul tuleb jälgida kehtivaid hüpertensiooni ravijuhiseid (vt lõik 4.4).
Ravi ärajätmine:
Uuringuprogrammis ei ole täheldatud ilmseid ärajätusümptomeid. Oluliste kõrvaltoimete tekkimisel võib atomoksetiinravi järsult katkestada, muidu on soovitatav ravi lõpetamisel annust teatava aja jooksul
Eripopulatsioonid
Maksapuudulikkus: mõõduka maksapuudulikkusega patsientidel
Neerupuudulikkus: lõppstaadiumis neeruhaigusega patsientidel tuvastati süsteemselt tsirkuleeriva atomoksetiini suurem hulk kui normaalse neerufunktsiooniga inimestel (ligikaudu 65 % suurem), kuid erinevust ei esinenud siis, kui annust korrigeeriti mg/kg alusel. Seega võib Strattera’t manustada aktiivsus- ja tähelepanuhäirega patsientidele, kel esineb lõppstaadiumis neeruhaigus või neerupuudulikkuse kergemad astmed, tavalise annustamisskeemi alusel. Lõppstaadiumis neeruhaigusega patsientidel võib atomoksetiin ägestada arteriaalset hüpertensiooni (vt lõik 5.2).
Ligikaudu 7
Eakad: atomoksetiini kasutamist ei ole üle
Alla
Manustamisviis
Suukaudseks kasutamiseks. Strattera’t võib manustada koos toiduga või ilma. Strattera suukaudset lahust ei ole soovitatav segada toiduga või veega, kuna see võib takistada patsiendil saamast kogu annust või võib mõjutada maitset.
4.3Vastunäidustused
Ülitundlikkus toimeaine või lõigus 6.1 loetletud mis tahes abiainete suhtes.
Atomoksetiini ei tohi kasutada koos monoaminooksüdaasi inhibiitoritega (MAO inhibiitoritega). Atomoksetiini ei tohi kasutada vähemalt 2 nädala jooksul pärast MAO inhibiitorite kasutamise lõpetamist. Ravi MAO inhibiitoritega ei tohi alustada varem kui 2 nädalat pärast atomoksetiinravi lõppu.
Atomoksetiini ei tohi kasutada suletudnurga glaukoomiga patsientidel, kuna kliinilistes uuringutes kaasnes atomoksetiini kasutamisega müdriaasi esinemissageduse suurenemine.
Atomoksetiini ei tohi kasutada raske südameveresoonkonna või tserebrovaskulaarse häirega patsientidel (vt lõik 4.4 Erihoiatused ja ettevaatusabinõud kasutamisel – Kardiovaskulaarsed toimed). Südameveresoonkonna raske häire all mõistetakse rasket hüpertensiooni, südamepuudulikkust, arterite sulgust, stenokardiat, hemodünaamiliselt olulist kaasasündinud südamehaigust, kardiomüopaatiaid, müokardiinfarkti, potentsiaalselt eluohtlikku arütmiat ja
Atomoksetiini ei tohi kasutada feokromotsütoomiga või anamneesis feokromotsütoomiga patsiendid (vt lõik 4.4 Erihoiatused ja ettevaatusabinõud kasutamisel – Kardiovaskulaarsed toimed).
4.4Erihoiatused ja ettevaatusabinõud kasutamisel
Suitsidaalne käitumine
Atomoksetiiniga ravitud patsientidel on täheldatud suitsidaalset käitumist (suitsiidikatsed ja suitsiidimõtted). Topeltpimedates kliinilistes uuringutes esines suitsidaalseid juhte
Äkksurm ja eelnev kardiaalne hälve
Atomoksetiini tavaannustes kasutanud struktuurse kardiaalse hälbega patsientidel on teatatud äkksurmast. Kuigi mõned tõsised struktuursed kardiaalsed hälbed ise põhjustavad kõrgemat riski äkksurma tekkeks, tohib atomoksetiini teadaoleva tõsise struktuurse kardiaalse hälbega patsientidel kasutada ainult erilise ettevaatusega ning kardioloogiga konsulteerides.
Kardiovaskulaarsed toimed
Atomoksetiin võib mõjutada pulsisagedust ja vererõhku.
Enamus atomoksetiini võtvatest patsientidest kogeb mõõdukat pulsisageduse kiirenemist (keskmiselt <10 lööki/minutis) ja/või vererõhu tõusu (keskmiselt <5 mm/Hg) (vt lõik 4.8).
Siiski näitavad ADHD kontrolliga ja kontrollita kliinilistest uuringutest saadud kombineeritud andmed, et ligikaudu 8…12 % lastest ja noorukitest ning 6...10% täiskasvanutest kogevad tugevalt väljendunud pulsisageduse (20 või enam lööki minutis) ning vererõhu muutusi (15…20 või enam mm/Hg). Nende kliiniliste uuringute andmete analüüs näitas, et ligikaudu 15…26 % lastest ja noorukitest ning 27...32% täiskasvanutest kogeb atomoksetiinravi ajal sellist pidevat või progressiivset
vererõhu ja pulsisageduse muutust. Pikaajalised püsivad vererõhu muutused võivad potentsiaalselt kaasa tuua kliinilisi tagajärgi nagu südamelihase hüpertroofia.
Nende leidude tulemuste tõttu tuleb patsientidelt, kellele on kavatsetud määrata atomoksetiinravi, võtta anamnees väga hoolikalt ja teha patsiendi läbivaatus, et hinnata südamehaiguse olemasolu ning kui esialgsed leiud viitavad sellise anamneesi või haiguse olemasolule, on soovitatav kardioloogi konsultatsioon.
Enne ravi algust, ravi ajal ja pärast annuse igakordset korrigeerimist ning seejärel vähemalt iga 6 kuu järel on soovitatav mõõta ja salvestada pulsisagedust ja vererõhu väärtusi, et tuvastada paremini võimalikku kliiniliselt olulist tõusu. Laste puhul on soovitatav kasutada pertsentiilide tabelit. Täiskasvanute puhul tuleb jälgida kehtivaid hüpertensiooni ravijuhiseid.
Atomoksetiini ei tohi kasutada raske kardiovaskulaarse või tserebrovaskulaarse häirega patsiendid (vt lõik 4.3 Vastunäidustused – Südameveresoonkonna või tserebrovaskulaarse raske häirega patsiendid). Atomoksetiini tuleb kasutada ettevaatusega patsientidel, kelle kaasuv haigus võib vererõhu tõusu ja pulsisageduse kiirenemise tõttu halveneda, nt hüpertoonikud, tahhükardia või kardiovaskulaarse või tserebrovaskulaarse haigusega patsiendid.
Patsiendid, kes kogevad atomoksetiinravi ajal südamehaigusele viitavaid sümptomeid, nt palpitatsioonid, pingutusel valu rinnus, seletamatud minestamised, düspnoe ja teisi sümptome, peaksid minema koheselt kardioloogi juurde erialasele konsultatsioonile.
Lisaks tuleb atomoksetiini kasutada ettevaatusega kaasasündinud või omandatud pika
Kuna teatatud on ka ortostaatilise hüpotensiooni tekkest, tuleb atomoksetiini kasutada ettevaatusega mistahes seisundi korral, mis võivad patsiendil soodustada hüpotensiooni teket või seisundite korral, mis on seotud järskude südamerütmi või vererõhu muutustega.
Tserebrovaskulaarsed toimed
Tserebrovaskulaarsete seisundite lisariskifaktoritega patsientidel (nt anamneesis kardiovaskulaarne haigus, kaasuv ravi vererõhku tõstvate ravimitega), tuleb pärast ravi alustamist atomoksetiiniga iga visiidi ajal hinnata neuroloogilisi nähte ja sümptomeid.
Toimed maksale
Väga harva on olnud spontaanseid teateid maksakahjustusest, mis on väljendunud maksaensüümide aktiivsuse tõusus ja bilirubiinitaseme tõusus koos ikterusega. Samuti on väga harva teatatud raskest maksakahjustusest, sh ägedast maksapuudulikkusest. Ikteruse või laboratoorselt kinnitatud maksakahjustusega patsientidel tuleb Strattera manustamine lõpetada ega tohi enam uuesti alustada.
Psühhootilised või maniakaalsed sümptomid
Ravi atomoksetiini tavaannustega võib põhjustada ilma eelneva psüühilise või maniakaalse haiguseta patsientidel psühhootilisi või maniakaalseid sümptomeid, nt hallutsinatsioone, pettekujutelmi, maniat või agiteeritust. Selliste sümptomite ilmnemisel tuleb kaaluda nende võimalikku seost atomoksetiinraviga ning vajadusel ravi katkestada. Ei saa välistada võimalust, et Strattera võib põhjustada eelnevalt olemasolevate psühhootiliste või maniakaalsete sümptomite ägenemist.
Agressiivne käitumine, vaenulikkus või emotsionaalne labiilsus
Vaenulikkust (eeskätt agressiivsust, vastuolulist käitumist ja viha) täheldati kliinilistes uuringutes sagedamini Strattera`ga ravitud lastel, noorukitel ja täiskasvanutel, võrreldes platseeboga. Lastega läbiviidud kliinilistes uuringutes täheldati Stratterat saanud lastel emotsionaalset labiilsust sagedamini kui platseebot saanutel. Patsiente tuleb tähelepanelikult jälgida agressiivse käitumise, vaenulikkuse või emotsionaalse labiilsuse ilmnemise või halvenemise osas.
Võimalikud allergilised reaktsioonid
Atomoksetiini kasutavatel patsientidel on
Krambid
Atomoksetiiniga kaasneb potentsiaalne krampide tekke risk. Atomoksetiini tuleb ettevaatusega kasutama hakata patsientidel, kellel on varem esinenud krampe. Atomoksetiinravi lõpetamist peaks kaaluma iga patsiendi puhul, kellel tekivad krambid või juhul, kui krampide esinemissagedus suureneb ning selleks ei ole mingit muud põhjust avastatud.
Kasv ja areng
Atomoksetiinravi ajal tuleb jälgida laste ja noorukite kasvu ja arengut. Pikaajalist ravi vajavaid patsiente tuleb jälgida ning laste ja noorukite puhul, kes ei kasva või ei võta piisavalt kaalus juurde, tuleb kaaluda annuse vähendamist või ravi katkestamist.
Kliinilised andmed ei osuta atomoksetiini kahjulikele toimetele seoses kognitiivse arengu või sugulise küpsemisega, kuid pikaajaliste vaatlusandmete hulk on piiratud. Seetõttu tuleb pikaajalist ravi saavaid patsiente hoolikalt jälgida.
Kaasuva depressiooni, ärevuse ja tikkide uued hood või seisundi halvenemine
ADHD ja kaasuvate krooniliste motoorsete tikkidega või Tourette’i sündroomiga pediaatrilistel patsientidel läbi viidud kontrollitud uuringus ei halvendanud atomoksetiin platseeboga võrreldes tikke. ADHD ja kaasuva depressiooniga täiskasvanud patsientidel läbi viidud kontrollitud uuringus ei halvendanud atomoksetiin platseeboga võrreldes depressiooni. Kahes ADHD ja kaasuva ärevushäirega patsientidega läbi viidud kontrollitud uuringus (üks lastega ja teine täiskasvanutega) ei halvendanud atomoksetiin platseeboga võrreldes ärevushäiret.
Turuletulekujärgselt on olnud harva teateid ärevuse ja depressiooni või depressiivse meeleolu ja väga harva tikkide esinemise kohta atomoksetiini kasutavatel patsientidel (vt lõik 4.8).
Patsiente, kellel juba ravitakse
Alla 6 aasta vanused lapsed
Strattera’t ei tohi alla 6 aasta vanustel patsientidel kasutada, sest ravimi ohutust ja efektiivsust selles patsientide vanusegrupis ei ole tõestatud.
Muu terapeutiline kasutamine
Strattera ei ole näidustatud depressiivsete episoodide ja/või ärevuse raviks, kuna nende täiskasvanute seas, kellel ei esinenud
Strattera suukaudne lahus sisaldab sorbitooli. Patsiendid, kellel on harvaesinev pärilik fruktoosi talumatus, ei tohi seda ravimit kasutada.
4.5Koostoimed teiste ravimitega ja muud koostoimed
Teiste ravimite toimed atomoksetiinile
MAO inhibiitorid
Atomoksetiini ei tohi koos MAO inhibiitoritega kasutada (vt lõik 4.3).
CYP2D6 inhibiitorid
Neid ravimeid saavatel patsientidel võib atomoksetiini ekspositsioon 6…8 korda suureneda ja maksimaalne tasakaalukontsentratsioon (Css max) on 3…4 korda suurem, sest ta metaboliseerub CYP2D6 kaasabil. Patsientidel, kes juba kasutavad CYP2D6 inhibiitoreid, võib osutuda vajalikuks aeglasem tiitrimine ja atomoksetiini väiksem lõplik annus. Kui pärast atomoksetiini sobiva annuse
väljatiitrimist ordineeritakse või jäetakse ära CYP2D6 inhibiitor, tuleb antud patsiendil kliinilist vastust ja taluvust uuesti hinnata, otsustamaks, kas on vaja annuse korrigeerimist.
Samaaegne tsütokroom P450 inhibiitorite manustamine aeglastele CYP2D6 abil metaboliseerijatele peab toimuma ettevaatusega, kuna kliiniliselt oluliste tõusude toime atomoksetiini avaldumises on in vivo uuringutest teadmata.
Salbutamool (või teised beeta2 agonistid)
Patsientidele, kes kasutavad samaaegselt salbutamooli (või teiste beeta2 agonistide) suuri annuseid kas nebulisaatori kaudu või süsteemselt, tuleb atomoksetiini manustada ettevaatusega, kuna toime kardiovaskulaarsüsteemile võib tugevneda.
Selle koostoime kohta on leitud vasturääkivaid fakte. Süsteemselt manustatud salbutamool
(600 mikrogrammi i.v. 2 tunni järel) kombinatsioonis atomoksetiiniga (60 mg kaks korda ööpäevas, 5 päeva) tekitab pulsisageduse kiirenemise ja vererõhu tõusu. See toime avaldus kõige ilmekamalt salbutamooli ja atomoksetiini algsel koosmanustamisel, kuid taandus algväärtusele 8 tunni möödudes. Kuid eraldi uuringus tervete asiaatidest täiskasvanutega, kes on atomoksetiini kiired metaboliseerijad, ei suurenenud siiski salbutamooli toimed vererõhule ja pulsisagedusele tavaannuste
(200 mikrogrammi) inhaleerimisel atomoksetiini (80 mg üks kord ööpäevas 5 päeva vältel) koosmanustamisel. Salbutamooli korduva inhaleerimise (800 mikrogrammi) järel oli pulsisagedus samasugune nii atomoksetiini kasutamisel kui ka mittekasutamisel. Kui atomoksetiini või salbutamooli (või teiste beeta2 agonistide) koosmanustamise ajal on südame löögisagedus või vererõhk märkimisväärselt tõusnud, tuleb vererõhku ja südame löögisagedust tähelepanelikult jälgida ning vajadusel annust kohandada.
QT intervalli pikenemise potentsiaalne risk esineb juhul, kui atomoksetiini manustatakse koos teiste
Atomoksetiini kasutamisega kaasneb potentsiaalne krampide tekke risk. Ettevaatusega tuleb atomoksetiiniga samaaegselt kasutada krampide esinemissagedust vähendavaid ravimeid (nt tritsüklilised antidepressandid või
Antihüpertensiivsed ravimid
Atomoksetiini tuleb kasutada ettevaatusega koos antihüpertensiivsete ravimitega. Vererõhu võimaliku tõusu tõttu võib atomoksetiin vähendada antihüpertensiivsete ravimite/hüpertensiooni ravimite efektiivsust. Tähelepanu tuleb pöörata vererõhu kontrollile ja vajadusel tuleb atomoksetiini või antihüpertensiivne ravi üle vaadata ning vererõhu märkimisväärsete muutuste korral annuseid kohandada.
Pressoorsed ained ja vererõhku tõstvad ravimid
Vererõhu võimaliku tõusu tõttu tuleb atomoksetiini ettevaatusega kasutada koos pressoorsete ainete või ravimitega, mis võivad vererõhku tõsta (nt salbutamool). Vererõhu jälgimisel on vajalik ettevaatus ja vajadusel tuleb atomoksetiini või pressoorsete ainete ravi üle vaadata ning vererõhu märkimisväärsete muutuste korral annuseid kohandada.
Noradrenaliini toimet mõjutavad ravimid
Noradrenaliini toimet mõjutavaid ravimeid tuleb koos atomoksetiiniga kasutada ettevaatusega, kuna esineb farmakoloogiliste toimete summeerumise või sünergismi võimalus. Selliste ravimite hulka kuuluvad antidepressandid nagu imipramiin, venlafaksiin ja mirtasapiin ning nina limaskestade turset alandav aine pseudoefedriin või fenüülefriin.
Mao
Mao
Suure valguseonduvusega ravimid
Atomoksetiini ja teiste suure seonduvusega ravimite terapeutiliste kontsentratsioonidega viidi in vitro läbi ravimi sidumiskohast väljatõrjumise uuringud. Varfariin, atsetüülsalitsüülhape, fenütoiin või diasepaam ei mõjutanud atomoksetiini seondumist inimese albumiinidega. Samuti ei mõjutanud atomoksetiin nende ühendite seondumist inimese albumiiniga.
4.6Fertiilsus, rasedus ja imetamine
Rasedus
Loomkatsed ei näita üldiselt otsest kahjulikku toimet rasedusele, embrüo/loote arengule, sünnitusele või postnataalsele arengule (vt lõik 5.3). Atomoksetiini kasutamise kohta rasedatel on andmeid piiratud hulgal. Need andmed on ebapiisavad otsustamaks kas atomoksetiini ja kahjuliku toime vahel rasedusele ja/või imetamisele on seos või see seos puudub. Atomoksetiini ei tohi raseduse ajal kasutada, kui võimalik kasu emale ei ületa ohtu lootele.
Imetamine
Atomoksetiin ja/või selle metaboliidid eritusid rottidel emapiima. Ei ole teada, kas atomoksetiin eritub inimese rinnapiima. Andmete puudumise tõttu ei tohi atomoksetiini rinnaga toitmise ajal kasutada.
4.7Toime reaktsioonikiirusele
Andmed ravimi toime kohta autojuhtimisele ja masinate käsitsemise võimele on piiratud. Stratteral on kerge toime autojuhtimise ning masinate kasutamise võimele. Atomoksetiini on seostatud väsimuse, unisuse ja pearingluse tekke suurenemisega lastel ja täiskasvanutel võrreldes platseeboga. Patsientidel tuleb soovitada autojuhtimisel või ohtlike masinate kasutamisel olla eriti ettevaatlik, kuni nad ei ole täiesti kindlad, et atomoksetiin ei ole nende tähelepanuvõimet kahjustanud.
4.8Kõrvaltoimed
Lapsed:
Ohutusprofiili kokkuvõte
Lastega läbiviidud platseebokontrolliga uuringutes olid kõige sagedamini esinevateks atomoksetiiniga seotud kõrvaltoimeteks peavalu, kõhuvalu1 ja söögiisu vähenemine, mida on registreeritud vastavalt 19
Koos söögiisu vähenemisega esineb mõnel patsiendil ravi alguses kasvu pidurdumine (aeglustumine) nii kaalu kui ka pikkuse näitajates. Enamasti, pärast esialgset kehakaalu ja kehapikkuse tõusu aeglustumist saavutasid atomoksetiiniga ravitud patsiendid grupi algandmete põhjal ette nähtud keskmise kehakaalu ja kehapikkuse tõusu pikaajalise ravi jooksul.
Iiveldus, oksendamine ja unisus2 võivad esineda ligikaudu 10…11
Nii laste kui täiskasvanutega läbiviidud platseebokontrolliga uuringutes täheldati atomoksetiini kasutavatel patsientidel südame löögisageduse kiirenemist, süstoolse ja diastoolse vererõhu tõusu (vt lõik 4.4).
Atomoksetiini kasutavatel patsientidel on registreeritud ortostaatilist hüpotensiooni (0,2 %) ja sünkoopi (0,8 %), kuna aine mõjutab noradrenergilist toonust. Igasuguste hüpotensiooni soodustavate seisundite korral tuleb atomoksetiini kasutada ettevaatusega.
Järgnev kõrvaltoimete tabel põhineb kõrvaltoimetest teatamisel ning laboratoorsetel leidudel kliinilistest uuringutest ja kõrvaltoime teadetest turuletulekujärgselt lastel ja noorukitel.
Kõrvaltoimete tabelkokkuvõte
Esinemissagedus: väga sage (≥ 1/10), sage (≥ 1/100 kuni < 1/10),
Organsüsteemi |
Väga sage |
Sage |
Harv |
|
klass |
≥1/10 |
≥ 1/100 kuni |
≥ 1/1000 kuni |
≥ 1/10000 kuni |
|
|
< 1/10 |
< 1/100 |
< 1/1000 |
Vähenenud |
Anoreksia |
|
|
|
toitumishäired |
söögiisu |
(söögiisu |
|
|
|
|
puudumine |
|
|
Psühhiaatrilised |
|
Ärrituvus, |
Suitsidaalne |
|
häired |
|
meeleolu |
käitumine, |
|
|
|
muutused, |
agressiivsus, |
|
|
|
unetus, |
vaenulikkus, |
|
|
|
agiteeritus*, |
emotsionaalne |
|
|
|
ärevus, |
labiilsus*, psühhoos |
|
|
|
depressioon ja |
(sh |
|
|
|
depressiivne |
hallutsinatsioonid)* |
|
|
|
meeleolu*, |
|
|
|
|
tikid* |
|
|
Närvisüsteemi |
Peavalu, |
Pearinglus |
Sünkoop, treemor, |
|
häired |
unisus |
|
migreen, |
|
|
|
|
paresteesia*, |
|
|
|
|
hüpesteesia*, |
|
|
|
|
krambid** |
|
Silma |
|
Müdriaas |
Hägune nägemine |
|
kahjustused |
|
|
|
|
Südame häired |
|
|
Palpitatsioonid, |
|
|
|
|
siinustahhükardia, |
|
|
|
|
QT intervalli |
|
|
|
|
pikenemine** |
|
Vaskulaarsed |
|
|
|
Raynaud’ sündroom |
häired |
|
|
|
|
Respiratoorsed, |
|
|
Düspnoe (vt lõik |
|
rindkere ja |
|
|
4.4) |
|
mediastiinumi |
|
|
|
|
häired |
|
|
|
|
Seedetrakti |
Kõhuvalu, |
Kõhukinnisus, |
|
|
häired |
oksendamine, |
düspepsia |
|
|
|
iiveldus |
|
|
|
Maksa ja |
|
|
Bilirubiinisisalduse |
Maksaensüümide |
sapiteede häired |
|
|
tõus veres* |
aktiivsuse |
|
|
|
|
muutused/tõus, |
|
|
|
|
ikterus, hepatiit, |
|
|
|
|
maksakahjustus, äge |
|
|
|
|
maksapuudulikkus* |
Naha ja |
|
Dermatiit, |
Hüperhidroos, |
|
nahaaluskoe |
|
pruuritus, |
allergilised |
|
kahjustused |
|
lööve |
reaktsioonid |
|
|
|
|
|
Neerude ja |
|
|
|
Urineerimisraskus, |
kuseteede häired |
|
|
|
kusepeetus |
Reproduktiivse |
|
|
|
Priapism, genitaalide |
süsteemi ja |
|
|
|
valu meestel |
rinnanäärme |
|
|
|
|
häired |
|
|
|
|
Üldised häired ja |
|
Väsimus, |
Asteenia |
|
manustamiskoha |
|
letargia, valu |
|
|
reaktsioonid |
|
rinnus (vt lõik |
|
|
|
|
4.4) |
|
|
Uuringud |
Vererõhu |
Kehakaalu |
|
|
|
tõus, |
langus |
|
|
|
pulsisageduse |
|
|
|
|
kiirenemine |
|
|
|
Siia kuulub ka ülakõhuvalu, ebamugavustunne maos, kõhuõõnes ja ülakõhus
Siia kuulub ka sedatsioon
Siia kuulub algne, kesköine ja varajane unetus (varahommikused ärkamised)
Pulsisageduse ja vererõhu leiud põhinevad mõõdetud elulistel näitajatel |
|
|
*Vt lõik 4.4
** Vt lõigud 4.4 ja 4.5.
CYP2D6 aeglased metaboliseerijad (AM)
Järgnevaid kõrvaltoimeid täheldati vähemalt 2
Täiskasvanud
Ohutusprofiili kokkuvõte
Täiskasvanud ADHD patsientidega läbiviidud kliinilistes uuringutes esines ravi ajal atomoksetiiniga järgmistes organsüsteemi klassides kõrvaltoimeid kõige suurema esinemissagedusega: seedetrakti, närvisüsteemi ja psühhiaatrilised häired. Kõige sagedamini teatatud kõrvaltoimed (≥5%) olid söögiisu vähenemine (14,9%), unetus (11,3%), peavalu (16,3%), suukuivus (18,4%) ja iiveldus (26,7%). Enamus nendest kõrvaltoimetest olid tõsiduselt kerged või mõõdukad ning nendest omakorda kõige sagedamini teatati raskekujulisest iiveldusest, unetusest, väsimusest ja peavalust.. Täiskasvanutel tuleb kusepeetuse või urineerimisraskuse esinemisel selle võimaliku põhjusena arvestada atomoksetiinravi.
Järgnev kõrvaltoimete tabel põhineb kõrvaltoimetest teatamisel ning laboratoorsetel leidudel kliinilistest uuringutest ja kõrvaltoime teatistest turuletulekujärgselt täiskasvanutel.
Kõrvaltoimete tabelkokkuvõte
Esinemissagedus: väga sage (≥ 1/10), sage (≥ 1/100 kuni < 1/10),
Organsüsteemi |
Väga sage |
Sage |
Harv |
|
klass |
≥ 1/10 |
≥ 1/100 kuni |
≥ 1/1000 kuni |
≥1/10000 kuni |
|
|
< 1/10 |
< 1/100 |
<1/1000 |
Ainevahetus- ja |
Vähenenud |
|
|
|
toitumishäired |
söögiisu |
|
|
|
Psühhiaatrilised |
Unetus |
Agiteeritus*, |
Suitsidaalne |
Psühhoosid (sh |
häired |
|
libiido langus, |
käitumine*, |
hallutsinatsioonid)* |
|
|
unehäired, |
agressiivsus, |
|
|
|
depressioon ja |
vaenulikkus ja |
|
|
|
depressiivne |
emotsionaalne |
|
|
|
meeleolu*, ärevus |
labiilsus*, |
|
|
|
|
rahutus, tikid* |
|
Närvisüsteemi |
Peavalu |
Pearinglus, |
Sünkoop, |
Krambid** |
häired |
|
düsgeuusia, |
migreen, |
|
|
|
paresteesia, |
hüpesteesia* |
|
|
|
somnolentsus (sh |
|
|
|
|
sedatsioon), |
|
|
|
|
treemor |
|
|
Südame häired |
|
Palpitatsioonid, |
QT intervalli |
|
|
|
tahhükardia |
pikenemine** |
|
Silma kahjustused |
|
|
Hägune |
|
|
|
|
nägemine |
|
Vaskulaarsed |
|
Nahaõhetus, |
Perifeerne |
Raynaud’ sündroom |
häired |
|
kuumahood |
külmatunne |
|
Respiratoorsed, |
|
|
Düspnoe (vt |
|
rindkere ja |
|
|
lõik 4.4). |
|
mediastiinumi |
|
|
|
|
häired |
|
|
|
|
Seedetrakti |
Suukuivus, |
Kõhuvalu, |
|
|
häired |
iiveldus |
kõhukinnisus, |
|
|
|
|
düspepsia, |
|
|
|
|
kõhupuhitus, |
|
|
|
|
oksendamine |
|
|
Maksa ja |
|
|
|
Maksaensüümide |
sapiteede häired |
|
|
|
aktiivsuse |
|
|
|
|
muutused/tõus, |
|
|
|
|
ikterus, hepatiit, |
|
|
|
|
maksakahjustus, äge |
|
|
|
|
maksapuudulikkus, |
|
|
|
|
vere |
|
|
|
|
bilirubiinisisalduse |
|
|
|
|
tõus* |
Naha ja |
|
Dermatiit, |
Allergilised |
|
nahaaluskoe |
|
hüperhidrooos, |
reaktsioonid, |
|
kahjustused |
|
lööve |
pruuritus, |
|
|
|
|
urtikaaria |
|
|
|
Lihasspasmid |
|
|
sidekoe |
|
|
|
|
kahjustused |
|
|
|
|
Neerude ja |
|
Düsuuria, |
Kusepakitsus |
|
kuseteede häired |
|
pollakisuuria, |
|
|
|
|
urineerimisraskus, |
|
|
|
|
kusepeetus |
|
|
Reproduktiivse |
|
Düsmenorröa, |
Ejakulatsiooni |
Priapism |
süsteemi ja |
|
ejakulatsiooni |
puudus, |
|
|
|
|
|
rinnanäärme |
|
häired, |
ebaregulaarne |
|
häired |
|
erektsioonihäired, |
menstruatsioon, |
|
|
|
prostatiit, |
ebanormaalne |
|
|
|
genitaalide valu |
orgasm |
|
|
|
meestel |
|
|
Üldised häired ja |
|
Asteenia, väsimus, |
Külmatunne, |
|
manustamiskoha |
|
letargia, |
valu rinnus (vt |
|
reaktsioonid |
|
külmavärinad, |
lõik 4.4) |
|
|
|
närviline olek, |
|
|
|
|
ärrituvus, janu |
|
|
Uuringud |
Vererõhu |
Kehakaalu langus |
|
|
|
tõus, |
|
|
|
|
pulsisageduse |
|
|
|
|
kiirenemine |
|
|
|
Siia kuulub ka ülakõhuvalu, ebamugavustunne maos, kõhuõõnes ja ülakõhus.
Siia kuulub algne, kesköine ja varajane (varahommikuse ärkamisega) unetus
Pulsisageduse ja vererõhu leiud põhinevad mõõdetud elulistel näitajatel
Siia kuuluvad anafülaktilised reaktsioonid ja angioneurootiline turse |
|
|
*Vt lõik 4.4
** Vt lõigud 4.4 ja 4.5.
CYP2D6 aeglased metaboliseerijad (AM)
Järgnevaid kõrvaltoimeid täheldati vähemalt 2
Võimalikest kõrvaltoimetest teavitamine
Ravimi võimalikest kõrvaltoimetest on oluline teavitada ka pärast ravimi müügiloa väljastamist. See võimaldab jätkuvalt hinnata ravimi kasu/riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest www.ravimiamet.ee kaudu.
4.9Üleannustamine
Sümptomid
Turuletulekujärgselt on teatatud atomoksetiini monoteraapia mitteletaalsetest ägedatest ja kroonilistest üleannustamistest. Ägedate ja krooniliste üleannustamistega kõige sagedamini kaasnevateks sümptomiteks on olnud gastrointestinaalsed sümptomid, unisus, pearinglus, treemor ja käitumishäired. Teatatud on ka hüperaktiivsusest ja agiteeritusest. Samuti täheldati sümpaatilise närvisüsteemi aktivatsiooniga seotud kergeid kuni mõõduka raskusega nähte (nt tahhükardia, vererõhu tõus, pupillide laienemine, suukuivus) ning on saadud teateid ka nahasügeluse ja
Seoses atomoksetiini üleannustamisega on kliiniline kogemus piiratud.
Ravi
Tuleb tagada vabad hingamisteed. Ühe tunni jooksul pärast üleannuse sisse võtmist võib olla kasu aktiveeritud söe manustamisest, et takistada ravimi imendumist. Soovitatav on kardiaalsete ja eluliste funktsioonide jälgimine ning sobivate sümptomaatiliste ja toetavate meetmete rakendamine. Patsienti tuleb jälgida vähemalt 6 tunni jooksul. Kuna atomoksetiin seondub suurel määral plasmavalkudega, siis dialüüsist üleannustamise ravis tõenäoliselt kasu ei ole.
5.FARMAKOLOOGILISED OMADUSED
5.1Farmakodünaamilised omadused
Farmakoterapeutiline rühm: psühhoanaleptikumid, tsentraalse toimega sümpatomimeetikumid
Toimemehhanism ja farmakodünaamilised toimed
Atomoksetiini toimemehhanism põhineb arvatavasti väga selektiivsel ja tugeval presünaptilise noradrenaliini transportija inhibeerimisel, ilma otsese mõjuta serotoniini või dopamiini transportijatele. Atomoksetiinil on minimaalne afiinsus teiste noradrenergiliste retseptorite või teiste neuromediaatorite transportijate või retseptorite suhtes. Atomoksetiinil on kaks peamist oksüdatiivset metaboliiti:
Atomoksetiin ei ole psühhostimulant ega amfetamiini derivaat. Täiskasvanutega läbiviidud randomiseeritud, topeltpimedas, platseebokontrollitud, kuritarvitamise potentsiaali uuringutes, milles võrreldi atomoksetiini toimeid platseeboga, ei tuvastatud atomoksetiinil sellist ravivastuse mudelit, mis oleks osutanud stimuleerivatele või euforiseerivatele omadustele.
Kliiniline efektiivsus ja ohutus
Lapsed
Strattera’t on uuritud uuringutes, mis hõlmasid üle 5000 lapse ja nooruki, kel esines ADHD. Strattera lühiajalist efektiivsust ADHD ravis hinnati esialgselt kuues randomiseeritud, topeltpimedas, platseebokontrollitud, kuue- kuni üheksanädalase kestusega uuringus. ADHD sümptomite hindamiseks võrreldi Strattera- ja
Lisaks tõestati
Strattera oli efektiivne nii ööpäevase üksikannusena kui ka kahe osaannusena, mida manustati hommikul ja hilisel pärastlõunal/varajasel õhtul. Õpetajate ja lapsevanemate hinnangust lähtuvalt kaasnes Strattera manustamisega üks kord ööpäevas statistiliselt oluliselt suurem ADHD sümptomite raskusastme vähenemine võrreldes platseeboga.
Aktiivsed võrdlusuuringud
Randomiseeritud, topeltpimedas, paralleelgruppidega,
Täiskasvanud
Strattera’t on uuritud kliinilistes uuringutes üle
Tabel X Efektiivsuse näitajate keskmised muutused platseebokontrolliga uuringutes
|
|
|
Muutused võrreldes algväärtusega vähemalt ühes algväärtuse järgses näitajas |
||||||
|
|
|
|
AAQoL |
|||||
|
|
|
|
AISRSA |
|||||
Uuring |
|
Ravi |
N |
Keskmine |
Keskmine |
Keskmine |
|||
|
|
|
|
muutus |
|
muutus |
|
muutus |
|
Akuutne |
|
|
|
|
|
|
|
|
|
uuring |
|
|
|
|
|
|
|
|
|
LYAA |
|
ATX |
0,006 |
0,011 |
- |
- |
|||
|
|
PBO |
|
|
|
|
|||
LYAO |
|
ATX |
0,002 |
0,002 |
- |
- |
|||
|
|
PBO |
|
|
|
|
|||
LYBY |
|
ATX |
0,007 |
0,048 |
- |
- |
|||
|
|
PBO |
|
|
|
|
|||
LYDQ |
|
ATX |
<0,001 |
0,022 |
14,9 |
0,030 |
|||
|
|
PBO |
|
|
11,1 |
|
|||
LYDZ |
|
ATX |
<0,001 |
<0,001 |
15,8 |
0,005 |
|||
|
|
PBO |
|
|
11,0 |
|
|||
LYEE |
|
ATX |
<0,001 |
<0,001 |
12,83 |
<0,001 |
|||
|
|
PBO |
|
|
8,20 |
|
|||
Pikaajaline |
|
|
|
|
|
|
|
||
uuring |
|
|
|
|
|
|
|
|
|
LYBV |
|
ATX |
0,412 |
0,173 |
13,90 |
0,045 |
|||
|
|
PBO |
|
|
11,18 |
|
|||
LYCU |
|
ATX |
0,005 |
0,001 |
13,14 |
0,004 |
|||
|
|
PBO |
|
|
8,62 |
|
|||
LYCW |
|
ATX |
<0,001 |
<0,001 |
- |
- |
|||
|
|
PBO |
|
|
|
|
|||
Lühendite tähendus: AAQoL = Täiskasvanute ADHD elukvaliteedi koguskoor; AISRS = Täiskasvanute ADHD uurija sümptomite hindamise skaala koguskoor; ATX = atomoksetiin;
versioon ADHD sümptomite koguskoor;
A ADHD sümptomite skaalad; tulemused, mis on näidatud uuringule LYBY on AISRS jaoks; tulemused kõikide teiste jaoks on
Tundlikkuse analüüsis, kus patsientidel, kellel ei tehtud algtasemejärgset hindamist (st kõik ravitud patsiendid), kasutati
Kliiniliselt olulise ravivastuse analüüsis kõigis 6 akuutses uuringus ja mõlemas edukas pikaajalises uuringus, kus kasutati mitmeid a priori ja post hoc definitsioone, täheldati atomoksetiiniga ravitud patsientidel püsivalt statistiliselt oluliselt kõrgemat ravivastuse määra võrreldes platseebot saanud patsientidega (Tabel Y).
Tabel Y Patsientide arv (n) ja protsent, kes vastasid ühendatud platseebokontrolliga uuringute ravivastuse kriteeriumitele
|
|
Ravivastus, mis on määratletud |
Ravivastus, mis on määratletud |
||||
|
|
paranemisega vähemalt ühes |
|||||
|
|
|
|
40% paranemisega |
|||
Grupp |
Ravi |
N |
n (%) |
N |
n (%) |
||
Ühendatud akuutsed |
|
|
|
|
|
|
|
uuringudA |
|
|
|
|
|
|
|
|
ATX |
401 (62,7%) |
<0,001 |
347 (41,3%) |
<0,001 |
||
|
PBO |
283 (43,4%) |
|
215 (25,3%) |
|
||
Ühendatud pikaajalised |
|
|
|
|
|
|
|
uuringud |
|
|
|
|
|
|
|
|
ATX |
482 (63,6%) |
<0,001 |
292 (44,0%) |
<0,001 |
||
|
PBO |
301 (49,3%) |
|
175 (31,4%) |
|
||
A sisaldab kõiki Tabelis X olevaid uuringuid, va: Akuutne
Kahes nendest akuutsetest uuringutest uuriti ADHD ja kaasuva alkoholismi või sotsiaalse ärevushäirega patsiente ja mõlemas uuringus täheldati ADHD sümptomite paranemist. Uuringus kaasuva alkoholi kuritarvitamisega patsientidega puudus erinevus atomoteksiini ja platseebogruppide vahel alkoholi tarbimiskäitumise suhtes. Uuringus kaasuva ärevushäirega patsientidega kaasuv ärevusseisund atomoksetiinravi foonil ei ägenenud.
Atomoksetiini efektiivsust sümptomite allumise säilitamisel näidati uuringus, kus pärast
QT/QTc uuring
Põhjalikus QT/QTc uuringus, mis viidi läbi tervete täiskasvanutega, kes olid aeglased CYP2D6 metaboliseerijad (AM), manustati kuni 60 mg atomoksetiini kaks korda ööpäevas. Näidati, et maksimaalse oodatava kontsentratsiooni korral ei erinenud atomoksetiini toime
5.2Farmakokineetilised omadused
Atomoksetiini farmakokineetika lastel ja noorukitel on sarnane täiskasvanute omaga. Atomoksetiini farmakokineetikat ei ole uuritud alla 6 aasta vanustel lastel.
Farmakokineetilised uuringud näitavad, et atomoksetiini kapslid ja suukaudne lahus on bioekvivalentsed.
Imendumine: Atomoksetiin imendub pärast suukaudset manustamist kiiresti ja peaaegu täielikult, kusjuures keskmine maksimaalne tuvastatud kontsentratsioon plasmas (CMAX) saabub ligikaudu 1...2 tundi pärast manustamist. Atomoksetiini absoluutne biosaadavus pärast suukaudset manustamist on 63 %...94 %, sõltuvalt individuaalsest erinevusest üldiselt vähese esmase maksapassaži osas. Atomoksetiini võib manustada söögiajast sõltumatult.
Jaotumine: Atomoksetiin jaotub ulatuslikult ning seondub suurel määral (98 %) plasmavalkude, peamiselt albumiiniga.
Biotransformatsioon: Atomoksetiin allub biotransformatsioonile, peamiselt tsütokroom P450 2D6 (CYP2D6) ensümaatilist rada pidi. 7
Tsütokroom P450 ensüümid: Atomoksetiin ei põhjustanud tsütokroom P450 ensüümide, sh CYP1A2, CYP3A, CYP2D6 ja CYP2C9, kliiniliselt olulist inhibeerimist ega indutseerimist.
Eritumine: Atomoksetiini keskmine eliminatsiooni poolväärtusaeg pärast suukaudset manustamist on kiiretel metaboliseerijatel 3,6 tundi ja aeglastel metaboliseerijatel 21 tundi. Atomoksetiin eritub peamiselt
Lineaarsus/mittelineaarsus: nende annuste ulatuses, mida on uuritud nii kiiretel kui aeglastel metaboliseerijatel, on atomoksetiini farmakokineetika lineaarne.
Eripopulatsioonid
Maksakahjustuse korral on atomoksetiini kliirens vähenenud, süsteemne ekspositsioon suurenenud (AUC suureneb mõõduka maksakahjustuse korral 2 korda ja raske maksakahjustuse korral 4 korda), ning eelravimi poolväärtusaeg - võrreldes tervete vabatahtlikega, kellel on CYP2D6 kiire metabolismi genotüüp sarnane - pikenenud. Mõõduka kuni raske maksakahjustusega (Child Pugh B ja C klass) patsientidel on vaja alg- ja lõplikku annust kohandada (vt lõik 4.2).
Lõppstaadiumis neeruhaigusega (ESRD) patsientidel on atomoksetiini keskmised plasmakontsentratsioonid üldiselt kõrgemad kui tervetel isikutel saadud keskmised kontrollväärtused, näidates Cmax (7% erinevus) ja
kohandamist vastavalt kehakaalule olid gruppidevahelised erinevused minimaalsed. Atomoksetiini ja tema metaboliitide farmakokineetika lõppstaadiumis neeruhaigusega patsientidel viitab asjaolule, et annust ei ole vaja kohandada (vt lõik 4.2).
5.3Prekliinilised ohutusandmed
Farmakoloogilise ohutuse, korduvtoksilisuse, genotoksilisuse, kartsinogeensuse või reproduktsioonitoksilisuse traditsioonilised prekliinilised uuringud ei ole näidanud kahjulikku toimet inimesele. Seoses annuse piirangutega, mida on tinginud kliiniline (või ülemäärane farmakoloogiline) vastus ravimile loomadel koos metaboolsete erinevustega liikide lõikes, kutsusid mittekliinilistes uuringutes kasutatud maksimaalsed talutavad annused loomadel esile tsirkuleeriva atomoksetiini koguse, mis oli samasugune või veidi suurem kui see, mille saavutavad aeglased CYP2D6 metaboliseerijad maksimaalse soovitatava ööpäevase annuse korral.
Hindamaks atomoksetiini toimet kasvule ning neurokäitumuslikule ja seksuaalsele arengule, viidi läbi uuring noorte rottidega. Täheldati kerget hilinemist tupe arengus (kõigi annuste korral) ja eesnaha eraldumises (≥ 10 mg/kg/ööpäevas) ning vähest munandimanuste kaalu ja spermatosoidide arvu langust (≥ 10 mg/kg/ööpäevas), kuid ei avastatud toimeid sigivusele ega reproduktiivsele funktsioonile. Nende leidude tähtsus inimesele ei ole teada.
Tiineid küülikuid raviti atomoksetiini annustega kuni 100 mg/kg/ööpäevas, mida manustati makku kunstliku toitmise sondi kaudu kogu organogeneesi perioodil. Selle annuse puhul täheldati 1 uuringus kolmest, loote elulemuse vähenemist, varajase resorptsiooni sagenemist, unearteri ebatüüpilise lähtekoha ning rangluualuse arteri puudumise vähest sagenemist. Neid leide tuvastati selliste annuste korral, mis põhjustasid emal kerget toksilisust. Nende leidude esinemissagedus jäi varasemate kontrollväärtuste piiridesse. Neid leide mittepõhjustav annus oli 30 mg/kg/ööpäevas. Seondumata atomoksetiini AUC küülikutel oli annuse 100 mg/kg/ööpäevas puhul ligikaudu 3,3 korda (CYP2D6 kiiretel metaboliseerijatel) ja 0,4 korda (CYP2D6 aeglastel metaboliseerijatel) suurem kui inimestel, kes on saanud maksimaalse ööpäevase annuse 1,4 mg/kg/ööpäevas. Kolmest
6.FARMATSEUTILISED ANDMED
6.1Abiainete loetelu
Naatriumbensoaat (E211)
Naatriumdivesinikfosfaatdihüdraat
Lahjendatud fosforhape
Vedel (kristalliseeruv) sorbitool (E420)
Ksülitool
Kunstlik vaarika maitseaine
Sukraloos
Naatriumhüdroksiid (pH korrigeerimiseks)
Puhastatud vesi
6.2Sobimatus
Ei kohaldata.
6.3Kõlblikkusaeg
2 aastat
Kõlblikkusaeg pärast esmast avamist: 45 päeva
6.4Säilitamise eritingimused
See ravimpreparaat ei vaja säilitamisel eritingimusi.
6.5Pakendi iseloomustus ja sisu
Merevaigukollasest klaasist lapsekindla turvakorgiga pudel sisaldab 100 ml lahust. Pakendis on ka annustamise seade, mis koosneb 10 ml suusüstlast, mis on gradueeritud 1 ml kaupa ja pudeli kaelale surutavast LDPE adapterist.
Turustatakse 1 pudeliga pakendeid ja kolme pudeliga multipakendit. Kõik pakendi suurused ei pruugi olla müügil.
6.6Erihoiatused ravimpreparaadi hävitamiseks
Atomoksetiinil on silma ärritav toime. Suukaudse lahuse silma sattumisel tuleb kahjustatud silma kohe veega loputada ning küsida meditsiinilist nõuannet. Käsi ja saastunud pindu, mis võivad olla kokku puutunud atomoksetiiniga, tuleb esimesel võimalusel pesta.
7.MÜÜGILOA HOIDJA
Eli Lilly Holdings Limited Lilly House,
Priestley Road,
Basingstoke,
RG24 9NL Ühendkuningriik
8.MÜÜGILOA NUMBER
9.ESMASE MÜÜGILOA VÄLJASTAMISE/MÜÜGILOA UUENDAMISE KUUPÄEV
Müügiloa esmase väljastamise kuupäev: 03.12.2014
10.TEKSTI LÄBIVAATAMISE KUUPÄEV
juuni 2015
Täpne teave selle ravimpreparaadi kohta on kättesaadav Ravimiameti kodulehel.
