Eileen - transdermaalne plaaster (0,06mg +0,013mg 24h) - Ravimi omaduste kokkuvõte
Artikli sisukord
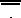
 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest. Kõrvaltoimetest teavitamise kohta vt lõik 4.8.
Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest. Kõrvaltoimetest teavitamise kohta vt lõik 4.8.
RAVIMI OMADUSTE KOKKUVÕTE
1. RAVIMPREPARAADI NIMETUS
Eileen 60 mikrogrammi/13 mikrogrammi/24 tunnis transdermaalne plaaster
2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS
Üks 11 cm2 transdermaalne plaaster sisaldab 2,10 mg gestodeeni ja 0,55 mg etünüülöstradiooli.
Üks transdermaalne plaaster vabastab 24 tunni jooksul 60 mikrogrammi gestodeeni ja 13 mikrogrammi etünüülöstradiooli (vastab suukaudsele annusele 20 mikrogrammi). INN. Gestodenum, ethinylestradiolum
Abiainete täielik loetelu vt lõik 6.1.
3. RAVIMVORM
Transdermaalne plaaster.
Viiest kihist koosnev õhuke maatriksi tüüpi transdermaalne plaaster.
Plaaster on ümmargune, läbipaistev ja suurusega 11 cm. Plaastri kleepuvat poolt katab kaheosaline ruudukujuline läikiv värvitu kaitsekile.
4. KLIINILISED ANDMED
4.1Näidustused
Raseduse hormonaalne vältimine naistel.
Ravim on näidustatud fertiilses eas, selle ohutus ja efektiivsus on tõestatud
Preparaadi väljakirjutamisel tuleb võtta arvesse konkreetsel naisel käesoleval hetkel esinevaid riskifaktoreid, eriti venoosse trombemboolia (VTE) riskifaktoreid ning VTE riski selle ravimiga, võrreldes teiste kombineeritud hormonaalsete kontratseptiividega (KHKdega) (vt lõigud 4.3 ja 4.4).
4.2Annustamine ja manustamisviis
Annustamine
Eileen’t kasutatakse
Kolmel järjestikusel nädalal (21 päeva) pannakse igal nädalal nahale üks uus plaaster ning eemaldatakse kasutatud plaaster. Neljas nädal on plaastrivaba. Sellel ajal algab eeldatavalt menstruatsioonilaadne veritsus. Nädal aega pärast viimase plaastri eemaldamist alustatakse uue 4- nädalase tsükliga. Selleks asetatakse nahale uus plaaster (samal nädalapäeval nagu ennegi, nn
„plaastri vahetamise päeval“), sõltumata sellest, kas tavapärane menstruatsioonilaadne veritsus on lõppenud või mitte. Juhul kui tavapärast menstruatsioonilaadset veritsust ei teki, vt lõigu 4.4 alalõiku “Menstruaaltsüklit reguleeriva toime vähenemine”. Täpset plaastri peale panemise/eemaldamise skeemi vt lõigu 4.2 alalõigust “Kuidas Eileen´t kasutada”.
Millal Eileen’ga esimest korda alustada
•Varem (eelmisel kuul) ei ole kasutatud hormonaalset kontratseptiivi
Plaaster tuleb nahale asetada naise loomuliku tsükli esimesel päeval (st menstruatsiooni esimesel päeval). Võib alustada ka 2...5. päeval, kuid sel juhul tuleb esimese tsükli plaastri kandmise esimese
•Üleminek kombineeritud hormonaalselt kontratseptiivilt (kombineeritud suukaudne kontratseptiiv (KSK), tuperõngas või mõni teine transdermaalne plaaster)
Plaaster tuleks soovitatavalt peale panna päev pärast viimase hormooni sisaldava kombineeritud suukaudse kontratseptiivi võtmist, kuid hiljemalt päeval pärast KSK tavapärast tabletivaba või platseebotablettide perioodi.
Tuperõnga või muu transdermaalse plaastri kasutamisel peab naine plaastri nahale asetama tsüklipaki viimase rõnga või plaastri eemaldamise päeval, kuid hiljemalt ajal, mil peaks toimuma järgmine kasutamine.
•Üleminek ainult progestageeni sisaldavalt meetodilt (ainult progestageeni sisaldav pill, süst, implantaat) või progestageeni vabastavalt emakasiseselt ravivahendilt
Naine võib ainult progestageeni sisaldavalt pillilt üle minna mis tahes päeval (implantaadilt või emakasiseselt ravivahendilt selle eemaldamise päeval; süstitavalt vahendilt päeval, mil peaks toimuma järgmine süstimine). Kõikidel nendel juhtudel tuleb soovitada naisel kasutada täiendavalt barjäärimeetodit esimese plaastri kandmise seitsmel päeval.
•Pärast esimesel trimestril tehtud aborti
Naine võib alustada kohe. Sellisel juhul ei pea ta kasutama täiendavaid rasestumisvastaseid vahendeid.
•Pärast sünnitust või teisel trimestril tehtud aborti
Naistel tuleb soovitada plaastri kasutamist alustada 21…28. päeval pärast sünnitust või teisel trimestril tehtud aborti. Hilisemal alustamisel tuleb naisele soovitada täiendava barjäärimeetodi kasutamist esimese plaastri esimesel seitsmel päeval. Kui seksuaalvahekord on siiski juba toimunud, tuleb enne Eileen kasutamist välistada rasedus või oodata ära esimene menstruatsioon.
Teavet rinnaga toitvate naiste kohta, vt lõik 4.6.
Kuidas Eileen’t kasutada
Eileen’t kasutatakse
•Plaastri vahetamise päev
Iga uus plaaster tuleb nahale panna samal nädalapäeval. Seda päeva nimetatakse „plaastri vahetamise päevaks“. Näiteks kui esimene plaaster pandi nahale pühapäeval, tuleb kõik järgnevad plaastrid panna nahale pühapäeviti. Samaaegselt võib nahal olla ainult üks plaaster.
1. plaaster |
1. päev: 1. plaastri nahale panemine (Eileen´t esimest korda kasutavate naiste |
|
kohta vt lõik “Millal Eileen’ga esimest korda alustada”) |
2. plaaster |
8. päev: 1. plaastri eemaldamine ja kohene 2. plaastri nahale panemine |
3. plaaster |
15. päev: 2. plaastri eemaldamine ja kohene 3. plaastri nahale panemine |
Ilma plaastrita |
22. päev: 3. plaastri eemaldamine (22…28. päeval plaastrit ei kasutata) |
Plaastri eemaldamine toimub alati samal nädalapäeval (nn plaastri vahetamise päeval). Sellel päeval võib plaastrit vahetada mis tahes kellaajal. Järgnevaid tsükleid alustatakse samal plaastri vahetamise päeval, pärast
•Plaastrivabad päevad
Plaastrit ei kanta 22. päevast (pärast 3. plaastri eemaldamist) kuni 28. päevani (neljas nädal).
Ühelgi juhul ei tohi tsüklitevaheline plaastrivaba periood olla pikem kui 7 päeva.
Kui plaastrivabu päevi on rohkem kui seitse, EI PRUUGI NAINE OLLA RASESTUMISE EEST KAITSTUD. Uut tsüklit tuleb alustada (uue plaastri nahale asetamisega) niipea, kui naine märkab uue tsükli alustamise unustamist; järgmise seitsme päeva vältel tuleb sel juhul kasutada täiendavat rasestumisvastast vahendit (nt kondoom, spermitsiid või tupepessaar). Sarnaselt kombineeritud suukaudsetele kontratseptiividele suureneb ovulatsioonirisk iga päevaga, mis lisandub soovitatavale ravimivabale perioodile.
Juhul, kui sellisel pikemaajalisel plaastrivabal perioodil on toimunud seksuaalvahekord, tuleb arvestada võimaliku rasedusega.
Vt ka lõiku “Mida teha lahti tulnud, ununenud või vahetamata jäänud plaastri korral”.
Manustamisviis
Manustamistee: transdermaalne
Kuhu plaaster kinnitada
Plaaster tuleb kinnitada ühele järgmistest kasutuskohtadest (vt allolevat joonist): kõht, tuharad, õlavarre välimine külg.
Vältida tuleb piirkondi, kust plaaster võib ära tulla (nt vöökoht).
Plaaster tuleb kanda puhtale, kuivale, vigastamata, tervele ja eelistatult raseeritud nahale.

Eileen’t ei tohi kinnitada rasusele, punetavale, ärritunud, kriimustatud või muul moel kahjustatud nahale.
Plaastrit ei tohi panna rindadele.
Vältimaks Eileen kleepuvuse vähenemist ei tohi plaastri kinnitamise kohale kanda jumestusvahendeid, kreeme, ihupiima, pulbreid ega muid paikseid nahahooldusvahendeid.
Plaastri kinnitamise kohtasid tuleb vahetada. Selleks võib kasutada sama kasutuskoha erinevaid piirkondi. Nt võib naine panna plaastri vaheldumisi kõhu vasakule ja paremale küljele või paremale ja vasakule tuharale/õlavarrele.
Naine võib kasutada igal nädalal ka erinevat manustamiskohta (nt ühel nädalal õlavarre välisküljel, järgmisel nädalal kõhul).
Naine peab plaastrit iga päev visuaalselt kontrollima, veendumaks et see on korralikult nahale kinnitunud.
Pidage meeles järgmist
•Samaaegselt võib nahal olla ainult üks plaaster.
•Kui plaaster on kinnitatud nõuetekohaselt, saab naine käia tavapäraselt vannis või duši all.
•Läbipaistev plaaster on ultraviolett- ja päikesekiirguse eest kaitstud. Seetõttu ei pea plaastrit katma riietega, vaid see võib olla päikese käes.
Nahaärrituse tekkimine
Kui plaastri kasutamine põhjustab selle manustamiskohal ebamugavat ärritust, tuleb plaaster eemaldada. Uus plaaster tuleb panna teise asukohta. Seda uut plaastrit kasutatakse järgmise plaanipärase plaastri vahetamise päevani.
Kuidas plaastrit nahale kandmiseks ette valmistada
Eileen on karbis, mis sisaldab brošüüri ja lisaks kas 3, 9 või 18 suletud kotikest, millest igaühes on üks Eileen transdermaalne plaaster.
Plaaster on ümmargune ja läbipaistev.
Plaastri kleepuvat poolt katab kaheosaline ruudukujuline läikiv värvitu kaitsekile. See kile kaitseb plaastri kleepuvat poolt, mis sisaldab toimeaineid. Samuti tagab kaitsekile ka plaastri kleepuvuse kuni selle nahale kandmise ajani.
Plaastri teine pool on kaetud piimjasvalge ruudukujulise kattelehega, mis ei lase plaastril kotikese seinte külge kleepuda.
Ümmargune läbipaistev plaaster koos kaheosalise ruudukujulise läikiva värvitu kaitsekilega
Piimjasvalge ruudukujuline katteleht
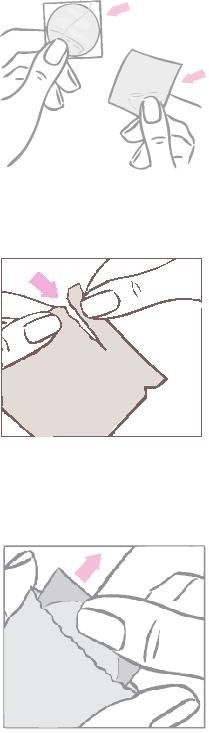
Naine peab avamiseks kotikese ülemise otsa sõrmedega lahti rebima. Sälgud hõlbustavad rebimist. Avamiseks ei tohi kasutada kääre, samuti ei tohi plaastrit lõigata, kahjustada või muuta, sest see võib vähendada Eileen rasestumisvastast toimet.
Ümmargune kontratseptiivne plaaster on kaheosalise ruudukujulise läikiva värvitu kaitsekile ja piimjasvalge ruudukujulise kattelehe vahel. Oluline on plaaster kotikesest välja võtta koos värvitu kaitsekile ja piimjasvalge kattelehega. Kotikest ei tohi ära visata, seda tuleb alles hoida plaastri ära viskamiseks pärast kasutamist.
Pärast kotikese avamist tuleb plaaster vastavalt allpool toodud juhistele kohe nahale kinnitada. Kõigepealt tuleb eemaldada plaastri pealmiselt poolelt üheosaline piimjasvalge ruudukujuline katteleht.
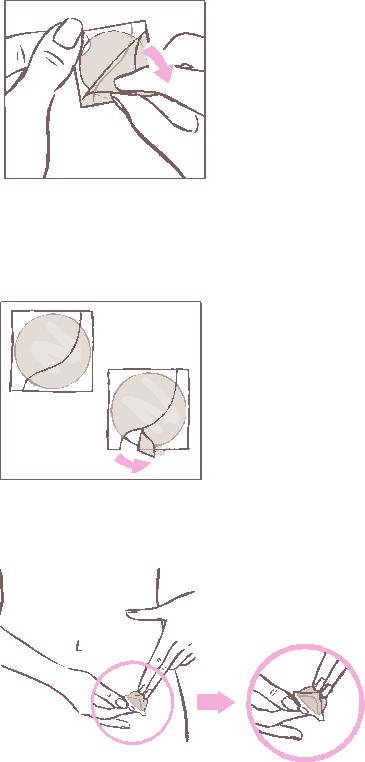
Pärast plaastrilt eemaldamist tuleb piimjasvalge ruudukujuline katteleht (hoiab ära plaastri kleepumise kotikese seintele) ära visata.
Seejärel tuleb eemaldada pool kaheosalisest ruudukujulisest läikivast värvitust kaitsekilest, mis katab ümmarguse läbipaistva plaastri alumist kleepuvat poolt (kleepuv pool sisaldab toimeaineid). Kleepuvuse säilitamiseks tuleb vältida plaastri kleepuva pinna puudutamist.
Hoides plaastrit kinni servast, mida katab veel kaitsekile teine pool, tuleb plaaster paigutada nahal kohale, kus seda kandma hakatakse.
Kui pool plaastrist on õrnalt kasutuskohale kinnitunud, tuleb eemaldada kaitsekile teine pool.
Plaastrit tuleb 30 sekundi vältel tugevalt peopesaga vastu nahka suruda ja veenduda, et plaastri servad on kindlalt vastu nahka kleepunud.
Märkus: kotikest ei tohi ära visata, sest seda on pärast vaja kasutatud plaastri ära viskamiseks.
Plaastrite hävitamine
Vt lõik 6.6.
Mida teha lahti tulnud, ununenud või vahetamata jäänud plaastri korral
Plaastri
•Kui plaaster on osaliselt või täielikult naha küljest lahti
vähem kui ühe päeva vältel (kuni 24 tundi)
Naine peab püüdma seda kohe uuesti kinnitada samale kohale või asendama lahti tulnud plaastri uuega. Täiendavate rasestumisvastaste vahendite kasutamine ei ole vajalik. Naise plaastri vahetamise päev jääb samaks.
kauem kui üks päev (24 tundi või kauem)
või kui naine ei tea täpselt, kui kaua on plaaster naha küljest lahti olnud
NAINE EI PRUUGI ENAM RASESTUMISE EEST KAITSTUD OLLA. Ta peab lõpetama käesoleva kontratseptiivse tsükli ja alustama kohe uut tsüklit, pannes nahale uue plaastri. Nüüd on uus 1. päev ja uus plaastri vahetamise päev. Uue tsükli esimesel nädalal tuleb kasutada täiendavaid rasestumisvastaseid vahendeid (nt kondoom, spermitsiid või tupepessaar).
Plaastrit ei tohi uuesti nahale kinnitada, kui see ei ole enam kleepuv, kui see on omavahel või mõne muu pinna külge kleepunud, kui sinna külge on kleepunud muud materjali või kui plaaster on eelnevalt lahti tulnud või ära kukkunud. Kui plaastrit ei saa uuesti nahale kinnitada, tuleb viivitamatult nahale kanda uus plaaster. Eileen paigalhoidmiseks ei tohi kasutada muid adhesiivseid aineid või sidemeid.
•Kui naine unustab plaastrit vahetada
mis tahes plaastritsükli alguses (1. nädal / 1. päev)
NAINE EI PRUUGI ENAM RASESTUMISE EEST KAITSTUD OLLA. Ta peab uue tsükli esimese plaastri nahale kinnitama niipea kui see talle meenub. Nüüd on uus plaastri vahetamise päev ja uus 1. päev. Uue tsükli esimesel nädalal peab naine kasutama täiendavaid rasestumisvastaseid vahendeid (nt kondoom, spermitsiid või tupepessaar).
plaastritsükli keskel (2. nädal / 8. päev või 3. nädal / 15. päev)
ühe või kahe päeva jooksul (kuni 48 tundi)
Kohe tuleb nahale kinnitada uus plaaster. Järgmine plaaster tuleb nahale panna tavapärasel plaastri vahetamise päeval. Täiendavate rasestumisvastaste vahendite kasutamine ei ole vajalik.
rohkem kui kahe päeva jooksul (48 tundi või kauem)
NAINE EI PRUUGI ENAM RASESTUMISE EEST KAITSTUD OLLA. Ta peab lõpetama käesoleva kontratseptiivse tsükli ja alustama kohe uut
Naine peab ühe nädala vältel kasutama täiendavaid rasestumisvastaseid vahendeid.
plaastritsükli lõpus (4. nädal / 22. päev)
Kui naine unustab 22. päeval plaastri eemaldada, peab ta selle eemaldama niipea, kui see talle meenub (hiljemalt 28. päeval). Seejärel tuleb uut tsüklit alustada uue plaastriga (päeval pärast 28. päeva – tavalisel plaastri vahetamise päeval, mitte hiljem). Täiendavate rasestumisvastaste vahendite kasutamine ei ole vajalik.
•Plaastri lahtitulemise, unustamise või mitteasendamise tagajärjed ja nõutavad toimingud
Plaastri lahtitulemise, unustamise või mitteasendamise tagajärjed ja nõutavad toimingud
Lahtitulnud |
Ajavahemik |
Mõju |
Nõutav toimingA |
plaastridA |
|
kontratseptiivsele |
|
|
|
toimeleA |
|
Plaaster on lahti |
< 24 tundi |
Kontratseptiivne |
- Asetage nahale kohe uus plaaster |
tulnud |
|
efektiivsus on |
- Täiendavate rasestumisvastaste |
|
|
tagatud |
vahendite kasutamine ei ole vajalik |
|
|
|
- Plaastri vahetamise päev ei muutu |
|
> 24 tundi |
Kontratseptiivne |
- Alustage kohe uut |
|
|
efektiivsus on |
asetades nahale uue plaastri |
|
|
vähenenud |
- Kasutage järgmise seitsme päeva vältel |
|
|
|
täiendavaid rasestumisvastaseid |
|
|
|
vahendeidB |
|
|
|
- Märkige üles uus plaastri vahetamise |
|
|
|
päev |
Plaastreid ei |
Ajavahemik |
Mõju |
Nõutav toimingA |
vahetata õigeaegseltA |
|
kontratseptiivsele |
|
|
|
toimeleA |
|
1. plaastrit |
Plaastrivaba |
Kontratseptiivne |
- Alustage kohe uut |
(1. nädal, 1. päev) |
perioodD |
efektiivsus on |
asetades nahale uue plaastri |
ei pandud peale |
> 7 päeva |
vähenenud |
- Kasutage järgmise seitsme päeva vältel |
õigeaegselt |
|
|
täiendavaid rasestumisvastaseid |
|
|
|
vahendeidB |
|
|
|
- Märkige üles uus plaastri vahetamise |
|
|
|
päev |
1. või 2. plaastrit |
< 48 tundi |
Kontratseptiivne |
- Asetage nahale kohe uus plaaster |
(1./2. või 2./3. nädal) |
|
efektiivsus on |
- Täiendavate rasestumisvastaste |
ei asendatud |
|
tagatud |
vahendite kasutamine ei ole vajalik |
õigeaegselt |
|
|
- Plaastri vahetamise päev ei muutu |
|
|
> 48 tundi |
Kontratseptiivne |
- Alustage kohe uut |
|
|
|
efektiivsus on |
asetades nahale uue plaastri |
|
|
|
vähenenud |
- Kasutage järgmise seitsme päeva vältel |
|
|
|
|
täiendavaid rasestumisvastaseid |
|
|
|
|
vahendeidB |
|
|
|
|
- Märkige üles uus plaastri vahetamise |
|
|
|
|
päev |
3. plaastrit |
|
Kontratseptiivne |
- Eemaldage plaaster |
|
(3./4. nädal) |
|
efektiivsus on |
- Alustage järgmist |
|
ei eemaldatud |
|
tagatudC |
tavapärasel plaastri vahetamise päeval |
|
õigeaegselt |
|
|
|
|
• |
A Kohaldub igale tsüklile. |
|
|
|
• |
B Täiendav rasestumisvastane vahend on mis tahes täiendav mittehormonaalne rasestumisvastane |
|||
|
meetod, v.a kalendrimeetod ja temperatuurimeetod. |
|
||
• |
C Eeldusel, et 3. plaaster on uue vastu vahetatud hiljemalt uue plaastritsükli tavapärasel 1. päeval. |
|||
• |
D Aeg eelmise tsükli viimase plaastri eemaldamisest. |
|
||
Kindlustamaks, et naisel ei saa plaastrid otsa, tuleb retsept järgmise pakendi ostuks soetada õigeaegselt, st enne pakendi viimase plaastri kasutamist.
Plaastri vahetamise päeva muutmine
Kui naine soovib muuta plaastri vahetamise päeva, peab ta oma käesoleva tsükli lõpuni tegema, eemaldades kolmanda plaastri õigel päeval. Plaastrivabal nädalal võib ta valida varasema plaastri vahetamise päeva, asetades uue plaastri nahale soovitud nädalapäeval. Ühelgi juhul ei tohi olla enam kui seitse järjestikust plaastrivaba päeva.
Erirühmad
Sugu
Eileen on näidustatud kasutamiseks ainult naistele.
Eakad naised
Ei ole asjakohane. Eileen ei ole näidustatud kasutamiseks pärast menopausi.
Kehamassiindeks
Andmeid kontratseptiivse efektiivsuse kohta naistel kehamassiindeksiga ≥ 30 kg/m2 on piiratud hulgal.
Neerufunktsiooni kahjustus
Eileen’t ei ole uuritud neerufunktsiooni kahjustusega naistel. Eeldatavalt ei ole neerufunktsiooni kahjustusega naistel suuremat riski (vt lõik 5.2).
Maksafunktsiooni kahjustus
Eileen’t ei ole maksakahjustusega naistel uuritud. Eileen on vastunäidustatud naistele, kellel on või on varem olnud tõsine maksahaigus, kui maksafunktsiooni näitajad ei ole normaliseerunud. Vt ka
lõik 4.3.
Etnilised erinevused
Etünüülöstradiooli farmakokineetikat uuriti kombinatsioonis teise progestiiniga europiididel, Hiina ja Jaapani naistel. Ühtegi kliiniliselt olulist erinevust ei ilmnenud. Eileen farmakokineetikat ei ole eraldi uuritud erineva etnilise taustaga naistel. Ei ole teada ühtegi polümorfset ensüümi, mis osaleksid suurel määral gestodeeni metaboliseerimises. Olemasolevad andmed europiidide, mustanahaliste ja hispaanlannade kohta ei osuta ühelegi erinevusele Eileen farmakokineetikas erinevasse rassi või etnilisse tausta kuuluvate naiste puhul. Asiaatide kohta on andmeid väga piiratud hulgal.
Lapsed
Ohutus ja efektiivsus alla
4.3Vastunäidustused
•Venoosne trombemboolia (VTE) või selle tekkerisk
O Venoosne trombemboolia – käesolev
süvaveenitromboos või kopsuemboolia).
OTeadaolev pärilik või omandatud eelsoodumus venoosse trombemboolia tekkeks, nt aktiveeritud
OSuurem kirurgiline protseduur koos pikaajalise liikumatusega (vt lõik 4.4).
OMitme riskifaktori esinemisest tingitud venoosse trombemboolia kõrge risk (vt lõik 4.4).
•Arteriaalne trombemboolia (ATE) või selle tekkerisk
OArteriaalne trombemboolia - käesolev või anamneesis (nt müokardiinfarkt) või selle eelne seisund (nt stenokardia).
OTserebrovaskulaarne haigus – insult praegu või anamneesis või selle eelne seisund (nt mööduv isheemiline atakk).
OTeadaolev pärilik või omandatud eelsoodumus arteriaalse trombemboolia tekkeks, nt hüperhomotsüsteineemia ja fosfolipiidivastased antikehad (kardiolipiinivastased antikehad, luupusantikoagulant).
OVarem esinenud koldeliste neuroloogiliste sümptomitega migreen.
OKõrge risk arteriaalse trombemboolia tekkeks mitme riskifaktori esinemise tõttu (vt lõik 4.4) või kui esineb üks tõsine riskifaktor näiteks:
•vaskulaarsete sümptomitega suhkurtõbi;
•raske hüpertensioon;
•raske düslipoproteineemia.
•Raske maksahaiguse olemasolu või varasem esinemine, kui maksafunktsiooni näitajad ei ole normaliseerunud.
•Maksakasvajate (hea- või pahaloomulised) olemasolu või varasem esinemine.
•Suguhormoonidest sõltuvate kasvajate (nt suguorganite kasvaja või rinnanäärmevähk) olemasolu või selle kahtlus.
•Ebaselge põhjusega vaginaalne veritsus.
•Ülitundlikkus toimeainete või lõigus 6.1 loetletud mis tahes abiainete suhtes.
4.4 Erihoiatused ja ettevaatusabinõud kasutamisel
Hoiatused
Mis tahes allpool nimetatud seisundi või riskifaktori esinemisel tuleb Eileen’i sobivust arutada koos naisega. Naisele tuleb öelda, et nimetatud seisundite või riskifaktorite ägenemisel või esmakordsel ilmnemisel tuleb pöörduda oma arsti poole, et teha kindlaks, kas Eileen kasutamine tuleb katkestada.
•Vereringe häired
Venoosse trombemboolia (VTE) risk
Mis tahes kombineeritud hormonaalse kontratseptiivi (KHK) kasutamine suurendab venoosse trombemboolia (VTE) tekkeriski, võrreldes mittekasutamisega. Levonorgestreeli, norgestimaati või noretisterooni sisaldavad ravimid on madalaima VTE tekkeriskiga. Veel ei ole teada, kui suur
on Eileen risk võrreldes nende madalama riskiga preparaatidega. Otsus mis tahes ravimi kasutamise kohta, mis ei ole madalaima VTE tekkeriskiga, tuleb teha alles pärast naisega nõu pidamist, veendumaks, et ta mõistab Eileen kasutamisega seotud VTE tekkeriski; seda, kuidas tema olemasolevad riskifaktorid seda riski mõjutavad ja et tema VTE tekkerisk on kõige kõrgem esimesel kasutamisaastal. On olemas ka mõned tõendid selle kohta, et VTE risk suureneb ka
Naistel, kes ei kasuta
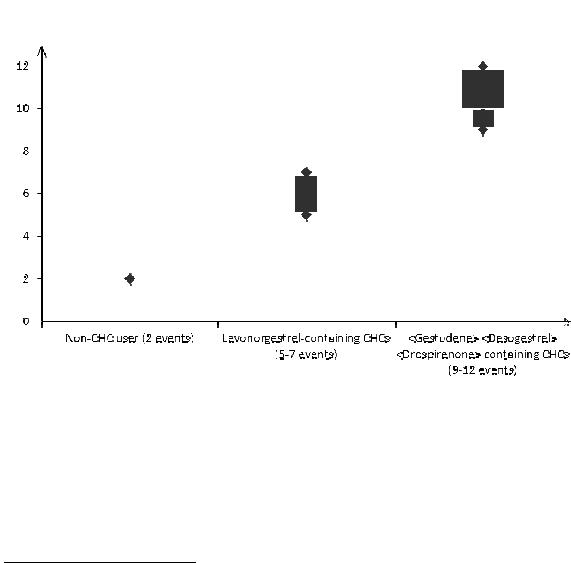
Hinnanguliselt1 tekib VTE ühe aasta jooksul 9...12 naisel 10
VTE juhtude arv aastas on mõlemal juhul väiksem, kui VTE eeldatav esinemissagedus raseduse ajal või sünnitusjärgsel perioodil.
Veel ei ole teada, kui suur on Eileen VTE risk võrreldes levonorgestreeli sisaldavate madala- annuseliste
VTE võib 1...2% juhtudest lõppeda surmaga.
VTE juhtude arv 10 000 naise kohta ühes aastas
VTE juhtude
juhtude arv
arv











|
Levonorgestreeli sisaldavad |
|
Gestodeeni sisaldavad |
|
(2 juhtu) |
|
(5…7 juhtu) |
|
(9…12 juhtu) |
|
|
|
|
|
|
|
|
|
|
Väga harva on
VTE riskifaktorid
KHK kasutajatel võib venoosse trombemboolia tüsistuste risk märkimisväärselt suureneda naistel, kellel esinevad täiendavad riskifaktorid, eriti, kui neid on mitu (vt tabel).
Eileen on vastunäidustatud, kui naisel on mitu riskifaktorit, mille tõttu on risk venoosse tromboosi tekkeks kõrge (vt lõik 4.3). Kui naisel on riskifaktoreid rohkem kui üks, võib riski suurenemine olla
1 Need juhud määratleti epidemioloogilise uuringu kõikide andmete alusel, kasutades erinevate ravimite suhtelisi riske võrrelduna levonorgestreeli sisaldavate
2 Levonorgestreeli sisaldavate
suurem kui üksikute riskifaktorite summa. Sellisel juhul tuleb arvestada naise VTE koguriskiga. Kui ravimi kasu/riski suhet peetakse negatiivseks, ei tohi
Tabel. VTE riskifaktorid
Riskifaktor |
Märkus |
Rasvumine (kehamassiindeks üle 30 kg/m²). |
KMI tõusuga suureneb risk märkimisväärselt. |
|
Eriti oluline on seda arvestada juhul, kui esineb ka |
|
teisi riskifaktoreid. |
Pikaajaline liikumatus, suurem kirurgiline |
Nendel juhtudel on soovitatav plaastri kasutamine |
protseduur, mis tahes jalgade või vaagnapiirkonna |
katkestada (plaanilise kirurgilise protseduuri korral |
operatsioon, neurokirurgia või ulatuslik trauma. |
vähemalt neli nädalat varem) ja mitte taasalustada |
|
enne, kui täielikust liikumisvõime taastumisest on |
|
möödunud kaks nädalat. Soovimatu raseduse |
|
vältimiseks tuleb kasutada muud rasestumisvastast |
|
vahendit. |
Märkus: ajutine liikumatus, sh lennureis kestusega |
|
üle 4 tunni, võib samuti olla VTE riskifaktoriks, |
Kui Eileen kasutamist ei ole eelnevalt katkestatud, |
eriti naistel, kellel esineb ka teisi riskifaktoreid. |
tuleb kaaluda tromboosivastast ravi. |
Esinemine perekonnas (venoosne trombemboolia |
Päriliku eelsoodumuse kahtluse korral tuleb enne |
õdedel/vendadel või vanematel, eriti just suhteliselt |
mis tahes KHK määramise otsust saata naine |
noores eas, nt enne 50. eluaastat). |
eriarsti konsultatsioonile. |
Teised |
Vähkkasvaja, süsteemne erütematoosluupus, |
|
|
|
põletikuline soolehaigus (Crohni tõbi või |
|
haavandiline koliit) ja sirprakuline aneemia. |
Vanuse tõus. |
Eriti üle 35 aasta. |
Puudub üksmeel varikoossete veenide ja pindmise tromboflebiidi võimaliku rolli kohta venoosse tromboosi tekkimisel või progresseerumisel.
Arvestada tuleb trombemboolia tekkeriski suurenemist raseduse ajal ja eriti 6 nädala vältel pärast sünnitust (teavet raseduse ja imetamise vt kohta lõigust 4.6).
VTE sümptomid (süvaveenitromboos ja kopsuemboolia)
Sümptomite ilmnemisel tuleb soovitada naistele kohest arsti poole pöördumist ja tervishoiutöötajate teavitamist sellest, et ta kasutab
Süvaveenitromboosi sümptomid võivad olla:
-ühepoolne jala ja/või jalalaba paistetus või paistetus piki jalaveeni;
-valu või tundlikkus jalas, mis võib tunda anda ainult seistes või kõndides;
-haige jala kõrgem temperatuur; jalanaha punetus või värvimuutus.
Kopsuemboolia sümptomid võivad olla:
-äkki tekkinud ebaselge põhjusega õhupuudus või kiire hingamine;
-äkki tekkinud köha, millega võib kaasneda veriköha;
-terav valu rindkeres;
-tugev peapööritus või pearinglus;
-kiire või ebakorrapärane südamerütm.
Mõned nendest sümptomitest (nt õhupuudus, köha) on mittespetsiifilised ja neid võidakse ekslikult tõlgendada tavalisemate või vähemtõsiste haigustena (nt hingamisteede nakkused).
Veresoone sulgusele viitavad teised nähud võivad olla jäseme äkiline valu, paistetus ja kergelt sinine värvus.
Kui veresoone sulgus tekib silmas, võivad sümptomid varieeruda valutust hägustunud nägemisest kuni nägemiskaotuseni. Mõnikord võib nägemiskaotus tekkida peaaegu kohe.
Arteriaalse trombemboolia (ATE) risk
Epidemioloogilised uuringud on seostanud
ATE riskifaktorid
Riskifaktoritega
Tabel. ATE riskifaktorid
Riskifaktor |
Märkus |
Vanuse tõus |
Eriti üle 35 aasta. |
Suitsetamine |
Naistel tuleb soovitada mitte suitsetada, kui nad |
|
soovivad kasutada |
|
kes jätkavad suitsetamist, tuleb tungivalt soovitada |
|
kasutada mõnda teist rasestumisvastast meetodit. |
Hüpertensioon |
|
Rasvumine (kehamassiindeks üle 30 kg/m) |
KMI tõusuga suureneb risk märkimisväärselt. |
|
Eriti oluline naistel, kellel esineb ka teisi |
|
riskifaktoreid. |
Esinemine perekonnas (arteriaalne |
Päriliku eelsoodumuse kahtluse korral tuleb enne mis |
trombemboolia õdedel/vendadel või |
tahes KHK määramise otsust saata naine eriarsti |
vanematel, eriti just suhteliselt noores eas, |
konsultatsioonile. |
nt enne 50. eluaastat) |
|
Migreen |
Migreeni esinemissageduse või raskusastme |
|
suurenemine (mis võib olla tserebrovaskulaarse häire |
|
varajaseks sümptomiks) KHK kasutamise ajal võib |
|
olla ravimi kasutamise kohese katkestamise |
|
põhjuseks. |
Teised vaskulaarsete häiretega seotud |
Suhkurtõbi, hüperhomotsüsteineemia, südameklapi |
haigusseisundid |
kahjustus ja kodade virvendus, düslipoproteineemia |
|
ja süsteemne erütematoosluupus. |
ATE sümptomid |
|
Sümptomite ilmnemisel tuleb naistele soovitada kohest arsti poole pöördumist ning tervishoiutöötajate teavitamist sellest, et ta kasutab
Tserebrovaskulaarse haiguse sümptomid võivad olla:
-äkki tekkinud tuimus või nõrkus näos, käsivarres või jalas, eriti ühel kehapoolel;
-äkki tekkinud kõndimisraskus, pearinglus, tasakaalu- või koordinatsioonihäired;
-äkki tekkinud segasusseisund, rääkimis- või mõistmisraskus;
-äkki tekkinud nägemishäire ühes või mõlemas silmas;
-äkki tekkinud tugev või pikaajaline teadmata põhjusega peavalu;
-teadvusekaotus või minestamine krampidega või ilma.
Ajutised sümptomid viitavad mööduvale isheemilisele atakile (TIA).
Müokardiinfarkti sümptomid võivad olla:
-valu, ebamugavustunne, survetunne, raskustunne, pigistus- või täistunne rindkeres, käsivarres või rinnaku all;
-ebamugavustunne, mis kiirgub selga, lõuga, kõripiirkonda, käsivarde, kõhtu;
-täistunne, seedehäired või lämbumistunne;
-higistamine, iiveldus, oksendamine või pearinglus;
-äärmine nõrkus, ärevus või õhupuudus;
-kiire või ebakorrapärane südamerütm.
•Kasvajad
Mõned epidemioloogilised uuringud on näidanud, et kombineeritud suukaudsete kontratseptiivide pikaajalistel kasutajatel (> 5 aastat) on emakakaelakasvaja tekkerisk suurenenud, kuid puudub ühtne seisukoht, kui suures osas on need leiud seostatavad seksuaalkäitumise ja muude teguritega, nt inimese papilloomiviirusega (HPV).
54 epidemioloogilise uuringu metaanalüüs näitas, et
Harvadel juhtudel on
Enam kui 50 mikrogrammi etünüülöstradiooli sisaldavate
•Muud seisundid
Kui kestvad nahaärritused (nt plaastri kasutuskoha kestev erüteem või sügelus) esinevad korduvalt isegi kasutuskoha juhistekohasel muutmisel, tuleb kaaluda transdermaalse ravi lõpetamist.
Naistel, kellel on hüpertriglütserideemia või kelle perekonnas see haigus esineb, võib kombineeritud hormonaalsete kontratseptiivide kasutamisel olla suurem risk pankreatiidi tekkeks.
Ehkki paljudel kombineeritud hormonaalsete kontratseptiivide kasutajatel on teatatud vererõhu väikesest tõusust, esineb kliiniliselt olulist tõusu harva. Kui Eileen kasutamise ajal areneb siiski välja kestev kliiniliselt märkimisväärne hüpertensioon, on arstil mõistlik ravimi kasutamine katkestada ja ravida hüpertensiooni. Kui antihüpertensiivse raviga saavutatakse normi piiresse jäävad vererõhu näitajad, võib vajadusel Eileen kasutamist jätkata.
Järgmiste seisundite esinemisest või halvenemisest on teatatud nii raseduse kui
Päriliku angioödeemiga naistel võivad eksogeensed östrogeenid tekitada või süvendada angioödeemi sümptomeid.
Ägedate või krooniliste maksafunktsiooni häirete korral võib osutuda vajalikuks Eileen kasutamise katkestamine, kuni maksafunktsiooni näitajad on jälle normi piirides. Kolestaatilise ikteruse kordumine, mis esmakordselt tekkis raseduse või suguhormoonide varasema kasutamise ajal, muudab vajalikuks Eileen kasutamise katkestamise.
Kuigi
Aeg ajalt võivad tekkida kloasmid, seda eelkõige naistel, kellel on anamneesis raseduspigmendilaigud. Kui patsiendil on soodumus kloasmide tekkeks, tuleks
Erilist tähelepanu tuleb pöörata
Meditsiiniline läbivaatus/konsultatsioon
Enne Eileen’ga alustamist või taasalustamist tuleb naiselt võtta täielik meditsiiniline anamnees (sh perekonna anamnees) ja välistada rasedus. Tuleb mõõta vererõhku ja teostada füüsiline läbivaatus lähtudes vastunäidustustest (vt lõik 4.3) ja hoiatustest (vt lõik 4.4). Oluline on juhtida naise tähelepanu venoosse ja arteriaalse tromboosiga seotud teabele, sh Eileen riskile võrreldes teiste KHK- dega, VTE ja ATE sümptomitele, teadaolevatele riskifaktoritele ja sellele, mida teha tromboosikahtluse korral.
Naisele tuleb rõhutada ravimi pakendi infolehe tähelepaneliku lugemise vajadust ja seal antud soovituste järgmist. Uuringute sagedus ja olemus peavad põhinema kehtivatel ravijuhistel ning neid tuleb kohandada igale naisele eraldi.
Naistele tuleb selgitada, et hormonaalsed rasestumisvastased vahendid ei kaitse
Efektiivsuse vähenemine
Eileen efektiivsus võib väheneda näiteks järgmistel juhtudel:
-kui unustatakse plaaster õigel ajal nahale kinnitada;
-kui plaaster tuleb naha küljest lahti;
-plaastri vahetamise unustamisel (vt lõik 4.2 “ Mida teha lahti tulnud, ununenud või vahetamata jäänud plaastri korral“);
-samaaegselt kasutatavate ravimite tõttu (vt lõik 4.5).
Menstruaaltsüklit reguleeriva toime vähenemine
Kõikide kombineeritud hormonaalsete kontratseptiivide kasutamisel võib tekkida ebaregulaarne veritsemine (määrimine või läbimurde verejooks), eriti esimestel kasutamiskuudel. Sellistel juhtudel tuleb Eileen kasutamist jätkata. Ebaregulaarset veritsemist saab adekvaatselt hinnata alles pärast Eileen ligikaudu kolme tsükli järgset kohanemisperioodi. Pärast seda kohanemisperioodi esines tsüklisisest verejooksu
Amenorröad esines ainult vähestel naistel
Kui ebaregulaarsed vereeritused püsivad või tekivad pärast eelnevaid regulaarseid menstruaaltsükleid, tuleks kahtlustada mittehormonaalseid põhjuseid ja näidustatud on asjakohased diagnostilised meetmed raseduse ja pahaloomulise haiguse välistamiseks. Siia võib kuuluda küretaaž.
Mõnedel naistel ei pruugi plaastrivabal perioodil menstruatsioonilaadset veritsust tekkida. Kui Eileen’t on kasutatud vastavalt lõigus 4.2 kirjeldatud juhistele, on ebatõenäoline, et naine on rasestunud. Kui Eileen’t ei ole siiski enne esimest menstruatsioonilaadset veritsust kasutatud vastavalt nendele juhistele või kui vahele on jäänud kaks veritsust, tuleb enne Eileen kasutamise jätkamist välistada rasedus.
4.5Koostoimed teiste ravimitega ja muud koostoimed
Märkus: võimalike koostoimete tuvastamiseks tuleb tutvuda samaaegselt manustatavate ravimite ravimi omaduste kokkuvõtetega.
Teiste ravimite toimed Eileen’le
Koostoimed võivad esineda ravimitega, mis indutseerides mikrosomaalseid ensüüme võivad suurendada suguhormoonide kliirensit ja põhjustada seeläbi läbimurdeveritsust ja/või kontratseptsiooni ebaõnnestumist.
Kirjanduses on teatatud järgmistest koostoimetest.
Ained, mis suurendavad kombineeritud hormonaalsete kontratseptiivide kliirensit (ensüümide induktsiooni tõttu väheneb
Barbituraadid, bosentaan, karbamasepiin, fenütoiin, primidoon, rifampitsiin, rifabutiin ja
Ravi
Ensüüminduktsiooni võib täheldada juba mõni päev pärast ravi. Maksimaalne ensüüminduktsioon on täheldatav mõne nädala jooksul. Pärast ravi lõpetamist võib ensüüminduktsioon püsida kuni 4 nädalat.
Lühiajaline ravi
Naised, kes saavad ravi ensüümindutseerivate ravimitega, peavad ajutiselt lisaks
Kui kaasnev ravi kestab edasi pärast kolmenädalast plaastri kandmise perioodi, tuleb järgmine plaaster kohe peale panna ilma tavapärase transdermaalse plaastri vaba perioodita.
Pikaajaline ravi
Naistel, kes saavad pikaajalist ravi ensüümindutseerivate ainetega, on soovitatav kasutada mõnda teist usaldusväärset mittehormonaalset kontratseptsiooni.
Ained, millel on erinevad toimed kombineeritud hormonaalsetele kontratseptiividele
Paljud HIV proteaasi inhibiitorite kombinatsioonid ja mittenukleosiidsed pöördtranskriptaasi inhibiitorid, sealhulgas kombinatsioonid HCV- inhibiitoritega, võivad kombineeritud hormonaalsete kontratseptiividega koosmanustamisel kas suurendada või vähendada östrogeeni või progestiini plasmasisaldust. Need muutuste kogumõju võib mõnel juhul olla kliiniliselt oluline.
Seega tuleb tutvuda samaaegselt kasutatavate HIV/HCV ravimite ravimiinfodega, et tuvastada võimalikud koostoimed ja nendest tulenevad soovitused. Kahtluse korral tuleb naistel, kes saavad ravi proteaasi inhibiitoritega või mittenukleosiidsete pöördtranskriptaasi inhibiitoritega, kasutada täiendavat barjäärimeetodit.
Ained, mis suurendavad kombineeritud hormonaalsete kontratseptiivide plasmakontsentratsiooni (ensüümide inhibiitorid)
Etorikoksiibi toimel on suurenenud etünüülöstradiooli plasmasisaldus (50...60%), kui seda on kasutatud samaaegselt koos kolmefaasilise hormonaalse kontratseptiiviga. Arvatakse, et etorikoksiib suurendab etünüülöstradiooli sisaldust, kuna ta inhibeerib sulfotransferaasi aktiivsust ja pärsib seeläbi etünüülöstradiooli metabolismi.
Kombineeritud hormonaalsete kontratseptiivide toimed teistele ravimitele
Kombineeritud hormonaalsed kontratseptiivid võivad mõjutada teatud teiste toimeainete metabolismi. Kontsentratsioonid plasmas või kudedes võivad vastavalt kas suureneda (nt tsüklosporiin) või väheneda (nt lamotrigiin).
Erilist tähelepanu tuleb pöörata
Muud koostoimed
Laboratoorsed analüüsid
Kontratseptiivsete steroidide kasutamine võib mõjutada teatud laboratoorsete analüüside tulemusi, sh maksa, kilpnäärme, neerupealiste ja neerufunktsiooni biokeemilisi näitajaid; (kandja)valkude sisaldust plasmas, nt kortikoide siduva globuliini ja lipiidi/lipoproteiini fraktsioone; süsivesikute ainevahetuse näitajaid ja koagulatsiooni ning fibrinolüüsi näitajaid. Muutused jäävad tavaliselt laboratoorsete analüüside lubatud vahemikku.
Märkus: võimalike koostoimete kindlakstegemiseks tuleb lugeda samaaegselt manustatavate ravimite ravimi omaduste kokkuvõtteid.
4.6Fertiilsus, rasedus ja imetamine
Rasedus
Eileen ei ole näidustatud kasutamiseks raseduse ajal. Kui rasestumine toimub Eileen kasutamise ajal, tuleb plaaster eemaldada ja selle edasine kasutamine lõpetada. Ulatuslikud epidemioloogilised uuringud ei ole siiski näidanud suurenenud sünnidefektide tekkeriski lastel, kelle emad on kasutanud enne rasedust
Sünnitusjärgsel perioodil tuleb arvesse võtta suurenenud VTE riski, kui taasalustatakse Eileen kasutamist (vt lõigud 4.2 ja 4.4).
Imetamine
Kombineeritud hormonaalsed kontratseptiivid võivad mõjutada imetamist, sest võivad vähendada rinnapiima kogust ja muuta selle koostist. Seetõttu ei ole kombineeritud hormonaalsete kontratseptiivide kasutamine soovitatav enne, kui imetav ema on lapse rinnast täielikult võõrutanud. Väike kogus kontratseptiivseid steroide ja/või nende metaboliite võib erituda rinnapiima.
Fertiilsus
Eileen kasutamine ei mõjuta tulevase fertiilsuse kulgu. Eileen eemaldamise järgselt naiste normaalne fertiilsus taastub.
4.7Toime reaktsioonikiirusele
Ravimi toime kohta autojuhtimisele ja masinate käsitsemise võimele ei ole uuringuid läbi viidud. Kombineeritud hormonaalsete kontratseptiivide kasutajatel ei ole täheldatud toimet autojuhtimise ja masinate käsitsemise võimele.
4.8Kõrvaltoimed
Ohutusprofiili kokkuvõte
Kõige sagedamini teada antud kõrvaltoimed Eileen kasutamisel on kasutuskoha reaktsioonid (lööve, sügelus, ärritus, erüteem ja ülitundlikkus). Neid esineb 20,9% kasutajatest. Harva esinevad rasked kõrvaltoimed on arteriaalne ja venoosne trombemboolia.
Kõrvaltoimete koondtabel
Eileen’ga läbi viidud II ja III faasi kliinilistes uuringutes (N = 3573) teada antud kõrvaltoimete esinemissagedused on toodud kokkuvõtvalt allolevas tabelis. Igas esinemissageduse grupis on kõrvaltoimed toodud tõsiduse vähenemise järjekorras. Esinemissagedused on määratletud järgmiselt: väga sage (≥ 1/10), sage (≥ 1/100 kuni < 1/10),
Organs- |
Väga sage |
Sage |
Harv |
|
süsteemi klass |
|
|
|
|
(MedDRA) |
|
|
|
|
Psühhiaatrilised |
|
emotsionaalne |
depressioon / depressiivne |
|
häired |
|
labiilsus |
meeleolu, |
|
|
|
|
libiido vähenemine või |
|
|
|
|
kadumine |
|
Närvisüsteemi |
|
migreen |
|
|
häired |
|
|
|
|
Vaskulaarsed |
|
|
|
venoosne ja |
häired |
|
|
|
arteriaalne |
|
|
|
|
trombemboolia* |
Seedetrakti |
|
iiveldus |
|
|
häired |
|
|
|
|
Naha ja |
kasutuskoha |
|
|
|
nahaaluskoe |
reaktsioon |
|
|
|
kahjustused |
|
|
|
|
Reproduktiivse |
|
veritsus |
|
|
süsteemi ja |
|
suguteedes**, |
|
|
rinnanäärme |
|
rindade |
|
|
häired |
|
valulikkus |
|
|
Kõrvaltoimeid kodeeriti kliinilistes uuringutes vastavalt MedDRA sõnastikule (versioon 14.1). Teatud reaktsiooni ja selle sünonüümide ning sellega seotud seisundite kirjeldamiseks on kasutatud MedDRA eelistermineid. Tegeliku toime vähendamise või hägustamise vältimiseks on sama meditsiinilist fenomeni esindavad MedDRA erinevad terminid rühmitatud kokku üheks kõrvaltoimeks.
* Hinnanguline esinemissagedus kombineeritud suukaudsete kontratseptiivide rühma hõlmavatest epidemioloogilistest uuringutest. Esinemissagedus oli määratluse väga harv piirväärtuse lähedal.
- Venoosne ja arteriaalne trombemboolia hõlmab järgmisi meditsiinilisi juhte:
süvaveeni perifeerne oklusioon, tromboos ja emboolia / kopsuveresoone oklusioon, tromboos, emboolia ja infarkt/ müokardiinfarkt/ajuinfarkt ja
** Sisaldab meditsiinilisi seisundeid: veritsus naiste suguteedes, ootamatu emakaverejooks
Valitud kõrvaltoimete kirjeldus
Allpool on loetletud
Vereringe häired
•
isheemilise ataki, venoosse tromboosi ja kopsuemboolia tekkeks. Neid seisundeid on põhjalikumalt kirjeldatud lõigus 4.4.
Kasvajad
•Rinnavähi diagnooside esinemissagedus on kombineeritud hormonaalsete kontratseptiivide kasutajate seas veidi suurem. Kuna rinnavähki esineb alla
•Maksakasvajad (hea- ja pahaloomulised).
Muud seisundid
•Nodoosne erüteem, multiformne erüteem.
•Hüpertriglütserideemiaga naistel on kombineeritud suukaudsete kontratseptiivide kasutamisel suurem pankreatiidi tekkerisk.
•Hüpertensioon.
•Haigusseisundite tekkimine või süvenemine, mille puhul seos kombineeritud suukaudsete kontratseptiivide kasutamisega ei ole kindel: kolestaasiga seotud kollatõbi ja/või sügelus; sapikivide moodustumine; porfüüria; süsteemne erütematoosluupus;
•Päriliku angioödeemiga naistel võivad eksogeensed östrogeenid tekitada või süvendada angioödeemi sümptomeid.
•Maksafunktsiooni häired.
•Muutused glükoositaluvuses või toimed perifeersele insuliiniresistentsusele.
•Crohni tõve ja haavandilise koliidi süvenemine.
•Epilespia süvenemine.
•Kloasmid.
•Ülitundlikkus (sh sümptomitena lööve, nõgestõbi).
Koostoimed
Võimalikest kõrvaltoimetest teavitamine
Ravimi võimalikest kõrvaltoimetest on oluline teavitada ka pärast ravimi müügiloa väljastamist. See võimaldab jätkuvalt hinnata ravimi kasu/riski suhet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest kõrvaltoimetest www.ravimiamet.ee kaudu.
4.9Üleannustamine
Kombineeritud suukaudsete kontratseptiivide kasutamise üldise kogemuse alusel võivad üleannustamisel tekkida järgmised sümptomid: iiveldus, oksendamine ja noortel tüdrukutel kerge menstruatsioonilaadne veritsus. Antidoodid puuduvad, edasine ravi peab olema sümptomaatiline. Täiendavad või valesti paigaldatud plaastrid tuleb nahalt eemaldada.
5. FARMAKOLOOGILISED OMADUSED
5.1Farmakodünaamilised omadused
Farmakoterapeutiline rühm: Suguhormoonid ja genitaalsüsteemi modulaatorid; gestageenide ja östrogeenide fikseeritud kombinatsioonid
Toimemehhanism
Kombineeritud hormonaalsete kontratseptiivide rasestumisvastane toime põhineb mitmete tegurite vastastikusel toimel, millest kõige olulisemad on ovulatsiooni pärssimine ja muutused emakakaela sekreedis.
Kliiniline efektiivsus ja ohutus
Euroopa Liidus,
Pearli indeks (vanus 18...35 aastat, kehamassiindeks ≤ 30 kg/m)
Meetodi viga: |
Pearli indeks 0,82 (ülemine 95% usalduspiir 1,55) |
Meetodi ja kasutaja viga: |
Pearli indeks 1,19 (ülemine 95% usalduspiir 2,00) |
Euroopa elanikkonna kohta arvutati välja järgmised Pearli indeksid:
Pearli indeks (vanus 18...35 aastat, kehamassiindeks ≤ 30 kg/m)
Meetodi viga: |
Pearli indeks 0,40 (ülemine 95% usalduspiir 1,18) |
Meetodi ja kasutaja viga: |
Pearli indeks 0,76 (ülemine 95% usalduspiir 1,66) |
Meetodi viga: |
Pearli indeks 2,91 (ülemine 95% usalduspiir 4,41) |
Meetodi ja kasutaja viga: |
Pearli indeks 3,92 (ülemine 95% usalduspiir 5,53) |
Eileen valesti kasutamisel võib kontratseptsiooni ebaõnnestumise tõenäosus suureneda.
Ühes kliinilises uuringus uuriti
5.2Farmakokineetilised omadused
Imendumine
Pärast Eileen nahale kandmist imenduvad etünüülöstradiool ja gestodeen hästi läbi naha. Keskmiselt saavutatakse Eileen
Etünüülöstradiooli ja gestodeeni sisaldust seerumis määrati erinevate ravitsüklite (1. kuni 7. tsükkel) kolmandal nädalal. Etünüülöstradiooli keskmine maksimaalne plasmatase (vahemikus 36...51 ng/l) saavutati ligikaudu üks päev pärast plaastri nahale kinnitamist. Seejärel vähenes etünüülöstradiooli plasmatase ühenädalase kasutusaja lõpuks keskmise minimaalse väärtuseni vahemikus 15...23 ng/l. Keskmine plasmatase 3. nädalal oli vahemikus 22...33 ng/l.
Gestodeeni keskmine maksimaalne plasmakontsentratsioon (vahemikus 4,7...7,5 µg/l) saavutati ligikaudu 1...1,5 päeva pärast plaastri nahale kinnitamist. Seejärel vähenes gestodeeni plasmatase ühenädalase kasutusaja lõpuks keskmise minimaalse väärtuseni vahemikus 2,6...4,0 µg/l. Keskmine plasmatase 3. nädalal oli vahemikus 3,6...5,7 µg/l.
Kehakaalu ja kehamassiindeksi mõju
Etünüülöstradiooli ja gestodeeni plasmakontsentratsioon
Kuumuse, niiskuse, füüsilise koormuse ja kasutuskoha mõju
Etünüülöstradiooli ja gestodeeni farmakokineetikat Eileen’i kasutamisel uuriti kindlates kuumuse, niiskuse ja füüsilise koormuse tingimustes (st sauna, mullivanni kasutamisel, ujudes ja erinevatel füüsilistel koormustel). Saadud andmeid võrreldi tavatingimustega. Erilistes tingimustes olid üldiselt etünüülöstradiooli ja gestodeeni CMAX ja AUC bioekvivalentsed. Tulemused näitavad, et erilistes tingimustes (nt spordiklubis sauna ja mullivanni kasutamisel, ujudes või erinevate füüsiliste koormuste korral) ei esine kliiniliselt olulisi erinevusi etünüülöstradiooli ja gestodeeni plasmatasemes, võrrelduna igapäevaste tavatingimustega.
Ametlikus farmakokineetika uuringus (lahterdamata analüüs), kus kasutati kolme erinevat manustamiskohta, olid gestodeeni ja etünüülöstradiooli plasmatasemed vastavalt 24% ja 31% võrra kõrgemad, kui plaaster oli kinnitatud õlavarre välisküljele, võrreldes tuharatele ja kõhule kinnitamisega. Plasmatasemete väärtused kattusid kõigi kolme kasutuskoha puhul suurel määral. Populatsiooni farmakokineetika analüüsil (metaanalüüs), oli etünüülöstradiooli plasmataseme geomeetriline keskmine (AUC
Transdermaalse Eileen ja kombineeritud suukaudse kontratseptiivi võrdlusandmed
Suhtelise biosaadavuse uuringus olid Eileen kasutamisel etünüülöstradiooli ja gestodeeni püsikontsentratsiooni plasmatasemed ja farmakokineetilised parameetrid võrreldavad 0,020 mg etünüülöstradiooli ja 0,075 mg gestodeeni sisaldava kombineeritud suukaudse kontratseptiiviga. Etünüülöstradiooli ja gestodeeni keskmise püsikontsentratsiooni
Jaotumine
Etünüülöstradiool seondub ulatuslikult, kuid mittespetsiifiliselt seerumi albumiiniga (ligikaudu 98%), kuid mitte
Biotransformatsioon
Etünüülöstradiool (EE) metaboliseerub peamiselt aromaatse hüdroksülatsiooni kaudu, kus moodustuvad paljud erinevad hüdroksüülitud ja metüülitud metaboliidid, mis esinevad vabade metaboliitidena ja glükuroniidide ning sulfaatide konjugaatidena. Etünüülöstradiooli peamine metabolismirada on
Gestodeen metaboliseerub täielikult üldiselt polaarsemateks metaboliitideks. Gestodeeni metabolismi iseloomustab hüdroksüülimine steroidi tuuma erinevates kohtades ning
CYP3A4 inhibiitorite (ketokonasool, erütromütsiin) toimet uurivas kahes uuringus ei mõjutanud kumbki kahest inhibiitorist püsikontsentratsiooni tingimustes etünüülöstradiooli plasmataset. Gestodeeni kasutamisel põhjustas inhibiitorite koosmanustamine
Uuringus, kus jälgiti Eileen toimet ühekordselt manustatavale midasolaamile (CYP3A4 poolt metaboliseeritavate ainete mudelsubstraat), ei täheldatud midasolaami plasmasisalduse kliiniliselt olulist suurenemist. Midasolaamiga koosmanustamine põhjustas midasolaami
Eritumine
Etünüülöstradiool ei eritu märkimisväärselt muutumatul kujul. Etünüülöstradiooli metaboliidid erituvad kuse- ja sapiteede kaudu suhtes 4:6. Plasmataseme vähenemist iseloomustavad vähemalt kaks dispositsioonifaasi, lõpliku poolväärtusajaga ligikaudu 16 tundi (määrati kindlaks pärast intravenoosset manustamist, kaks päeva pärast plaastri eemaldamist ei olnud kontsentratsioon mõõdetav).
Gestodeen ei eritu muutumatul kujul. Selle metaboliidid erituvad kuse- ja sapiteede kaudu suhtes 6:4. Pärast plaastri eemaldamist väheneb gestodeeni plasmatase aeglasemalt kui etünüülöstradioolil, keskmise lõpliku poolväärtusajaga ligikaudu 26 tundi.
Lineaarsus/mittelineaarsus
Etünüülöstradiooli farmakokineetika on lineaarne annusevahemikus 0,020 mg kuni 0,100 mg. Etünüülöstradiooli farmakokineetika kliiniliselt olulist muutumist ajas ei täheldatud.
Gestodeeni farmakokineetika sõltub SHBG kontsentratsioonist, mida mõjutavad östrogeenid, androgeenid ja ka gestodeen. Pärast Eileen korduvat nahale kinnitamist täheldati SHBG sisalduse 3- kuni
Erirühmad
Sugu
Eileen on näidustatud kasutamiseks ainult naistel.
Eakad naised
Eileen ei ole näidustatud kasutamiseks pärast menopausi.
Kehamassiindeks
Andmeid kontratseptiivse efektiivsuse kohta naistel kehamassiindeksiga > 30 kg/m2 on piiratud hulgal.
Neerufunktsiooni kahjustus
Eileen’t ei ole uuritud neerufunktsiooni kahjustusega naistel. Kuna etünüülöstradiool ja gestodeen metaboliseeruvad täielikult enne eritumist inaktiivseteks metaboliitideks ja on olemas ka teine eritumistee (maksa kaudu), siis eeldatavalt ei ole neerukahjustusega naistel risk suurenenud.
Maksafunktsiooni kahjustus
Eileen’t ei ole maksakahjustusega naistel uuritud. Eileen on vastunäidustatud naistele, kellel on või on varem olnud tõsine maksahaigus, kui maksafunktsiooni näitajad ei ole normaliseerunud. Vt ka
lõik 4.3.
Etnilised erinevused
Etünüülöstradiooli farmakokineetikat uuriti kombinatsioonis teise progestiiniga europiididel, Hiina ja Jaapani naistel. Ühtegi kliiniliselt olulist erinevust ei ilmnenud. Eileen farmakokineetikat ei ole eraldi uuritud erineva etnilise taustaga naistel. Ei ole teada ühtegi polümorfset ensüümi, mis osaleks suurel määral gestodeeni metaboliseerimises. Olemasolevad andmed europiidide, mustanahaliste ja hispaanlannade kohta ei osuta ühelegi erinevusele Eileen farmakokineetikas erinevasse rassi või etnilisse tausta kuuluvate naiste puhul. Asiaatide kohta on andmeid väga piiratud hulgal.
Suitsetamine
Ei ole ühtegi viidet sellele, et suitsetamine võiks mõjutada etünüülöstradiooli ja gestodeeni farmakokineetikat.
Lapsed
Ohutus ja efektiivsus alla
5.3Prekliinilised ohutusandmed
Toimeainete mittekliinilistest uuringutest saadud korduvtoksilisuse, genotoksilisuse, paikse taluvuse, kartsinogeensuse ja reproduktsioonitoksilisuse prekliinilised andmed ei ole näidanud konkreetseid riske inimesele. Siiski tuleb arvestada sellega, et suguhormoonid võivad soodustada teatud hormoontundlike kudede ja kasvajate kasvu. Bioloogilise sobivuse uuringud plaastri ja selles sisalduvate materjalidega ei ole näidanud konkreetseid riske inimesele plaastri paikse ja süsteemse ohutuse osas.
Keskkonnariski hindamine
Gestodeen ja etünüülöstradiool võivad olla ohtlikud keskkonnale, eriti kaladele. Gestodeen ja etünüülöstradiool on keskkonnas püsivad. Kõik kasutatud või kasutamata plaastrid tuleb ära visata vastavalt kohalikele nõuetele. Kahtluse korral tuleb küsida nõu apteekrilt (vt lõik 6.6).
6. FARMATSEUTILISED ANDMED
6.1Abiainete loetelu
Väliskiht:
madala tihedusega polüetüleenist (PE) väliskiht.
Adhesiivne kiht:
adhesiivne aine, mille koostisse kuuluvad: hüdrogeenitud vaigu ester,
polübuteen,
polüisobutüleen,
pentaerütritool tetrakis
Vahekile:
polüetüleentereftalaadist (PET) kile.
Adhesiivne maatriks:
adhesiivne aine, mille koostisse kuuluvad: hüdrogeenitud vaigu ester,
polübuteen,
polüisobutüleen,
pentaerütritool tetrakis
Toimeainet vabastav kiht:
silikoonitud polüetüleentereftalaadist (PET) kile.
6.2Sobimatus
Ei kohaldata.
6.3Kõlblikkusaeg
3 aastat.
6.4Säilitamise eritingimused
Hoida originaalkotikeses, valguse ja niiskuse eest kaitstult.
6.5Pakendi iseloomustus ja sisu
Sisepakend
Kotike koosneb neljast kihist: madala tihedusega polüetüleenkilest (kõige sisemine kiht), alumiiniumfooliumist, paberikihist ja polüetüleentereftalaatkilest.
Vaheleht, mis hoiab ära transdermaalse plaastri kleepumise kotikese seinte külge, on valmistatud silikoonitud polüetüleentereftalaadist.
Välispakend
Kotikesed on märgistatud ja pakendatud koos brošüüriga (sisaldab meelespeakaarti ja
Iga kartongkarp sisaldab eraldi kotikestes 3, 9 või 18 Eileen transdermaalset plaastrit.
Kõik pakendi suurused ei pruugi olla müügil.
6.6Erihoiatused ravimpreparaadi hävitamiseks ja käsitlemiseks
Plaaster tuleb kohe pärast kotikesest välja võtmist nahale kinnitada.
Vältimaks Eileen kleepuvuse vähenemist ei tohi plaastri kinnitamise kohale kanda jumestusvahendeid, kreeme, ihupiima, pulbreid ega muid paikseid nahahooldusvahendeid.
Gestodeen ja etünüülöstradiool võivad olla ohtlikud keskkonnale, eriti kaladele. Gestodeen ja etünüülöstradiool on keskkonnas püsivad. Kasutatud plaastreid ei tohi visata
Originaalkotike tuleb alles hoida kasutatud plaastri ära viskamiseks. Kasutatud plaaster tuleb voltida pooleks nii, et kleepuvad pooled jäävad sissepoole. Kokkuvolditud plaaster tuleb panna originaalkotikesse, misjärel tuleb voltida kokku selle avatud serv.
Kotikese peal on kahest lehest koosnev silt. Sildi esimene leht tuleb ära tõmmata ja kleepida sellega kinni kotikese kokkuvolditud serv. Teisel lehel on juhised plaastri äraviskamiseks.
Plaaster tuleb visata ära ohutult, lastele või lemmikloomadele kättesaamatusse kohta.
Kõik kasutatud või kasutamata plaastrid tuleb ära visata vastavalt kohalikele nõuetele. Kahtluse korral küsige nõu apteekrilt.
7. MÜÜGILOA HOIDJA
Gedeon Richter Plc.
Gyömrõi ut
Ungari
8. MÜÜGILOA NUMBER (NUMBRID)
9. ESMASE MÜÜGILOA VÄLJASTAMISE/MÜÜGILOA UUENDAMISE KUUPÄEV
Müügiloa esmase väljastamise kuupäev: 31.03.2014
10. TEKSTI LÄBIVAATAMISE KUUPÄEV
Veebruar 2017
